Bệnh Học, Bệnh tim mạch
Hội chứng Brugada ( lịch sử, dịch tế, chẩn đoán, quản lý)
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Tác giả : John Larkin và Mike Cadogan
Lịch sử hội chứng Brugada
Hội chứng Brugada là một bất thường về điện tâm đồ với tỷ lệ đột tử cao ở những bệnh nhân có cấu trúc tim bình thường.
Được mô tả lần đầu tiên vào năm 1992 bởi anh em nhà Brugada, căn bệnh này đã tăng theo cấp số nhân về số ca bệnh được báo cáo. Tuổi đột tử trung bình là 41, với tuổi chẩn đoán từ 2 ngày đến 84 tuổi.
Tỷ lệ mắc bệnh cao ở Đông Nam Á nơi trước đây được gọi là Hội chứng đột tử không rõ nguyên nhân về đêm (SUNDS).
Trước đây được biết đến một cách thông tục ở Philippines là bangungut (‘trỗi dậy và rên rỉ trong giấc ngủ’); ở Nhật Bản là pokkuri (‘hiện tượng ngừng đột ngột và bất ngờ’) và ở Thái Lan là Lai Tai (‘chết trong khi ngủ’).
Dịch tễ
- Nam> Nữ theo tỷ lệ 8 – 10: 1
- Tuổi từ 20 đến 40 (Có báo cáo trường hợp tuổi từ 2 ngày đến 84 tuổi)
- Dân số Châu Á> Hoa Kỳ
- Thường xảy ra vào ban đêm, khi có hoạt động âm đạo chiếm ưu thế
Hội chứng Brugada phổ biến như thế nào?
- Trên toàn thế giới có 4 – 12% tổng số ca tử vong đột ngột
- Brugada loại 1 xảy ra ở 12 / 10.000 người 1
- Brugada loại 2 và 3 xảy ra ở 58 / 10.000 người 1
- Tỷ lệ phổ biến ECG kiểu Brugada: Châu Á (0,36%), Châu Âu (0,25%) và ở Mỹ (0,03%) 2
- Mô hình điện tâm đồ có thể sáp và suy yếu, làm cho tỷ lệ mắc bệnh thực sự bị đánh giá thấp
Hội chứng Brugada nguy hiểm ra sao?
- Ngừng tim: nếu không được hỗ trợ lập tức, người bệnh có thể ngừng tim đột ngột, ngừng thở và mất ý thức. Mặc dù thường xảy ra khi ngủ và có tỷ lệ tử vong cao nhưng nếu được cấp cứu nhanh chóng và chính xác, người bệnh có thể vẫn được cứu sống.
- Ngất: nếu bệnh nhân đã từng được chẩn đoán hội chứng Brugada và bị mệt, ngất, cần gọi điện cấp cứu ngay lập tức.
Cơ sở dễ gây rối loạn nhịp tim nhất của Hội chứng Brugada là ở đâu?
- Đường đi ra ngoài tâm thất phải (RVOT)
- Chỉ cấu trúc tim nằm bên dưới khoang liên sườn thứ 2 và 3
- Hình thái Brugada có thể vắng mặt trong không gian liên sườn thứ 4 điển hình của các đạo trình V1 – V3
- Một số loại thuốc có thể gây ra VF / VT
Cách tốt nhất để phân tầng nguy cơ bệnh nhân bị Hội chứng Brugada là gì?
- Những bệnh nhân có triệu chứng bị ngất tái phát, hô hấp dồn dập vào ban đêm khi ngủ hoặc co giật không rõ nguyên nhân có nguy cơ tử vong cao nhất
- Bệnh nhân không có triệu chứng có tỷ lệ biến cố tim hàng năm là 0,25%, do đó, chiến lược phân tầng nguy cơ để xác định bệnh nhân có nguy cơ cao là rất ít giá trị.
Các điểm chính của hội chứng Brugada
- Thực sự chỉ có một loại hội chứng Brugada.
- Chẩn đoán phụ thuộc vào kết quả ECG đặc trưng VÀ tiêu chí lâm sàng.
- Phân tầng rủi ro hơn nữa đang gây tranh cãi.
- Điều trị dứt điểm = ICD.
- Dấu hiệu Brugada cô lập có ý nghĩa đáng nghi vấn.
Căn nguyên của hội chứng Brugada
Nguyên nhân Hội chứng Brugada gây ra chủ yếu do đột biến ở gen SCN5A mã hóa tiểu đơn vị α của Nav1.5 phân áp điện áp, kênh natri tim chịu trách nhiệm điều chỉnh dòng natri nhanh –INa-. Nó gây ra sự rối loạn hoạt động của các tiểu đơn vị kênh natri hoặc protein điều chỉnh chúng. Rối loạn chức năng của các kênh natri dẫn đến tắc nghẽn dẫn truyền cục bộ trong tim. Hiện tại, hơn 250 đột biến liên quan đến BrS đã được báo cáo ở 18 gen khác nhau ( SCN5A, SCN1B, SCN2B, SCN3B, SCN10A, ABCC9, GPD1L, CACNA1C, CACNB2, CACNA2D1, KCND3, KCNE3, KCNE1L-KCNE5-4, KCNJ8, HCNE5-, KCNJ8, HCN RANGRF, SLMAP và TRPM4 ), mã hóa cho các kênh natri, kali và canxi hoặc protein liên kết với các kênh này. Mặc dù xác định được 18 gen liên quan, 65% –70% các trường hợp được chẩn đoán lâm sàng vẫn không có nguyên nhân di truyền xác định được. Hầu hết các đột biến này được di truyền theo kiểu trội trên NST thường từ cha mẹ sang con cái của họ. Điều này có nghĩa là chỉ một bản sao duy nhất của gen bất thường là cần thiết cho sự xuất hiện của bệnh ở một cá nhân. Hầu hết các cá nhân mắc bệnh cũng có cha hoặc mẹ bị ảnh hưởng. Mỗi đứa trẻ của một cá thể bị ảnh hưởng có 50% cơ hội thừa hưởng biến thể di truyền, bất kể giới tính của cá thể đó. Gen chính được biết là có liên quan đến hội chứng Brugada nằm trên nhiễm sắc thể số 3 và được gọi là gen SCN5A . Khoảng 15% -30% cá nhân mắc hội chứng Brugada có đột biến gen SCN5A . Gen này chịu trách nhiệm sản xuất một loại protein cho phép di chuyển các nguyên tử natri vào tế bào cơ tim thông qua một kênh gọi là kênh natri. Sự bất thường trong gen SCN5A làm thay đổi cấu trúc hoặc chức năng của kênh natri và dẫn đến giảm natri vào tế bào tim. Lượng natri giảm có thể dẫn đến nhịp tim bất thường có thể dẫn đến đột tử. SCN5A _đột biến gen cũng liên quan đến hội chứng QT dài loại 3 (LQT3), là một dạng của bất thường nhịp tim được gọi là hội chứng Romano-Ward. Một số gia đình đã được báo cáo rằng có người thân mắc hội chứng Brugada và LQT3, cho thấy rằng những tình trạng này có thể là các dạng rối loạn khác nhau của cùng một loại rối loạn.
Tóm lại, hội chứng Brugada là do đột biến gen kênh natri tim. Đây thường được gọi là bệnh kênh natri. Hơn 60 đột biến khác nhau đã được mô tả cho đến nay và ít nhất 50% là đột biến tự phát, nhưng sự di truyền theo nhóm gia đình và di truyền trội trên NST thường đã được chứng minh.
Những thay đổi điện tâm đồ có thể thoáng qua với hội chứng Brugada và cũng có thể được tiết lộ hoặc tăng thêm bởi nhiều yếu tố:
- Sốt
- Thiếu máu cục bộ
- Nhiều loại thuốc
- Hạ kali máu
- Hạ thân nhiệt
- Post DC cardioversion
Tiêu chuẩn chẩn đoán
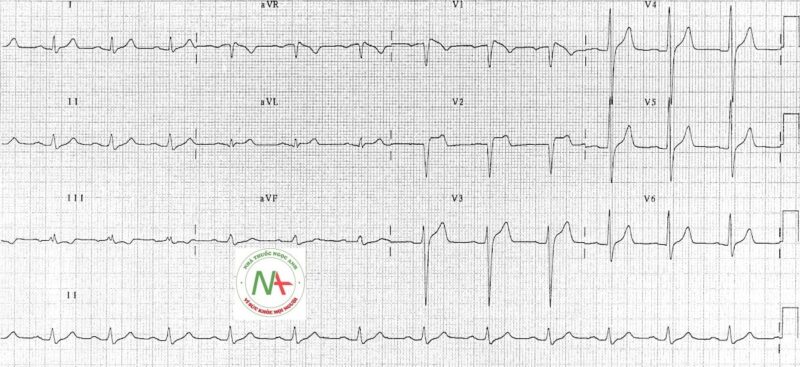
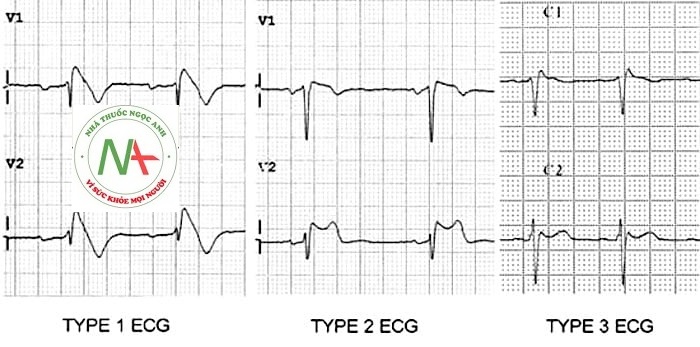
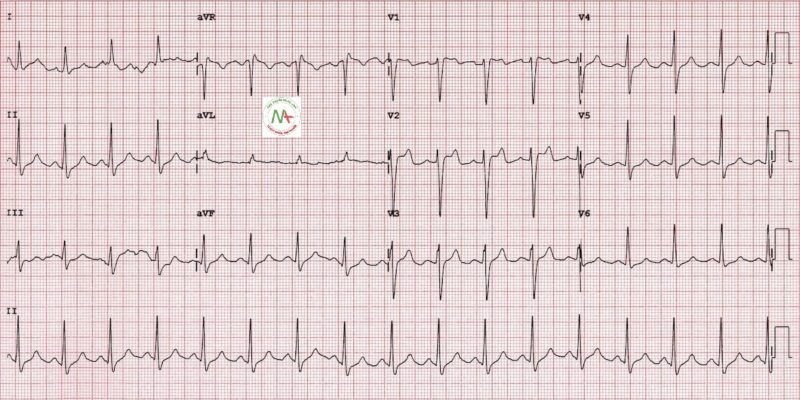
Loại 1
- Đoạn ST chênh lên> 2mm trong> 1 của V1-V3 theo sau là sóng T âm.
- Đây là bất thường điện tâm đồ duy nhất có khả năng chẩn đoán.
- Nó thường được gọi là dấu hiệu Brugada .
Bất thường điện tâm đồ này phải được kết hợp với một trong các tiêu chuẩn lâm sàng sau để chẩn đoán:
- Rung thất được ghi nhận (VF) hoặc nhịp nhanh thất đa hình (VT).
- Tiền sử gia đình đột tử do tim khi <45 tuổi.
- Điện tâm đồ kiểu coved ở các thành viên trong gia đình.
- Tính vô cảm của VT với kích thích điện được lập trình.
- Ngất.
- Hô hấp giao động về đêm.
Hai loại Brugada khác không phải là chẩn đoán nhưng có thể cần được điều tra thêm (xem thảo luận bên dưới).
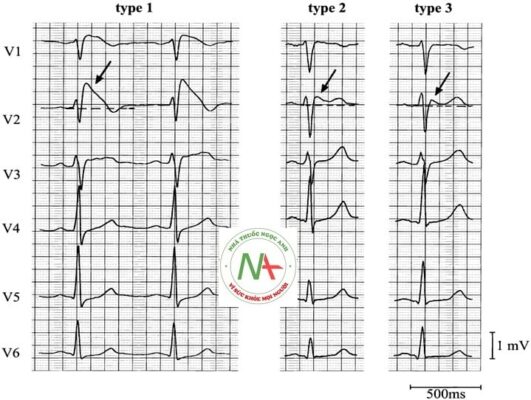
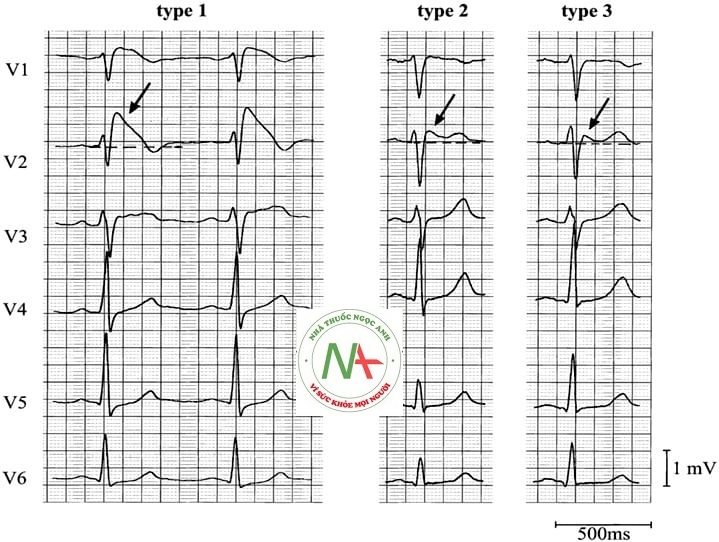
Loại 2
- Brugada Loại 2 có ST chênh lên hình yên ngựa> 2mm.
 Loại 3
Loại 3
- Brugada type 3: có thể là hình thái của type 1 hoặc type 2, nhưng với <2mm đoạn ST chênh lên.
Quản lý
Liệu pháp duy nhất đã được chứng minh là máy khử rung tim cấy ghép (ICD). Quinidine đã được đề xuất như một giải pháp thay thế ở những nơi không có sẵn ICD hoặc những nơi không phù hợp (ví dụ: trẻ sơ sinh).
Hội chứng Brugada chưa được chẩn đoán đã được ước tính có tỷ lệ tử vong là 10% mỗi năm. Điều này có nghĩa là chẩn đoán trong ED bắt buộc phải nhập học? Có thể có đối với tất cả bệnh nhân loại 1 nếu họ có các tiêu chí lâm sàng gợi ý.
Có thể thích hợp để phân tầng nguy cơ trên cơ sở bệnh nhân ngoại trú với một nghiên cứu điện sinh lý học (EPS) để xem liệu bệnh nhân có nhịp nhanh thất (VT) hoặc rung thất (VF) trong các cơ sở sau:
- Bệnh nhân không có triệu chứng với kiểu điện tâm đồ loại 1.
- Tất cả các mẫu điện tâm đồ loại 2 + 3.
Tuy nhiên, điều này còn gây tranh cãi với nhiều cuộc tranh luận trong các tài liệu khác nhau, từ ngưỡng rất thấp cho các nghiên cứu về EPS và chèn ICD (Brugada và cộng sự) đến các cách tiếp cận thận trọng hơn. Một trong những vấn đề là EPS khác xa so với tiêu chuẩn vàng, với giá trị dự đoán âm dưới 50% và một số nghiên cứu cho thấy rằng chúng ta có thể hơi quá phấn khích về phát hiện ECG được mô tả tương đối gần đây này.
Phải thừa nhận rằng quy mô nghiên cứu là khá nhỏ – nhưng một nghiên cứu đã theo dõi 98 bệnh nhân Nhật Bản không có triệu chứng với ‘dấu hiệu Brugada’ trên điện tâm đồ thường quy trong 7,8 năm và cho thấy họ không có tỷ lệ tử vong cao hơn phần còn lại của một nhóm thuần tập 14000 mạnh mẽ. Điều này làm nổi bật tầm quan trọng của các tiêu chuẩn lâm sàng cần thiết để chẩn đoán được liệt kê ở trên.
Đánh giá dược lý đã được đề xuất bởi một số trong các mẫu Loại 2 + 3, nếu nghi ngờ hội chứng Brugada trên lâm sàng – việc sử dụng thuốc ngăn chặn kênh natri có thể chuyển các dạng không chẩn đoán này thành dạng chẩn đoán 1, tuy nhiên độ nhạy của xét nghiệm này vẫn chưa được biết và Có vẻ như phân nhóm này có tỷ lệ tử vong cực kỳ thấp / không gia tăng khi so sánh với dân số chung.
Nguồn tham khảo:
- Moustafa El Sayed; Amandeep Goyal; Avery L. Callahan., Brugada Syndrome, NCBI. truy cập ngày 18/9/2022
- Sarquella-Brugada G, Campuzano O, Arbelo E, Brugada J, Brugada R. Brugada syndrome: clinical and genetic findings. Genet Med. 2016 Jan;18(1):3-12.truy cập ngày 18/9/2022
- Sieira J, Dendramis G, Brugada P. Pathogenesis and management of Brugada syndrome. Nat Rev Cardiol. 2016 Dec;13(12):744-756. truy cập ngày 18/9/2022.
- Louis C, Calamaro E, Vinocur JM. Hereditary arrhythmias and cardiomyopathies: decision-making about genetic testing. Curr Opin Cardiol. 2018 Jan;33(1):78-86.


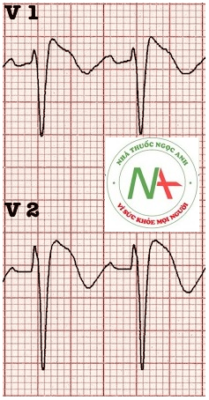
 Loại 3
Loại 3