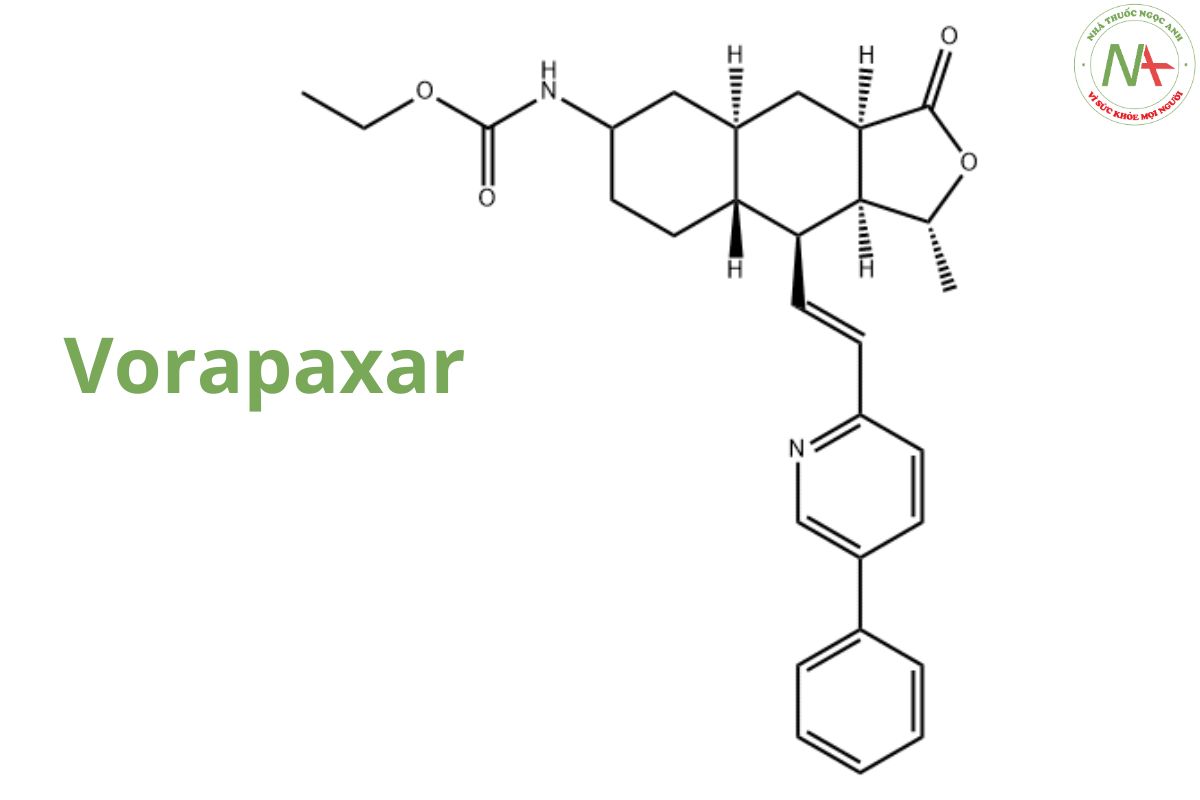
Vorapaxar
Biên soạn và Hiệu đính
Dược sĩ Xuân Hạo
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
EthylN-[(1R,3aR,4aR,6R,8aR,9S,9aS)-9-[(E)-2-[5-(3-fluorophenyl)pyridin-2-yl]ethenyl]-1-methyl-3-oxo-3a,4,4a,5,6,7,8,8a,9,9a-decahydro-1H-benzo[f][2]benzofuran-6-yl]carbamate.
Nhóm thuốc
Chất đối kháng thụ thể Thrombin
Mã ATC
B — Máu và các cơ quan tạo máu
B01 — Thuốc chống nhiễm mạch
B01A — Tác nhân chống nhiễm mạch
B01AC — Chất ức chế kết tập tiểu cầu ngoại trừ heparin
B01AC26 — Vorapaxar
Mã UNII
ZCE93644N2
Mã CAS
618385-01-6
Cấu trúc phân tử
Công thức phân tử
C29H33FN2O4
Phân tử lượng
492.6 g/mol
Cấu trúc phân tử
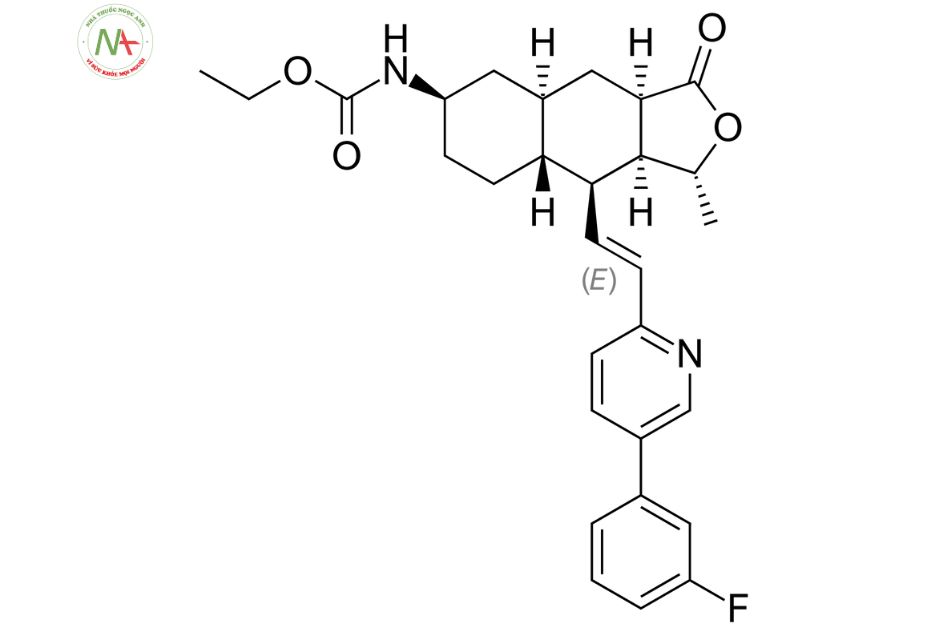
Vorapaxar là một este carbamate là este etyl của [(1R,3aR,4aR,6R,8aR,9S,9aS)-9-{(E)-2-[5-(3-fluorophenyl)pyridin-2-yl axit ]ethynyl}-1-methyl-3-oxododecahydronaphtho[2,3-c]furan-6-yl]carbamic. Nó là thành viên của pyridin, este carbamate, hợp chất flo hữu cơ, naphthofuran và một lacton. Nó là cơ sở liên hợp của vorapaxar(1+).
Các tính chất phân tử
Số liên kết hydro cho: 1
Số liên kết hydro nhận: 6
Số liên kết có thể xoay: 6
Diện tích bề mặt tôpô: 77,5 Ų
Số lượng nguyên tử nặng: 36
Các tính chất đặc trưng
LogP: 5.39
Sinh khả dụng: ~100%
Khả năng liên kết protein:>=99%
Thời gian bán hủy: 5-13%
Cảm quan
Không có thông tin
Dạng bào chế
Viên nén hàm lượng 2.5mg (tương đương 2.08mg Vorapaxar)
Độ ổn định và điều kiện bảo quản của Vorapaxar
Vorapaxar có thể được bảo quản ở 20–25 °C (68–77 °F). Tốt nhất là bảo quản vorapaxar trong bao bì gốc với chai được đóng chặt và tránh ẩm.
Nguồn gốc
Vorapaxar (tên thương hiệu Zontivity , trước đây gọi là SCH 530348 ) là một chất đối kháng thụ thể thrombin ( protease-activated receptor , PAR-1) dựa trên sản phẩm tự nhiên himbacine , được phát hiện bởi Schering-Plough và được phát triển bởi Merck & Co.
Vào tháng 1 năm 2011, các thử nghiệm lâm sàng do Merck tiến hành đã bị tạm dừng đối với những bệnh nhân bị đột quỵ và bệnh tim nhẹ do xuất huyết não ngày càng nhiều.
Vorapaxar đã được khuyến nghị để FDA chấp thuận vào ngày 15 tháng 1 năm 2014.
Vào ngày 5 tháng 5 năm 2014, vorapaxar đã được FDA chấp thuận.
Dược lý và cơ chế hoạt động
Để ngăn chặn sự kết tập tiểu cầu do hoạt động protease serine của thrombin, Vorapaxar ức chế PAR-1, một thụ thể kết hợp G-protein được biểu hiện cao trên tiểu cầu và được kích hoạt bởi thrombin để điều hòa phản ứng huyết khối. Vorapaxar không chỉ ngăn chặn sự kết tập tiểu cầu do thrombin gây ra, mà còn ngăn chặn sự kết tập tiểu cầu do TRAP gây ra. Tuy nhiên, Vorapaxar không ức chế sự kết tập tiểu cầu do các chất chủ vận khác như ADP, collagen hoặc chất tương tự thromboxane.
Ngoài ra, vorapaxar ức chế kết tập tiểu cầu do peptide chủ vận thụ thể thrombin (TRAP) gây ra mà không ảnh hưởng đến các thông số đông máu. Vorapaxar không ức chế kết tập tiểu cầu gây ra bởi các chất chủ vận khác như adenosine diphosphate (ADP), collagen hoặc chất bắt chước thromboxane.
Với liều 2,5 mg vorapaxar sulfat (tương đương với 2,08 mg vorapaxar) mỗi ngày, vorapaxar luôn đạt được hiệu quả ức chế ≥80% kết tập tiểu cầu do TRAP gây ra trong vòng một tuần kể từ khi bắt đầu điều trị. Thời gian ức chế tiểu cầu phụ thuộc vào liều lượng và nồng độ.
Sự ức chế kết tập tiểu cầu do TRAP gây ra ở mức ≥80% có thể kéo dài trong 2 đến 4 tuần sau khi ngừng dùng vorapaxar sulfat 2,5 mg hàng ngày. Thời gian của các tác dụng dược lực học này phù hợp với thời gian bán thải của thuốc.
Phù hợp với mục tiêu phân tử chọn lọc (PAR-1), vorapaxar không có tác dụng đối với sự kết tập tiểu cầu do ADP gây ra ở những đối tượng khỏe mạnh và quần thể bệnh nhân.
Trong các nghiên cứu về tình nguyện viên khỏe mạnh, không có sự thay đổi nào về biểu hiện P-selectin trong tiểu cầu và phối tử CD40 hòa tan (sCD40L) hoặc các thông số xét nghiệm đông máu (TT, PT, aPTT, ACT, ECT) sau khi dùng một hoặc nhiều lần.
Liều lượng (28 ngày) sử dụng vorapaxar. Không quan sát thấy những thay đổi có ý nghĩa về nồng độ Pselectin, sCD40L và hs-CRP ở những bệnh nhân được điều trị bằng vorapaxar trong các thử nghiệm lâm sàng Giai đoạn 2/3.
Đánh giá Zontivity trên khoảng QTc Tác dụng của vorapaxar trên khoảng QTc đã được đánh giá trong một nghiên cứu QT kỹ lưỡng và trong các nghiên cứu khác. Vorapaxar không ảnh hưởng đến khoảng QTc ở liều đơn lên đến 120 mg.
Ứng dụng trong y học của Vorapaxar
Vorapaxar được sử dụng cho những người có tiền sử nhồi máu cơ tim (đau tim) hoặc những người mắc bệnh động mạch ngoại vi . Các nghiên cứu đã chỉ ra rằng thuốc này có thể làm giảm tỷ lệ tử vong do tim mạch, MI, đột quỵ và tái thông mạch vành khẩn cấp.
Dược động học
Hấp thu
khi uống một liều vorapaxar sulfat 2,5 mg duy nhất, vorapaxar được hấp thu nhanh chóng và nồng độ đỉnh đạt được với tmax trung bình là 1 giờ trong khi đói. Sinh khả dụng tuyệt đối trung bình của vorapaxar từ liều 2.5mg vorapaxar sulfat ~100%.
Uống vorapaxar cùng với bữa ăn nhiều chất béo dẫn đến thay đổi AUC không có ý nghĩa với Cmax giảm nhẹ (21%) và tmax bị trì hoãn (45 phút). Zontivity có thể được thực hiện có hoặc không có thức ăn.
Sử dụng đồng thời thuốc kháng axit nhôm hydroxit/magie cacbonat hoặc chất ức chế bơm proton (pantoprazole) không ảnh hưởng đến AUC của vorapaxar chỉ với sự giảm nhẹ Cmax . Do đó, Zontivity có thể được sử dụng mà không cần quan tâm đến việc sử dụng đồng thời các tác nhân làm tăng pH dạ dày (thuốc kháng axit hoặc thuốc ức chế bơm proton).
Phân bố
Thể tích phân bố trung bình của vorapaxar là khoảng 424 lít. Vorapaxar và chất chuyển hóa có hoạt tính lưu hành chính,
M20, gắn kết rộng rãi (≥99%) với protein huyết tương của người. Vorapaxar liên kết cao với albumin huyết thanh người và không ưu tiên phân phối vào các tế bào hồng cầu.
Chuyển hóa
Vorapaxar được loại bỏ bằng quá trình chuyển hóa, với CYP3A4 và CYP2J2 chịu trách nhiệm hình thành M20, chất chuyển hóa tuần hoàn có hoạt tính chính của nó và M19, chất chuyển hóa chiếm ưu thế được xác định trong bài tiết. Mức độ phơi nhiễm toàn thân của M20 là ~20% mức độ phơi nhiễm với vorapaxar
Đào thải
Con đường thải trừ chính là qua phân, với khoảng 91,5% liều đánh dấu phóng xạ được dự đoán sẽ được tìm thấy trong phân so với 8,5% trong nước tiểu. Vorapaxar được thải trừ chủ yếu dưới dạng chất chuyển hóa, không phát hiện thấy vorapaxar trong nước tiểu. Thời gian bán hủy biểu kiến cuối cùng của vorapaxar là 187 giờ (trong khoảng 115-317 giờ) và tương tự đối với chất chuyển hóa có hoạt tính.
Độc tính của Vorapaxar
Tăng nguy cơ chảy máu và xuất huyết nội sọ (ICH), đó là lý do tại sao việc sử dụng vorapaxar bị chống chỉ định ở những bệnh nhân có tiền sử đột quỵ, cơn thiếu máu cục bộ (TIA), ICH hoặc chảy máu bệnh lý đang hoạt động như loét dạ dày tá tràng. Các nghiên cứu trên động vật đã gợi ý rằng có khả năng gây độc cho phôi thai/thai nhi thấp, tuy nhiên không có nghiên cứu đầy đủ và được kiểm soát tốt mô tả việc sử dụng thuốc ở phụ nữ mang thai. Vorapaxar cũng nên tránh trong thời kỳ cho con bú vì không biết liệu vorapaxar hoặc các chất chuyển hóa của nó có được bài tiết vào sữa mẹ hay không, tuy nhiên nó đã được chứng minh là được tiết ra chủ động trong sữa của chuột.
Tương tác của Vorapaxar với thuốc khác
Vorapaxar được loại bỏ chủ yếu bằng cách chuyển hóa bởi các enzym CYP3A. Tốt nhất là tránh bất kỳ chất ức chế mạnh CYP3A4 nào (ví dụ: ketoconazole, itraconazole, posaconazole, clarithromycin, nefazodone, ritonavir, saquinavir, nelfinavir, indinavir, boceprevir, telaprevir, telithromycin và conivaptan). Cũng nên tránh các chất gây cảm ứng CYP3A4 (Carbamazepine, rifampin, St. John’s Wort và Phenytoin).
Lưu ý khi dùng Vorapaxar
Lưu ý và thận trọng chung
Trước khi dùng thuốc Vorapacartar, bệnh nhân nên thông báo cho bác sĩ nếu họ có bất kỳ dị ứng với Vorapaxar hoặc bất kỳ thành phần nào khác của thuốc. Đặc biệt nếu bệnh nhân có tiền sử đột quỵ, chảy máu não, loét dạ dày, rối loạn đông máu, phẫu thuật gần đây, chấn thương nghiêm trọng, bệnh gan và các điều kiện liên quan khác. Các biện pháp phòng ngừa khác cần xem xét khi dùng thuốc này bao gồm tăng thời gian chảy máu nếu bệnh nhân bị cắt hoặc chấn thương, cần thận trọng khi sử dụng các vật sắc nhọn như dao cạo râu và bấm móng tay, và tránh các môn thể thao tiếp xúc hoặc các hoạt động thể chất khác có thể làm tăng nguy cơ chảy máu.
Bệnh nhân cũng có thể vẫn có nguy cơ chảy máu đến bốn tuần sau khi ngừng thuốc. Ngoài ra, nên hạn chế rượu và đồ uống có cồn khác trong quá trình điều trị, vì điều này có thể làm tăng nguy cơ chảy máu dạ dày.
Trước khi trải qua bất kỳ cuộc phẫu thuật nào, bệnh nhân nên thông báo cho bác sĩ về việc sử dụng thuốc Vorapaxar.
Lưu ý cho người đang mang thai
Không có dữ liệu đáng tin cậy về việc sử dụng vorapaxar ở phụ nữ mang thai. Không có tác dụng liên quan nào được quan sát thấy ở động vật. Zontivity chỉ nên được sử dụng trong thai kỳ nếu lợi ích tiềm năng cho người mẹ biện minh cho nguy cơ tiềm ẩn đối với thai nhi.
Lưu ý cho người đang cho con bú
Không biết liệu vorapaxar có được bài tiết qua sữa mẹ hay không. Các nghiên cứu trên chuột cho thấy vorapaxar và/hoặc các chất chuyển hóa của nó được bài tiết qua sữa. Do khả năng xảy ra các phản ứng bất lợi ở trẻ bú mẹ từ Zontivity chưa được biết rõ, hãy ngừng cho con bú hoặc ngừng Zontivity; có tính đến tầm quan trọng của sản phẩm thuốc đối với người mẹ.
Lưu ý cho người vận hành máy móc hay lái xe
Không có báo cáo về Vorapaxar trên nhóm đối tượng này
Một vài nghiên cứu về Vorapaxar trong Y học
Điều trị bằng Vorapaxar làm giảm sự mở rộng trung mô ở bệnh thận đái tháo đường do streptozotocin gây ra ở chuột

Đặt vấn đề: Hai mươi năm sau khi bệnh đái tháo đường khởi phát, có tới 40% bệnh nhân mắc bệnh thận đái tháo đường. Thụ thể được kích hoạt bằng protease-1 (PAR-1) gần đây đã được chứng minh là làm trầm trọng thêm sự phát triển của bệnh thận đái tháo đường thực nghiệm. Những con chuột bị thiếu PAR-1 phát triển ít albumin niệu và tổn thương cầu thận hơn và kích thích PAR-1 gây ra sự tăng sinh và sản xuất fibronectin trong các tế bào trung mô trong ống nghiệm . Vorapaxar là một chất ức chế PAR-1 có sẵn trên lâm sàng hiện đang được sử dụng để phòng ngừa thứ phát các biến cố thiếu máu cục bộ.
Mục tiêu: Mục đích của nghiên cứu này là điều tra trong môi trường tiền lâm sàng liệu điều trị bằng vorapaxar có thể là một chiến lược mới để giảm tổn thương thận do bệnh tiểu đường gây ra hay không.
Kết quả: Trong khi những con chuột mắc bệnh tiểu đường được điều trị phát triển albumin niệu đáng kể, mở rộng trung mô và lắng đọng fibronectin ở cầu thận, những con chuột mắc bệnh tiểu đường được điều trị bằng vorapaxar không có bất kỳ dấu hiệu tổn thương thận nào mặc dù có mức tăng đường huyết tương tự.
Kết luận: Những dữ liệu này cho thấy rằng sự ức chế PAR-1 bởi vorapaxar ngăn ngừa sự phát triển của bệnh thận đái tháo đường trong mô hình động vật tiền lâm sàng đối với bệnh đái tháo đường týp I này và xác định PAR-1 là mục tiêu điều trị mới để theo đuổi trong bối cảnh bệnh thận đái tháo đường.
Vật liệu và phương pháp: 22 con chuột C57Bl/6 được tạo ra bệnh tiểu đường bằng cách sử dụng nhiều mũi tiêm streptozotocin liều thấp (50 mg/kg) và 22 con cùng lứa được dùng làm đối chứng không mắc bệnh tiểu đường. Bốn tuần sau khi gây ra bệnh tiểu đường, 11 con chuột của mỗi nhóm được chỉ định kiểm soát hoặc điều trị bằng vorapaxar. Chuột đã chết sau 20 tuần điều trị và tổn thương thận đã được đánh giá.
Tài liệu tham khảo
- Drugbank, Vorapaxar , truy cập ngày 04/04/2023.
- Pubchem, Vorapaxar, truy cập ngày 04/04/2023.
- Waasdorp, M., Duitman, J., Florquin, S., & Spek, C. A. (2018). Vorapaxar treatment reduces mesangial expansion in streptozotocin-induced diabetic nephropathy in mice. Oncotarget, 9(31), 21655.
- https://www.wikidoc.org/index.php/File:Vorapaxar_label.jpg
