Thalidomid
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
2-(2,6-dioxopiperidin-3-yl)isoindole-1,3-dione
Nhóm thuốc
Thalidomide là thuốc gì? Thuốc ức chế miễn dịch
Mã ATC
L – Chất chống ung thư và điều hòa miễn dịch
L04 – Thuốc ức chế miễn dịch
L04A – Thuốc ức chế miễn dịch
L04AX – Thuốc ức chế miễn dịch khác
L04AX02 – Thalidomide
Mã UNII
4Z8R6ORS6L
Mã CAS
50-35-1
Cấu trúc phân tử
Công thức phân tử
C13H10N2O4
Phân tử lượng
258.23 g/mol
Đặc điểm cấu tạo
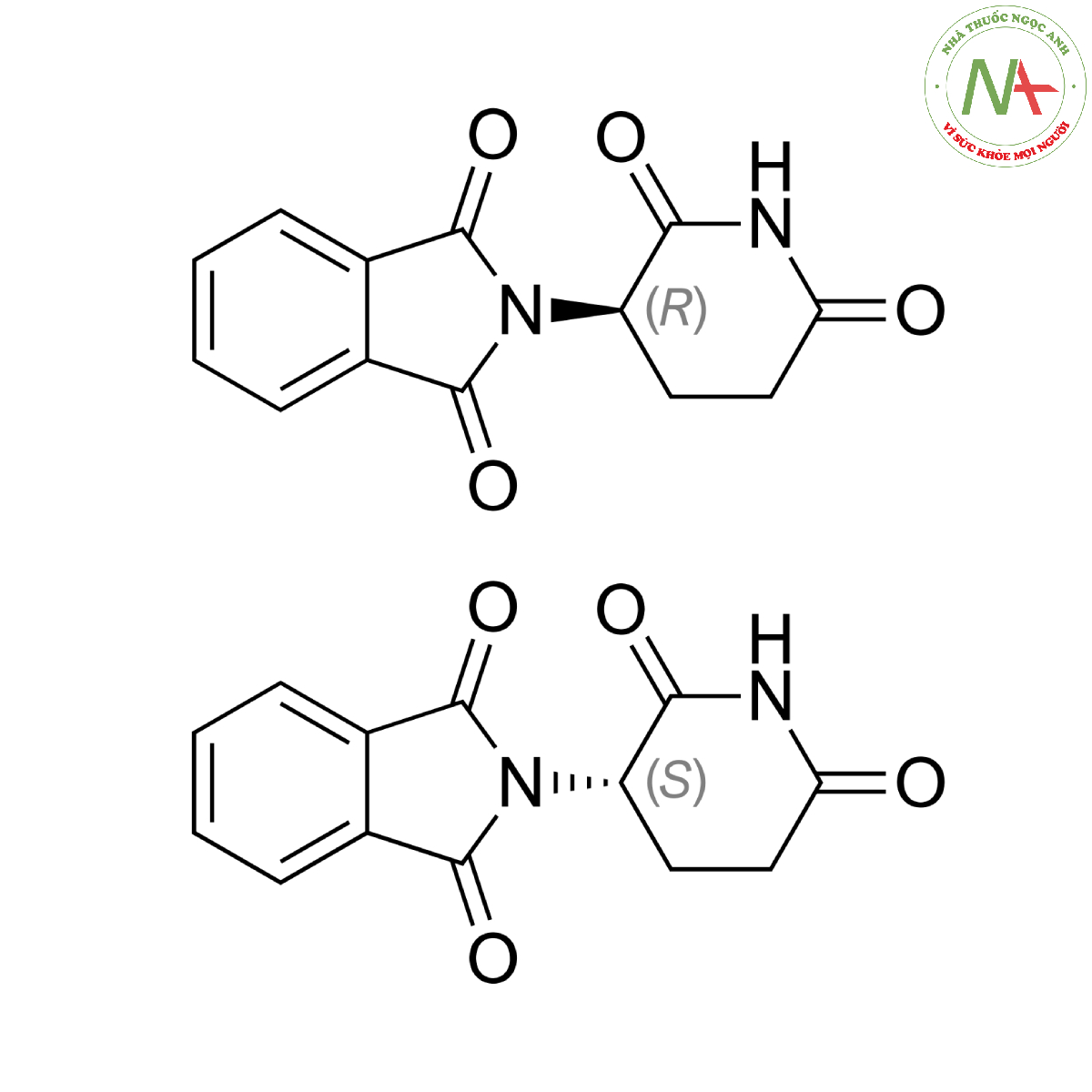
Thalidomide là isoindole-1,3(2H)-dione trong đó hydro gắn với nitơ là được thay thế bằng nhóm 2,6-dioxopiperidin-3-yl.
Mô hình bóng và que
Các tính chất phân tử
Số liên kết hydro cho: 1
Số liên kết hydro nhận: 4
Số liên kết có thể xoay: 1
Diện tích bề mặt cực tôpô: 83,6
Số lượng nguyên tử nặng: 19
Số lượng nguyên tử trung tâm xác định được: 1
Liên kết cộng hóa trị: 1
Tính chất
- Thalidomide có dạng kim hoặc bột màu trắng.
- Điểm nóng chảy 516 đến 520°F
- Độ hòa tan dưới 1 mg/mL ở 72°F.
- Ít tan trong butyl axetat, etanol, metanol,axeton, etyl axetat, axit axetic băng. Rất hòa tan trong DMF .
- Thực tế không tan trong ete, cloroform, benzen
- Rất hòa tan trong dioxan, pyridin
Dạng bào chế
Viên nang cứng: thuốc Thalidomide Capsules USP 100 mg,.
Nguồn gốc
- Năm 1952, thalidomide được tổng hợp bởi Công ty Hóa chất Basel nhưng tại thời điểm này chưa phát hiện được tác dụng của Thalidomide trên động vật.
- Năm 1956, Thalidomide đã được kiểm tra về độc tính trên một số động vật nhưng chưa bao giờ được thử nghiệm trên phụ nữ mang thai
- Ngày 1/10/1957, Thalidomide được tung ra trên thị trường và được coi là thuốc rất tốt trong điều trị chứng mất ngủ, đau đầu, ho, cảm lạnh.
- Vào cuối năm 1959, người ta đã phát hiện ra ở những bệnh nhân dùng Thalidomide trong 1 thời gian bị viêm dây thần kinh ngoại biên vì vậy Thalidomide ngừng cung cấp.
- Tháng 9/1960, FDA Hoa Kỳ từ chối phê duyệt thalidomide để phân phối và tiếp thị.
- Tháng 11/1960, Thực phẩm và Dược phẩm Canada đã phê duyệt việc bán thalidomide theo toa.
Dược lý và cơ chế hoạt động
- Thalidomide có các chất đối hình S(-) và R(+) hoán đổi cho nhau trong khi chất đối hình R(+) hoạt động như một thuốc an thần thông qua các thụ thể giấc ngủ thì đối hình S(-) ức chế trực tiếp sự giải phóng TNF-alpha. Sự thủy phân tự phát của thalidomide ở PH sinh lý dẫn đến việc tạo ra khoảng 20 hợp chất khác nhau. Các enzyme chuyển hóa tác động lên Thalidomide tạo ra các chất chuyển hóa có hoạt tính dẫn đến tăng sinh tế bào nội mô, ức chế sự hình thành mạch.
- Một thành phần của phức hợp ligase E3 ubiquitin của Thalidomide làm suy giảm có chọn lọc yếu tố phiên mã IKZF3 và IKZF1. Hai yếu tố này rất quan trọng cho sự tăng sinh và tồn tại của các tế bào u nguyên bào ác tính. Thalidomide chặn chất trung gian này thông qua nhiều cơ chế khác nhau. Thalidomide có thể ức chế một protein tiếp hợp có liên quan đến con đường truyền tín hiệu sản xuất TNF-alpha là MyD88 ở cấp độ protein và RNA. Ngoài ra, thalidomide ngăn chặn glycoprotein axit alpha-1 (AGP), ngăn chặn sự kích hoạt của Yếu tố hạt nhân Kappa B. Việc điều chỉnh giảm NF-kB và MyD88 cũng dẫn đến tác dụng chống tạo mạch của thalidomide.
Dược động học
Hấp thu
Thalidomide thuốc có sinh khả dụng chưa được xác định dẫn đến tác dụng chống tạo mạch của thalidomide. Thalidomide khi dùng liều 50-400mg đạt nồng độ tối đa trong huyết tương sau 2,9-5,7 giờ.
Chuyển hóa
Thalidomide được chuyển hóa không cần enzyme thông qua quá trình thủy phân thành nhiều chất chuyển hóa, vì bốn liên kết amide trong thalidomide cho phép thủy phân nhanh chóng dưới pH sinh lý.
Phân bố
Thalidomide có thể tích phân bố khoảng 70-120 L và có khả năng liên kết với protein huyết tương 55% – 66%.
Thải trừ
Thalidomide sau khi uống có độ thanh thải là 10,50 ± 2,10 L/giờ và thời gian bán thải 6,17 ± 2,56 giờ khi dùng liều 200mg. Thalidomide được bài tiết chủ yếu dưới dạng dạng chất chuyển hóa thủy phân qua nước tiểu.
Ứng dụng trong y học
Thalidomide có tác dụng gì? Thalidomide được chỉ định trong:
- Thalidomide được sử dụng trong điều trị cấp tính và điều trị duy trì để ngăn ngừa và ngăn chặn các biểu hiện ở da từ trung bình đến nặng của bệnh phong nút ban đỏ.
- Bệnh ghép chống lại vật chủ
- Nhiễm vi khuẩn Mycobacterium
- Viêm miệng tái phát nặng
- Các khối u ác tính nguyên phát ở não
- Hội chứng suy nhược liên quan đến HIV
- Bệnh Crohn
- Kaposi sarcoma
- Hội chứng loạn sản tủy
- Ghép tế bào gốc tạo máu
- Giãn mao mạch xuất huyết.
Tác dụng phụ
Phản ứng có hại liên quan đến Thalidomide: nhức đầu, bệnh thần kinh ngoại biên, táo bón,buồn ngủ, an thần, phát ban, suy giáp, xerostomia, sốt, thay đổi tâm trạng, kích thích ACTH, hạ đường huyết và huyết khối tĩnh mạch sâu.
Chống chỉ định
- Phụ nữ có thai và cho con bú vì Thalidomide gây quái thai và gây độc tính phôi thai, gây dị tật bẩm sinh nghiêm trọng hoặc tử vong.
- Tiền sử hoặc có nguy cơ đáng kể về biến cố huyết khối tĩnh mạch.
- Những bệnh nhân trước đây có biểu hiện tác dụng phụ nghiêm trọng như phản ứng quá mẫn loại 1, hội chứng Stevens-Johnson với Thalidomide.
- Chống chỉ định dùng Thalidomide cho phụ nữ cho con bú.
Độc tính ở người
Các triệu chứng phổ biến nhất liên quan đến ngộ độc thalidomide bao gồm mệt mỏi và bệnh lý thần kinh, táo bón, an thần.
Liều dùng
Đường uống: 50-200 mg mỗi ngày một lần.
Tương tác với thuốc khác
- Độc tính của thalidomid tăng lên khi dùng kết hợp với dexamethasone hoặc các loại thuốc hóa trị khác.
- Sử dụng thalidomide cùng với aripiprazole, duloxetine, ethanol, tramadol, carbamazepine, paroxetine, morphine prochlorperazine, có thể làm tăng tác dụng phụ như khó tập trung buồn ngủ, lú lẫn, chóng mặt.
- Sử dụng thalidomide và pamidronate, axit zoledronic cùng với nhau có thể làm tăng nguy cơ vấn đề về thận.
- Sử dụng thalidomide cùng với rosuvastatin/ bortezomib có thể làm tăng nguy cơ tổn thương thần kinh
- Việc dùng đồng thời Thalidomide và levofloxacin/metoprolol/ ondansetron có thể gây tăng tổn thương thần kinh và nhịp tim bất thường
Lưu ý khi sử dụng
- Trước khi bắt đầu điều trị bằng Thalidomide phải loại trừ khả năng mang thai ở bệnh nhân và trong quá trình điều trị Thalidomide cần có biện pháp tránh thai hợp lí.
- Trong quá trình dùng Thalidomide bệnh nhân nên thăm khám sức khỏe định kỳ với bác sĩ, kiểm tra bệnh nhân phát triển bệnh lý thần kinh thông qua các cuộc kiểm tra nghiên cứu EMG, thần kinh hoàn chỉnh sáu tháng một lần.
- Bệnh nhân được điều trị đồng thời bằng dexamethasone, thalidomide nên được theo dõi các dấu hiệu và triệu chứng của huyết khối tắc mạch.
- Bệnh nhân được điều trị bằng liệu pháp thalidomide cũng có thể dùng thuốc chống đông máu dự phòng hoặc điều trị bằng aspirin.
Một vài nghiên cứu của Thalidomide trong Y học
So sánh hiệu quả và độ an toàn của thalidomide và lenalidomide ở bệnh nhân đa u tủy ở Hoa Kỳ: Một nghiên cứu đoàn hệ dựa trên dân số

Nghiên cứu tiến hành đánh giá tỷ lệ sống sót và tỷ lệ mắc bệnh thần kinh ngoại biên so sánh của bệnh nhân u tủy được điều trị bằng thalidomide hoặc lenalidomide trong chăm sóc định kỳ ở Hoa Kỳ. Bệnh nhân u tủy được xác định và theo dõi đủ điều kiện bắt đầu điều trị bằng lenalidomide hoặc thalidomide trong khoảng thời gian từ năm 2004 đến năm 2013. Có tổng cộng m 1264 bệnh nhân u tủy đã bắt đầu sử dụng thalidomide hoặc lenalidomide. Trong số 858 người mới sử dụng lenalidomide, 244 người phát triển bệnh thần kinh trong 587 ngày.. Trong số 406 người mới sử dụng thalidomide, 142 người phát triển bệnh lý thần kinh ngoại biên trong thời gian theo dõi trung bình là 499 ngày. So với thuốc khởi đầu thalidomide, thuốc khởi đầu lenalidomide có ít nguy cơ mắc bệnh thần kinh ngoại biên hơn. Nghiên cứu kết luận thalidomide và lenalidomide tương đương nhau về kết quả sống sót nhưng khác nhau về độc tính thần kinh trong môi trường thực hành lâm sàng.
Tài liệu tham khảo
- Thư viện y học quốc gia, Thalidomide, pubchem. Truy cập ngày 07/11/2023.
- Dayton P. Grogan; Nicole R. Winston. Thalidomide, pubmed.com. Truy cập ngày 07/11/2023.
- Jing Luo 1, Joshua J Gagne 2, Joan Landon 2, Jerry Avorn 2, Aaron S Kesselheim (2016) Comparative effectiveness and safety of thalidomide and lenalidomide in patients with multiple myeloma in the United States of America: A population-based cohort study, pubmed.com. Truy cập ngày 07/11/2023.
Xuất xứ: Ấn Độ
Xuất xứ: Việt Nam