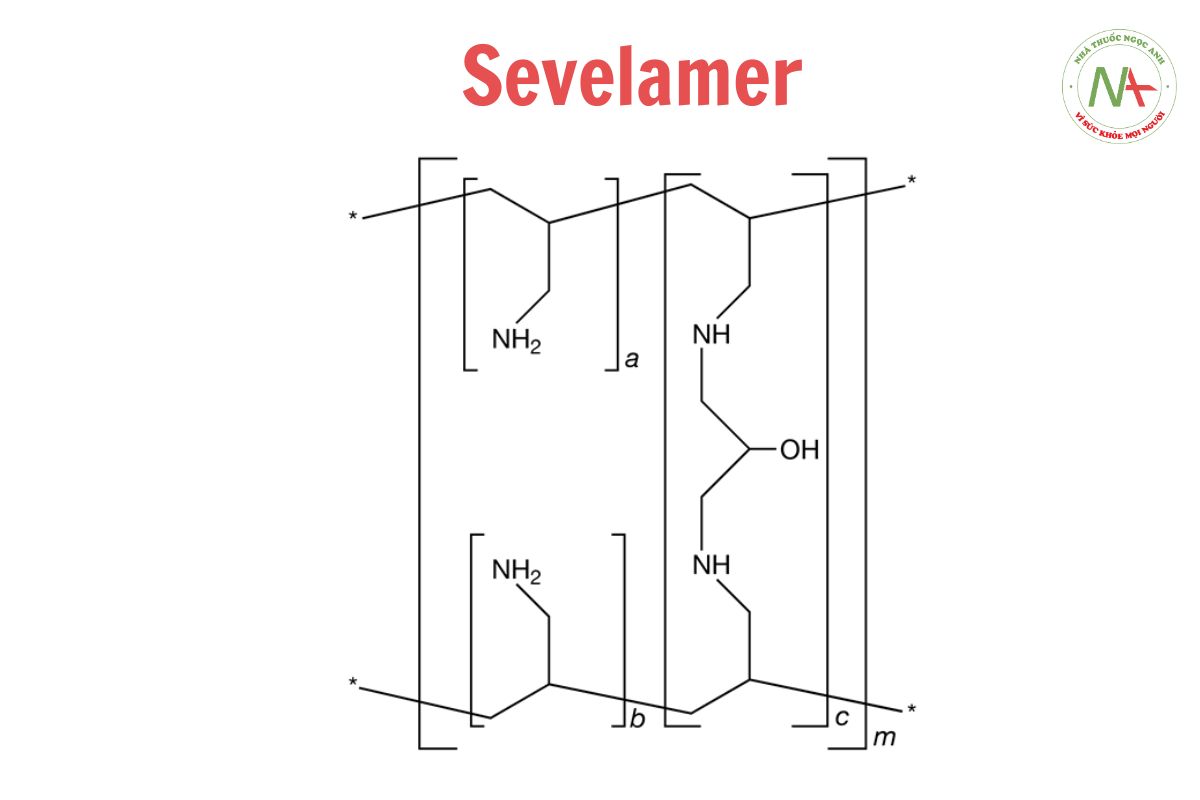
Sevelamer
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
Poly(allylamine-co-N,N’-diallyl-1,3-diamino-2-hydroxypropane)
Mã ATC
V – Khác nhau
V03 – Tất cả sản phẩm điều trị khác
V03A – Tất cả sản phẩm điều trị khác
V03AE – Thuốc điều trị tăng kali máu và tăng photphat máu
V03AE02 – Sevelamer
Mã UNII
941N5DUU5C
Mã CAS
52757-95-6
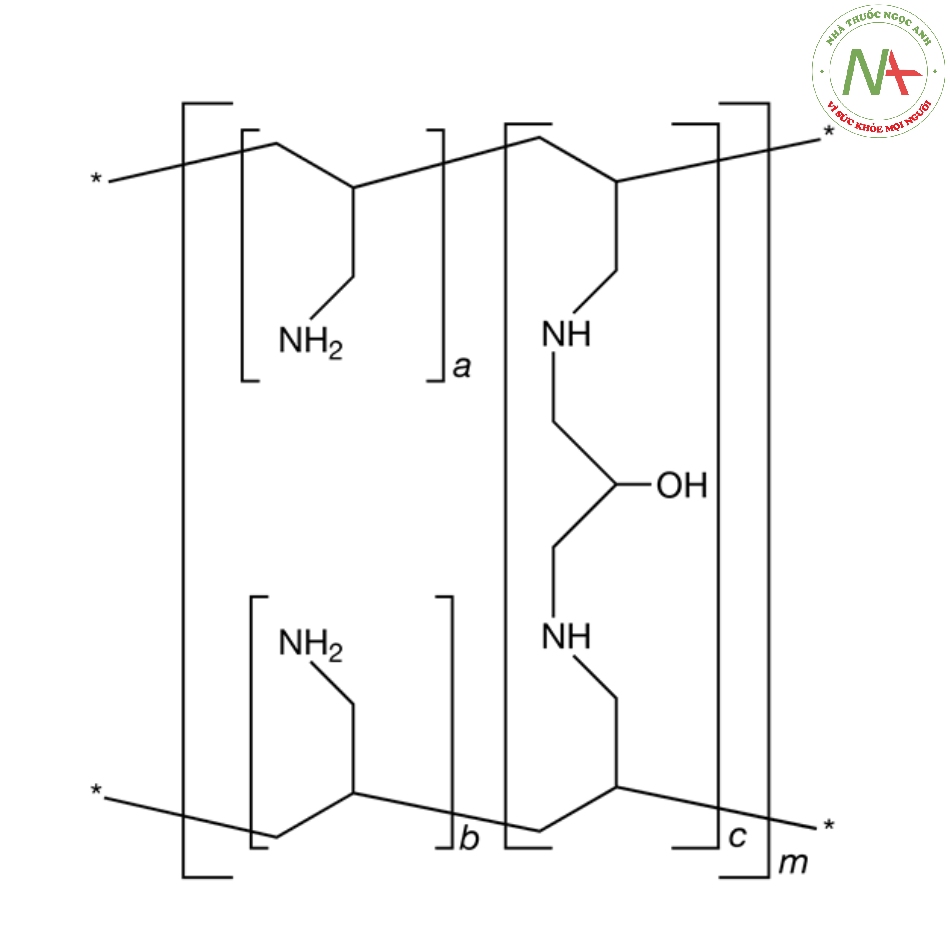
Cấu trúc phân tử
Công thức phân tử
[(C3H7N)a+b.(C9H17N2O)c]m
Phân tử lượng
Biến số
Cấu trúc phân tử
Tính chất
Sevelamer không hòa tan trong nước.
Dạng bào chế
Viên nén: Sevelamer 400mg, Sevelamer 800mg,…
Bột pha uống: Sevelamer carbonate Tablets 800 mg,..
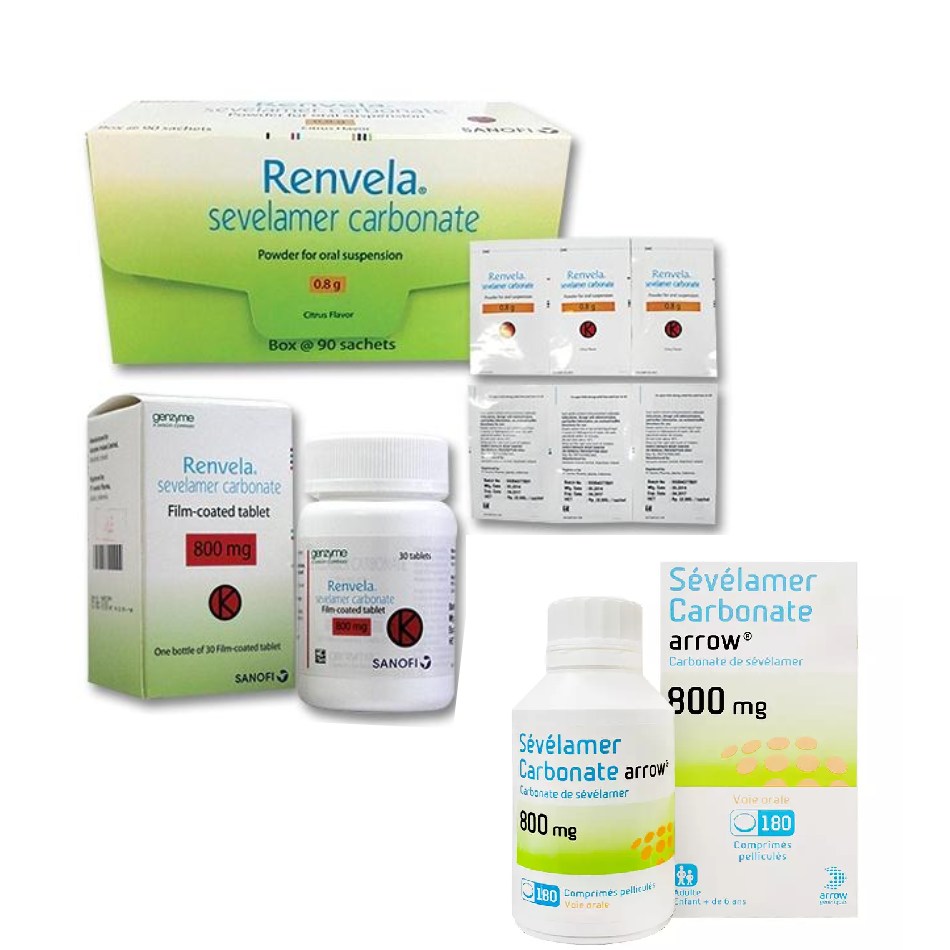
Độ ổn định và điều kiện bảo quản
Bảo quản ở 25 °C (77 °F), trong quá trình vận chuyển thuốc được phép đến 15-30 °C (59-86 °F).
Dược lý và cơ chế hoạt động
Sevelamer thuốc có cơ chế như sau:
Sevelamer là một chất liên kết amine và phosphate cao phân tử không thể hấp thụ, có thể được sử dụng để ngăn ngừa chứng tăng phosphate huyết. Sevelamer liên kết phốt phát trong đường tiêu hóa và làm giảm hấp thu phốt phát trong huyết thanh. Khi dùng trong bữa ăn, sevelamer làm giảm cả hormone tuyến cận giáp và phốt phát huyết thanh, nhưng không làm tăng canxi huyết thanh.Sau khi uống, các nhóm amin trong sevelamer bị proton hóa trong ruột và liên kết với các nhóm phốt phát trong chế độ ăn uống trong đường tiêu hóa (GI), do đó ngăn chặn sự hấp thụ phốt phát và kiểm soát nồng độ phốt phát trong huyết tương. Ngoài ra, sevelamer , như một chất kết dính phốt phát , có thể được sử dụng để ngăn chặn sự hấp thụ của hạt nhân phóng xạ phốt pho P 32 (P-32).
Dược động học
Một nghiên cứu cân bằng khối lượng sử dụng (14)C- sevelamer hydrochloride ở 16 tình nguyện viên nam và nữ khỏe mạnh cho thấy rằng sevelamer hydrochloride không được hấp thụ một cách có hệ thống. Không có nghiên cứu hấp thu đã được thực hiện ở những bệnh nhân bị bệnh thận.
Ứng dụng trong y học
- Sevelamer được chỉ định để kiểm soát chứng tăng phosphat máu ở bệnh nhân là người lớn đang chạy thận nhân tạo hoặc thẩm phân phúc mạc.
- Sevelamernên được sử dụng trong phương pháp điều trị đa dạng, có thể bao gồm chế độ bổ sung Vitamin D3, 1,25 – dihydroxy, canxi, hoặc một trong những chất tương tự Sevelamer để kiểm soát sự phát triển của bệnh xương thận.
- Sevelamer là một polyme liên kết ngang trao đổi photphat với HCl hoặc cacbonat trong đường tiêu hóa. Polyme chứa nhiều phốt phát được bài tiết qua phân. Cả sevelamer hydrochloride (HCl) và sevelamer cacbonat đều là những lựa chọn. Bên cạnh việc kiểm soát chứng tăng phosphate huyết, sevelamer còn cải thiện chức năng nội mô, liên kết với muối mật, dẫn đến giảm đáng kể cholesterol toàn phần trong huyết thanh và cholesterol lipoprotein tỷ trọng thấp. Tuy nhiên, hành động này có thể cản trở sự hấp thụ chất béo và vitamin tan trong chất béo.
Tác dụng phụ
Tác dụng phụ xảy ra ở 2% bệnh nhân trở lên bao gồm tiêu chảy, táo bón, khó tiêu, đầy hơi, buồn nôn, nôn, tăng huyết áp, hạ huyết áp, huyết khối, nhiễm trùng (viêm mũi họng, viêm phế quản, nhiễm trùng đường hô hấp trên), ho, khó thở, đau (ví dụ, đau nhức chân tay) , đau lưng), nhức đầu, đau khớp, sốt và ngứa.
Độc tính
Độc tính ở người
- Sevelamer đã được dùng cho những người tình nguyện khỏe mạnh bình thường với liều lên tới 14 gam mỗi ngày trong 8 ngày mà không có tác dụng phụ. Sevelamer đã được dùng với liều trung bình lên tới 13 gam mỗi ngày cho bệnh nhân chạy thận nhân tạo. Không có báo cáo về quá liều sevelamer ở bệnh nhân. Vì sevelamer không được hấp thụ nên nguy cơ nhiễm độc toàn thân thấp.
- Vì sevelamer không được hấp thu qua đường miệng nên sevelamer không đến được sữa mẹ hoặc ảnh hưởng xấu đến trẻ sơ sinh bú sữa mẹ sau khi mẹ dùng. Hỗn dịch sevelamer đã được thêm trực tiếp vào sữa mẹ để giảm nồng độ phốt pho trong sữa. Đây có thể là một thủ thuật hữu ích cho việc sử dụng sữa mẹ ở trẻ sơ sinh bị suy thận; tuy nhiên, sử dụng lâm sàng đã không được báo cáo. Ngoài việc giảm hàm lượng phốt pho trung bình từ 65% đến hơn 80%, hàm lượng canxi trong sữa mẹ cũng giảm gần như tương đương và hàm lượng casein cũng giảm đi phần nào. Với sevelamer hydrochloride , clorua tăng 60% và độ pH thay đổi từ 6,8 đến 7,8, mặc dù độ pH dường như tăng trở lại theo thời gian. Việc bổ sung một lượng lớn sevelamer vào công thức nhân tạo cũng làm giảm nồng độ đồng , magie , mangan , kali , lưu huỳnh và kẽm khoảng 20%. Giảm tương tự có thể xảy ra với sữa mẹ.
- Một so sánh ngẫu nhiên giữa sevelamer và chất kết dính phốt phát dựa trên canxi đã được thực hiện ở những bệnh nhân chạy thận nhân tạo được điều trị đến 45 tháng. Điểm cuối chính là tỷ lệ tử vong. Tiêu chí phụ bao gồm tử vong và nhập viện do nguyên nhân cụ thể; 2103 bệnh nhân được chọn ngẫu nhiên, 2040 được điều trị và 1065 hoàn thành điều trị. Tỷ lệ tử vong chung không giảm đáng kể bởi sevelamer (rủi ro tương đối được điều chỉnh = 0,92; khoảng tin cậy 95%, 0,78 đến 1,09; log-rank P = 0,40). Trong số những bệnh nhân > hoặc = 65 tuổi, sevelamer làm giảm nguy cơ tử vong (nguy cơ tương đối được điều chỉnh = 0,77; khoảng tin cậy 95%, 0,62 đến 0,97; log-rank P = 0,02). Sevelamerbệnh nhân có xu hướng nhập viện ít hơn (P = 0,06) và ít ngày nằm viện hơn (P = 0,09). Không thấy giảm đáng kể về mặt thống kê tỷ lệ tử vong trong toàn bộ dân số nghiên cứu. Sevelamer có liên quan đến lợi ích sống còn ở những bệnh nhân > hoặc = 65 tuổi.
Độc tính ở động vật
- Phơi nhiễm mãn tính hoặc khả năng gây ung thư. Các thử nghiệm sinh học về khả năng gây ung thư trong thời gian sống tiêu chuẩn được tiến hành ở chuột nhắt và chuột cống. Chuột được cung cấp sevelamer hydrochloride theo chế độ ăn uống ở mức 0,3 hoặc 3 g/kg/ngày. Có sự gia tăng tỷ lệ tế bào u nhú chuyển tiếp bàng quang tiết niệu ở chuột đực (3 g/kg/ngày) khi tiếp xúc gấp 2 lần liều uống tối đa ở người là 13 g, dựa trên so sánh diện tích bề mặt cơ thể tương đối. Chuột nhận được liều ăn kiêng trung bình là 0,8 hoặc 9 g/kg/ngày. Tỷ lệ mắc khối u gia tăng không được quan sát thấy ở chuột khi tiếp xúc gấp 3 lần liều uống tối đa ở người là 13g, dựa trên so sánh diện tích bề mặt cơ thể tương đối.
- Ở thỏ mang thai được cho uống các liều 100, 500, 1000 mg/kg/ngày bằng ống hút trong quá trình hình thành cơ quan, tỷ lệ tái hấp thu sớm tăng lên khi phơi nhiễm gấp 2 lần liều tối đa ở người là 13 g, dựa trên trên một so sánh của diện tích bề mặt cơ thể tương đối. Nhu cầu về vitamin và các chất dinh dưỡng khác tăng lên trong thời kỳ mang thai.
- Trong một nghiên cứu được thiết kế để đánh giá khả năng suy giảm khả năng sinh sản, chuột cái được cung cấp liều ăn kiêng 0,5, 1,5, 4,5 g/kg/ngày bắt đầu từ 14 ngày trước khi giao phối và tiếp tục trong suốt thời kỳ mang thai. Những con chuột đực được cho dùng liều tương tự và điều trị trong 28 ngày trước khi giao phối. Sevelamer hydrochloride không làm suy giảm khả năng sinh sản ở chuột cống đực hoặc cái khi phơi nhiễm gấp 3 lần liều uống tối đa ở người là 13 g, dựa trên so sánh diện tích bề mặt cơ thể tương đối.
- Trong một thử nghiệm di truyền tế bào ở động vật có vú trong ống nghiệm với sự kích hoạt trao đổi chất, sevelamer hydrochloride gây ra sự gia tăng đáng kể về mặt thống kê số lượng sai lệch cấu trúc nhiễm sắc thể. Sevelamer hydrochloride không gây đột biến trong xét nghiệm đột biến vi khuẩn Ames.
Tính an toàn
- Rủi ro khi mang thai: Các nghiên cứu đầy đủ, được kiểm soát tốt trên người còn thiếu, khi tiến hành nghiên cứu việc dùng Sevelamer trên động vật cũng cho thấy nguy cơ đối với thai nhi. Vì vậy tránh dùng Sevelamer cho phụ nữ có thai.
- Phu nữ cho con bú: Bởi vì sevelamer không được hấp thụ vào máu, nên nó sẽ không đến được trẻ sơ sinh qua sữa mẹ. Nó được chấp nhận để sử dụng trong thời kỳ cho con bú.
- Sevelamer không khuyến cáo dùng cho trẻ < 6 tuổi.
Tương tác với thuốc khác
Dùng sevelamer có thể khiến cơ thể bệnh nhân khó hấp thụ một số loại thuốc hơn, khiến chúng kém hiệu quả hơn:
- Tương tác dược động học (giảm sinh khả dụng của ciprofloxacin khoảng 50%) khi sevelamer được sử dụng đồng thời với ciprofloxacin. Bệnh nhân chỉ nên dùng ciprofloxacin trước khi dùng Sevelamer ít nhất 2 giờ hay sau khi dùng Sevelamer ít nhất 6 giờ.
- Bệnh nhân chỉ nên dùngMycophenolate mofetil trước khi dùng Sevelamer ít nhất 2 giờ.
- Một bệnh nhân lọc máu 30 tuổi bị ảnh hưởng bởi cường cận giáp thứ phát bắt đầu điều trị bằng sevelamer, 4,8 g/ngày, với nồng độ phosphate huyết thanh cơ bản là 6,9 mg/dL. Bệnh nhân cũng được điều trị bằng omeprazole (20 mg/ngày) vì viêm dạ dày mãn tính. Nồng độ phốt phát bình thường hóa (4,2 mg/dL), nhưng sau bốn tháng theo dõi, phốt phát huyết thanh bất ngờ tăng lên 7,2 mg/dL. Trong cùng khoảng thời gian đó /bệnh nhân/ đã tự ý tăng liều omeprazole lên 80 mg/ngày do tình trạng khó tiêu trở nên trầm trọng hơn. Phép đo pH dạ dày cho thấy mức trung bình là 4,1, thay vì giá trị bình thường là 1 – 2, cho thấy quá trình kiềm hóa dược lý quá mức. Khi omeprazolđược giảm xuống đúng liều 20 mg/ngày. nồng độ phốt phát giảm nhanh chóng /xảy ra/. Báo cáo trường hợp này nhấn mạnh ảnh hưởng của pH dạ dày đến khả năng liên kết sevelamer phosphate. Liều cao omeprazole và hậu quả là pH dạ dày tăng quá mức có thể là nguyên nhân làm giảm khả năng liên kết phốt phát của sevelamer . Khi bệnh nhân dùng liều sevelamer thích hợp không đáp ứng với điều trị, nên xem xét khả năng tương tác với các thuốc làm tăng pH dạ dày.
Lưu ý khi sử dụng
- Tính an toàn và hiệu quả của Renagel ở những bệnh nhân mắc chứng khó nuốt, rối loạn nuốt, rối loạn nhu động dạ dày-ruột (GI) nghiêm trọng bao gồm táo bón nặng hoặc phẫu thuật đường tiêu hóa lớn chưa được thiết lập. Do đó, nên thận trọng khi sử dụng Renagel cho những bệnh nhân mắc các rối loạn đường tiêu hóa này.
- Không nên dùng sevelamer nếu bệnh nhân bị tắc ruột.
- Dùng sevelamer khi bệnh nhân đang mang thai có thể làm giảm nồng độ một số vitamin hoặc axit folic trong máu. Với phụ nữ mang thai nên được bổ sung vitamin và khoáng chất theo chỉ định của bác sĩ.
- Dùng sevelamer với bữa ăn.
- Trong khi sử dụng sevelamer, bệnh nhân có thể cần xét nghiệm máu thường xuyên.
- Sevelamer có thể chỉ là một phần của chương trình điều trị hoàn chỉnh bao gồm một chế độ ăn kiêng đặc biệt. Điều rất quan trọng là tuân theo kế hoạch ăn kiêng do bác sĩ hoặc chuyên gia tư vấn dinh dưỡng lập cho bệnh nhân. Bệnh nhân nên làm quen với danh sách các loại thực phẩm bệnh nhân phải ăn hoặc tránh để giúp kiểm soát tình trạng của bệnh nhân.
- Sau khi ghép thận, bệnh nhân không đủ chức năng ghép có thể cần chất kết dính phốt phát . Vẫn chưa biết liệu sevelamer có cản trở sự hấp thu các chất ức chế miễn dịch hay không. Tác dụng của nó đối với dược động học của cyclosporin A (CsA) và mycophenolate mofetil đã được nghiên cứu. Mười người lớn và tám trẻ em có chức năng ghép thận ổn định và nồng độ đáy CsA ổn định đã được kiểm tra. Một hồ sơ dược động học 12 giờ (10 điểm quan sát) đã được tiến hành mà không có sevelamer, sau một liều duy nhất và sau 4 ngày điều trị với nó. Sevelamer không có ảnh hưởng đáng kể đến động học CsA [diện tích dưới đường cong (AUC), nồng độ đỉnh, thời gian, AUC của AM1 đã giảm 30% và C(max) giảm 25% sau 4 ngày dùng sevelamer. Nồng độ MPA giảm đáng kể trung bình 25% AUC và 30% C(max) sau một liều duy nhất sevelamer. Một liều sevelamer duy nhất làm giảm C(max) và AUC của MPA. Uống nó trong vài ngày không ảnh hưởng đáng kể đến động học CsA.
- Renagel chống chỉ định ở những bệnh nhân bị giảm phosphat máu hoặc tắc ruột.
Một vài nghiên cứu của Sevelamer trong Y học
Hiệu quả và an toàn của sevelamer. So sánh với canxi cacbonat trong điều trị tăng phosphat máu ở bệnh nhân chạy thận nhân tạo
Mục tiêu: Các chất kết dính phốt phát hiện tại được sử dụng ở bệnh nhân chạy thận nhân tạo bao gồm các chất kết dính dựa trên canxi dẫn đến tăng canxi máu thường xuyên. Việc sử dụng polyme liên kết với phốt phát không chứa canxi và nhôm trong chạy thận nhân tạo (sevelamer) cho thấy hiệu quả trong các nghiên cứu ngắn hạn và dài hạn. Tuy nhiên, do sự khác biệt về chủng tộc, nghiên cứu đã thực hiện một nghiên cứu ngắn hạn trên bệnh nhân chạy thận nhân tạo ở Ả Rập Xê Út và so sánh sevelamer với chất kết dính phốt phát dựa trên canxi tiêu chuẩn.
Phương pháp: Một nghiên cứu chéo, ngẫu nhiên, nhãn mở đã được thực hiện để đánh giá tính an toàn và hiệu quả của sevelamer hydrochloride trong việc kiểm soát chứng tăng phosphat máu ở bệnh nhân chạy thận nhân tạo. Sau khoảng thời gian 2 tuần rửa sạch chất kết dính phốt phát, bệnh nhân chạy thận nhân tạo ổn định được dùng sevelamer hoặc canxi cacbonat, và liều lượng được điều chỉnh để đạt được sự kiểm soát phốt phát trong khoảng thời gian 8 tuần. Sau khoảng thời gian 2 tuần loại bỏ thuốc, bệnh nhân chuyển sang thuốc thay thế trong 8 tuần. Hai mươi bệnh nhân từ Đơn vị lọc máu của Bệnh viện King Fahd, Jeddah, Vương quốc Ả Rập Saudi, đã được tuyển dụng cho nghiên cứu từ tháng 3 năm 2003 đến tháng 6 năm 2003.
Kết quả: Có sự giảm tương tự về giá trị phốt phát huyết thanh trong suốt quá trình nghiên cứu với cả sevelamer (-3,3 +/- 2,2 mg/dL) và canxi cacbonat (-3,9 +/- 2,8 mg/dL). Năm mươi hai phần trăm bệnh nhân phát triển canxi huyết thanh lớn hơn 2,75 mmol/L (11,0 mg/dL) trong khi dùng canxi cacbonat so với 26% bệnh nhân dùng sevelamer (p<0,05). Tỷ lệ tăng canxi máu đối với sevelamer không khác với tỷ lệ tăng canxi máu trong giai đoạn rửa trôi. Bệnh nhân được điều trị bằng sevelamer cũng duy trì mức giảm cholesterol huyết thanh trung bình là 13%.
Kết luận: Sevelamer có hiệu quả trong việc kiểm soát chứng tăng phosphate máu mà không làm tăng tỷ lệ tăng canxi máu như khi dùng canxi cacbonat. Tác nhân này tỏ ra khá hiệu quả trong điều trị chứng tăng phosphat máu ở bệnh nhân chạy thận nhân tạo và việc sử dụng nó có thể có lợi trong điều trị bệnh nhân chạy thận nhân tạo.
Tài liệu tham khảo
- Thư viện y học quốc gia, Sevelamer , pubchem. Truy cập ngày 04/08/2023.
- Laila S Badawi , Muhammad Z Souqiyyeh (2004),Efficacy and safety of sevelamer. Comparison with calcium carbonate in the treatment of hyperphosphatemia in hemodialysis patients,pubmed.com. Truy cập ngày 04/08/2023.
Xuất xứ: Ấn Độ
Xuất xứ: Nepal