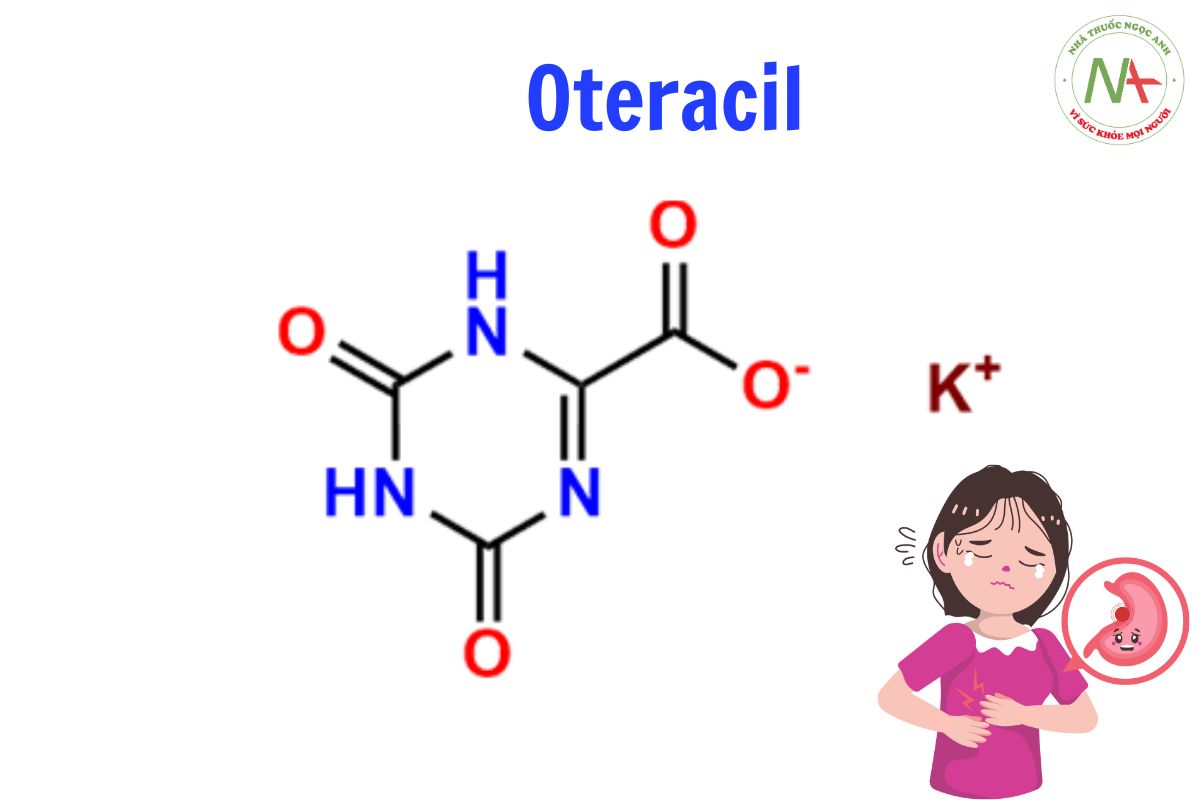
Oteracil
Danh pháp
Tên chung quốc tế
Oteracil _ Axit oxonic
Tên danh pháp theo IUPAC
Axit 4,6-dioxo-1 H -1,3,5-triazine-2-carboxylic
Nhóm thuốc
Thuốc điều trị ung thư
Mã ATC
Không có dữ liệu
Mã UNII
5VT6420TIG
Mã CAS
937-13-3
Xếp hạng phân loại cho phụ nữ có thai
AU TGA loại: NA
US FDA loại: NA
Cấu trúc phân tử
Công thức phân tử
C 4 H 3 N 3 O 4
Phân tử lượng
157,08 g/mol
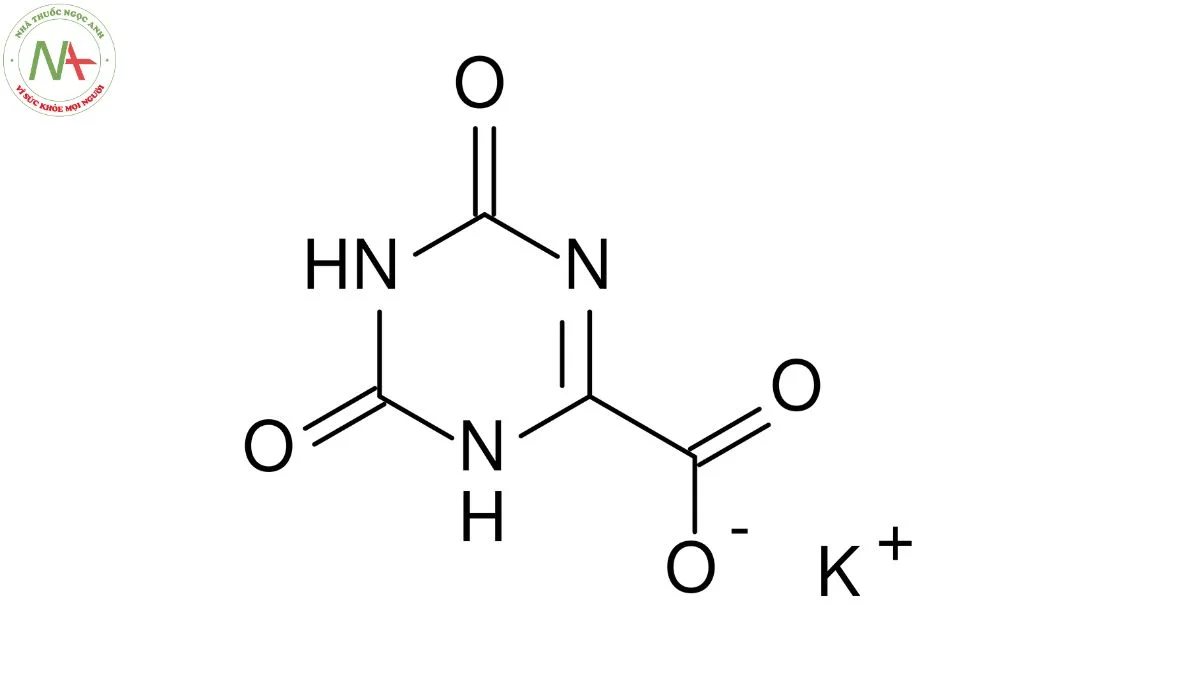
Cấu trúc phân tử
Oteracil, còn được gọi là 5-chloro-2,4-dihydroxypyrimidine, là một hợp chất hữu cơ thuộc nhóm pyrimidine. Điều đặc biệt trong cấu trúc phân tử của Oteracil là có sự xuất hiện của gốc Cl- (chlorine) nằm ở vị trí kế bên nguyên tử nitrogen.
Các tính chất phân tử
Số liên kết hydro cho: 3
Số liên kết hydro nhận: 4
Số liên kết có thể xoay: 1
Diện tích bề mặt tôpô: 108 Ų
Số lượng nguyên tử nặng: 11
Các tính chất đặc trưng
Điểm nóng chảy: 253-255°C
Độ hòa tan trong nước: tan tốt trong nước
Cảm quan
Oteracil hay còn được biết là Axit oxonic có khả năng tan tốt trong nước.
Không có dữ liệu về màu sắc, mùi hay hương vị của chất này.
Dạng bào chế
Thuốc điều trị ung thư Oteracil dạng viên nang, dạng phối hợp với các hoạt chất khác:
Tegafur (FT) 20 mg, Gimeracil (CDHP) 5,8 mg và Oteracil kali (Oxo) 19,6 mg.
Tegafur (FT) 25 mg, Gimeracil (CDHP) 7,25 mg và Oteracil kali (Oxo) 24,5 mg.
Độ ổn định và điều kiện bảo quản của Oteracil
Cần bảo quản Oteracil ở nơi khô ráo, thoáng mát, tránh tác động của ánh sáng, và cần bảo quản ở nhiệt độ dưới 30°C.
Nguồn gốc
Năm 1999, một nhóm các nhà khoa học tại Công ty chế tạo dược phẩm Sankyo (nay là phần của Daiichi Sankyo) ở Nhật Bản đã phát triển oteracil như một phần của một liệu pháp điều trị ung thư. Họ phối hợp oteracil với 5-fluorouracil (5-FU), một chất được sử dụng rộng rãi trong điều trị ung thư, để tạo thành một hợp chất mới gọi là tegafur/uracil/oteracil (Teysuno) hoặc UFT.
UFT là một loại chế phẩm dùng để cải thiện sự chịu đựng của bệnh nhân trong quá trình điều trị ung thư. Oteracil trong UFT có chức năng giảm tác động phụ của 5-FU lên niệu quản và dạ dày. Việc kết hợp oteracil và 5-FU trong UFT giúp tăng hiệu quả của liệu pháp mà vẫn giảm thiểu tác động phụ không mong muốn.
Vào năm 1999, UFT/oteracil đã được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) chấp thuận sử dụng trong điều trị ung thư vùng hạch và ruột giai đoạn cuối. Từ đó, nó đã được sử dụng rộng rãi trong một số loại ung thư, nhất là ung thư đại trực tràng, vùng hạch và dạ dày.
Tegafur/gimeracil/oteracil đã được phê duyệt để sử dụng trong y tế tại Liên minh Châu Âu vào tháng 3 năm 2011.
Trong những năm tiếp theo, nghiên cứu và phát triển trong lĩnh vực điều trị ung thư và dược phẩm đã tiếp tục mở ra nhiều hướng nâng cao hiệu quả và giảm tác động phụ của các liệu pháp.
Dược lý và cơ chế hoạt động
Vai trò chính của Oteracil trong UFT là làm giảm hoạt động của 5-FU trong niêm mạc đường tiêu hóa bình thường và do đó làm giảm độc tính đường tiêu hóa .
Oteracil hoạt động bằng cách ngăn chặn enzyme orotate photphoribosyltransferase (OPRT), có liên quan đến việc sản xuất 5-FU.
Ứng dụng trong y học của Oteracil
Tại Liên minh Châu Âu, tegafur/gimeracil/oteracil được chỉ định để điều trị ung thư dạ dày tiến triển khi dùng kết hợp với cisplatin.
UFT/oteracil trong điều trị ung thư đại trực tràng
UFT/oteracil đã được sử dụng trong điều trị ung thư đại trực tràng giai đoạn cuối, đã di căn và không thể phẫu thuật hoặc điều trị bằng phương pháp khác. UFT/oteracil giúp tăng hiệu quả của liệu pháp 5-fluorouracil (5-FU) trong việc tiêu diệt tế bào ung thư.
Giảm tác động phụ của 5-FU
Một trong những ứng dụng chính của oteracil là giảm tác động phụ của 5-FU lên niệu quản và dạ dày. 5-FU có thể gây ra tác động phụ nghiêm trọng đối với các cơ quan này, và oteracil giúp giảm thiểu những tác động không mong muốn này.
Tăng khả năng chịu đựng cho bệnh nhân ung thư (kéo dài thời gian sống)
UFT/oteracil có khả năng tăng sự chịu đựng và cải thiện chất lượng cuộc sống của bệnh nhân trong quá trình điều trị ung thư. Điều này đặc biệt quan trọng trong việc làm giảm sự khó khăn và tác động phụ của liệu pháp.
Ứng dụng trong các chế độ điều trị khác
Ngoài ứng dụng chính trong điều trị ung thư đại trực tràng, UFT/oteracil cũng đã được nghiên cứu và sử dụng trong một số loại ung thư khác, như ung thư vùng hạch và dạ dày.
Dược động học
Hấp thu
Sau khi dùng một liều duy nhất 50mg, Tmax trung bình của oteracil là 2,0 giờ .
Phân bố
Mặc dù không có dữ liệu tiêm tĩnh mạch ở người, thể tích phân bố có thể ước tính đại khái từ thể tích phân bố biểu kiến và dữ liệu bài tiết qua nước tiểu 23 l/m2 đối với oteracil.
Chuyển hóa
Oteraci liên kết với protein 8,4%. Dựa trên kết quả nghiên cứu in vitro, một phần oteracil bị dịch dạ dày phân hủy thành 5-azauracil (5-AZU) mà không cần tới enzyme phân hủy, sau đó được chuyển hóa thành một loại axit được gọi là axit cyanuric (CA) trong đường tiêu hóa. Chỉ một lượng nhỏ oteracil được chuyển hóa ở gan do tính thấm thấp.
Đào thải
Sau một liều duy nhất, khoảng 3,5% đến 3,9% oteracil đã dùng được bài tiết dưới dạng không đổi qua nước tiểu. Giá trị T1/2 dao động từ 1,8 đến 9,5 giờ đối với oteracil.
Phương pháp sản xuất
Không có dữ liệu
Độc tính của Oteracil
Chưa ghi nhận báo cáo về độc tính khi dùng quá liều Oteracil vì thuốc này không thể tự ý sử dụng mà phải có sự hướng dẫn của các bác sĩ.
Tương tác của Oteracil với thuốc khác
Hiện tại chỉ ghi nhận tương tác thuốc của Teysuno với các thuốc khác, chứ chưa có thông tin chính thức về tương tác thuốc của riêng Oteracil.
Lưu ý khi dùng Oteracil
Lưu ý và thận trọng chung
Cần tránh dùng Oteracil cho những người đang dùng fluoropyrimidine khác (một nhóm thuốc chống ung thư bao gồm tegafur/gimeracil/oteracil) hoặc những người đã có phản ứng nghiêm trọng và bất ngờ với liệu pháp fluoropyrimidine
Cần tránh dùng Oteracil cho những người được biết là không có hoạt động của enzyme DPD, cũng như những người, trong vòng bốn tuần trước đó, đã được điều trị bằng thuốc ngăn chặn enzyme này.
Cần tránh dùng Oteracil cho những người bị giảm bạch cầu, giảm bạch cầu hoặc giảm tiểu cầu nghiêm trọng (lượng bạch cầu hoặc tiểu cầu trong máu thấp).
Cần tránh dùng Oteracil cho những người có vấn đề về thận nặng cần chạy thận nhân tạo.
Cần tránh dùng Oteracil cho những người không nên dùng cisplatin.
Lưu ý cho người đang mang thai
Nếu đang mang thai hoặc có kế hoạch mang thai, cần thảo luận với bác sĩ về việc sử dụng oteracil. Thông thường, trong thời kỳ mang thai chống chỉ định dùng Oteracil.
Lưu ý cho người đang cho con bú
Tương tự nếu bệnh nhân đang thời gian cho con bú, cần thảo luận với bác sĩ. Thuốc có thể chuyển sang sữa mẹ và ảnh hưởng đến sức khỏe của trẻ sơ sinh. Thông thường, chống chỉ định dùng Oteracil cho nhóm đối tượng này.
Lưu ý cho người vận hành máy móc hay lái xe
Oteracil có thể gây buồn ngủ hoặc ảnh hưởng đến khả năng tập trung. Cần thận trọng khi dùng Oteracil cho nhóm đối tượng này.
Một vài nghiên cứu về Oteracil trong Y học
Áp dụng can thiệp điều dưỡng dựa trên bằng chứng trong điều trị ung thư biểu mô tế bào vảy tiến triển ở phổi bằng Erlotinib kết hợp với Tegafur, Gimeracil và Oteracil Kali và ảnh hưởng của nó đến chất lượng cuộc sống
Mục tiêu: Khám phá ứng dụng can thiệp điều dưỡng dựa trên bằng chứng trong điều trị ung thư biểu mô tế bào vảy tiến triển ở phổi bằng erlotinib kết hợp với tegafur, gimeracil và oteracil kali (TS-1) và ảnh hưởng của nó đến chất lượng cuộc sống (QOL).
Phương pháp: Dữ liệu lâm sàng của 92 bệnh nhân ung thư biểu mô tế bào vảy tiến triển ở phổi được điều trị bằng erlotinib và TS-1 tại bệnh viện của chúng tôi (tháng 1 năm 2017 đến tháng 1 năm 2021) đã được phân tích hồi cứu. Bốn mươi sáu bệnh nhân được điều dưỡng thông thường được chọn làm nhóm đối chứng (CG), và 46 bệnh nhân khác được can thiệp điều dưỡng dựa trên bằng chứng cũng được chọn làm nhóm nghiên cứu (SG). Các chỉ số quan sát lâm sàng của hai nhóm được so sánh và phân tích.
Kết quả: Không có sự khác biệt rõ ràng về dữ liệu chung giữa cả hai nhóm ( P > 0,05). Theo EORTC QLQ-C30, so với CG, điểm số về chức năng vai trò, chức năng thể chất, chức năng xã hội, chức năng nhận thức và chức năng cảm xúc ở SG cao hơn đáng kể ( P < 0,05). Sau can thiệp, điểm VAS của bệnh nhân thấp hơn rõ ràng so với trước can thiệp ( P < 0,05), và điểm VAS ở SG sau can thiệp rõ ràng thấp hơn điểm VAS ở CG ( P < 0,05). Sau can thiệp, điểm SAS và SDS thấp hơn so với trước can thiệp và điểm của SG rõ ràng là thấp hơn so với SG ( P< 0,05). So với CG, tỷ lệ mắc các phản ứng bất lợi như tiêu chảy, buồn nôn và nôn, ban đỏ, lở loét và giảm bạch cầu ở SG rõ ràng là thấp hơn ( P < 0,05). So với CG, mức độ “rất hài lòng” và mức độ hài lòng hoàn toàn ở SG rõ ràng là cao hơn ( P < 0,05).
Kết luận: Ứng dụng can thiệp điều dưỡng dựa trên bằng chứng trong điều trị ung thư biểu mô tế bào vảy giai đoạn muộn ở phổi bằng erlotinib kết hợp TS-1 có thể giúp bệnh nhân giảm đau, cải thiện trạng thái tâm lý, giảm tỷ lệ phản ứng bất lợi, cải thiện đáng kể chất lượng cuộc sống và cũng nâng cao sự hài lòng của điều dưỡng lâm sàng.
Hiệu quả và an toàn của tegafur-gimeracil-oteracil kali (TS-1) đối với bệnh ung thư vú di căn: một nghiên cứu hồi cứu đơn trung tâm
Thông tin cơ bản: Tegafur-gimeracil-oteracil kali (TS-1) là một loại thuốc được sử dụng chủ yếu như phương pháp điều trị bậc ba hoặc cao hơn cho bệnh ung thư vú di căn (MBC). Tuy nhiên, vẫn chưa có đủ bằng chứng về hiệu quả lâm sàng của nó và có rất ít báo cáo về nghiên cứu lâm sàng sử dụng TS-1 trước đó. Trong báo cáo này, chúng tôi đã kiểm tra tính hiệu quả và an toàn của liệu pháp TS-1 đối với MBC.
Bệnh nhân và phương pháp: Đối tượng là 46 bệnh nhân mắc MBC được điều trị bằng TS-1 trong khoảng thời gian từ tháng 1 năm 2005 đến tháng 1 năm 2013. Những bệnh nhân này được kiểm tra hồi cứu.
Kết quả: Tỷ lệ đáp ứng khách quan với liệu pháp TS-1 là 30,4%, tỷ lệ lợi ích lâm sàng (CBR) là 50,0% và thời gian trung bình đến khi thất bại điều trị là 10,7 tháng. Khi kiểm tra tại chỗ, CBR cao tại chỗ (46,2%), trong hạch bạch huyết (40,7%), trong xương (42,9%), trong phổi và màng phổi (44,8%). Tuy nhiên nó ở gan thấp (30,0%). Mối quan hệ đã được kiểm tra giữa các yếu tố bệnh lý lâm sàng và hiệu quả của liệu pháp TS-1. Tỷ lệ đáp ứng khách quan (ORR) cao hơn đáng kể ở những bệnh nhân có khoảng thời gian không bệnh (DFI) từ 2 năm trở lên (p=0,039), liệu pháp TS-1 được sử dụng như điều trị bậc ba hoặc sớm hơn (p=0,022), âm tính Tình trạng HER2 (p=0,020) và không có tiền sử điều trị bằng capecitabine (CAP) (p=0,049). CBR cao hơn đáng kể ở những bệnh nhân không có di căn nội tạng (p=0,032), TS-1 được sử dụng như điều trị bậc 3 hoặc sớm hơn (p=0,019), tình trạng HER2 âm tính (p= 0,045), không có tiền sử điều trị CAP (p=0,006) và không có tiền sử điều trị bằng tegafur-uracil/doxifluridine (p= 0,031). Phân tích đa biến cho thấy DFI từ 2 năm trở lên (p=0,035, tỷ lệ chênh lệch: 0,104) là yếu tố dự báo độc lập về hiệu quả được đánh giá bởi ORR. Chỉ có 4 bệnh nhân phải ngừng điều trị do tác dụng phụ và TS-1 nhìn chung được dung nạp tốt.
Kết luận: TS-1 có hiệu quả cao và dung nạp tốt ở bệnh nhân MBC. Việc sử dụng nó ngay từ đầu có thể cho phép duy trì QOL thỏa đáng và nâng cao hiệu quả lâm sàng của nó.
Tài liệu tham khảo
- Drugbank, Oteracil , truy cập ngày 26/08/2023.
- Pubchem, Oteracil , truy cập ngày 26/08/2023.
- Liu, S., Huang, X., Wen, J., Fu, F., & Wang, H. (2021). Application of evidence-based nursing intervention in the treatment of advanced squamous cell carcinoma of the lung by erlotinib combined with tegafur, gimeracil, and oteracil potassium and its influence on quality of life. Journal of Healthcare Engineering, 2021.
- Ishizuna, K., Ninomiya, J., Ogawa, T., Kojima, M., Tsuji, E., Kawashima, M., … & Ueda, Y. (2014). Effectiveness and safety of tegafur-gimeracil-oteracil potassium (TS-1) for metastatic breast cancer: a single-center retrospective study. Gan to Kagaku ryoho. Cancer & Chemotherapy, 41(13), 2577-2582.
