Olaparib
Danh pháp
Tên chung quốc tế
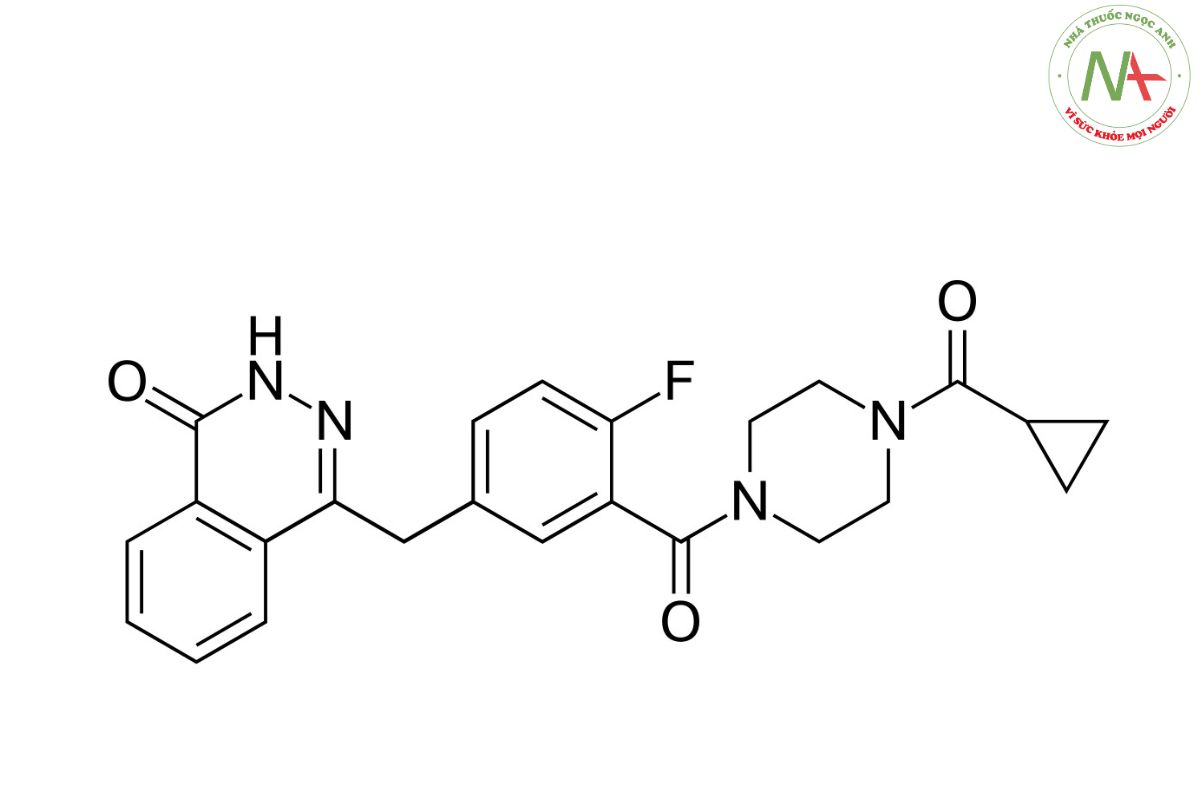
Tên danh pháp theo IUPAC
4-[[3-[4-(cyclopropanecarbonyl)piperazine-1-carbonyl]-4-fluorophenyl]methyl]-2H-phthalazin-1-one
Nhóm thuốc
Thuốc chống ung thư
Mã ATC
L – Chất chống ung thư và điều hòa miễn dịch
L01 – Thuốc chống ung thư
L01X – Thuốc chống ung thư khác
L01XK – Chất ức chế poly (adp-ribose) polymerase (parp)
L01XK01 – Olaparib
Mã UNII
WOH1JD9AR8
Mã CAS
763113-22-0
Cấu trúc phân tử
Công thức phân tử
C24H23FN4O3
Phân tử lượng
434.5 g/mol
Đặc điểm cấu tạo
Olaparib thu được bằng cách ngưng tụ chính thức nhóm cacboxy của 2-fluoro-5-[(4-oxo-3,4-dihydrophthalazin-1-yl)methyl]axit benzoic với amino tự do nhóm N-(cyclpropylcarbonyl) piperazin, là một thành viên của nhóm N-acylpiperazine.
Các tính chất phân tử
Số liên kết hydro cho: 1
Số liên kết hydro nhận: 5
Số liên kết có thể xoay: 4
Diện tích bề mặt cực tôpô: 82,1
Số lượng nguyên tử nặng: 32
Liên kết cộng hóa trị: 1
Dạng bào chế
Viên nén: thuốc Olaparib 150 mg,..
Nguồn gốc
- Olaparib được phát triển và sử dụng lần đầu tiên bởi Cambridge công ty công nghệ sinh học KuDOS Pharmaceuticals có trụ sở tại Vương quốc Anh
- Tháng 12 /2014, EMA và FDA đã phê duyệt olaparib dưới dạng đơn trị liệu điều trị ung thư buồng trứng tiến triển đột biến BRCA
- Tháng 1/ 2018, olaparib đã trở thành chất được FDA chấp thuận ức chế PARP đầu tiên cho bệnh ung thư vú di căn gBRCAm.
- Tháng 8/ 2017, Olaparib được phê duyệt tại Hoa Kỳ để điều trị ung thư phúc mạc nguyên phát tái phát, điều trị duy trì cho người lớn bị ung thư ống dẫn trứng, biểu mô buồng trứng
- Tháng 12/2018, olaparib đã được phê duyệt tại Hoa Kỳ để điều trị duy trì cho người lớn mắc bệnh ung thư ống dẫn trứng hoặc phúc mạc nguyên phát nguy hiểm, biểu mô buồng trứng, hoặc nghi ngờ có hại do BRCA tiến triển
- Tháng 12/2019, olaparib đã được phê duyệt điều trị duy trì ung thư biểu mô tuyến tụy di căn BRCA
- Tháng 03/2022, olaparib đã được phê duyệt để điều trị bổ trợ cho người lớn mắc bệnh ung thư vú giai đoạn đầu
- Tháng 03/2023, Dịch vụ Y tế Quốc gia (NHS) dùng Olaparib cho bệnh nhân ung thư như một phần của liệu pháp nhắm mục tiêu. Olaparib là loại thuốc đầu tiên được FDA phê chuẩn trong nhóm dành cho bệnh nhân ung thư buồng trứng,
Dược lý và cơ chế hoạt động
- Olaparib là một chất ức chế poly(ADP-ribose) polymerase (PARP) đường uống. Olaparib là một chất chống khối u, gây độc tế bào. Nó làm giảm sự phát triển khối u của bệnh ung thư ở người, ức chế sự phát triển của các dòng tế bào khối u chọn lọc. Thuốc có tác dụng chống khối u trên các gen khác liên quan đến quá trình sửa chữa tái tổ hợp tương đồng, dòng tế bào và các mô hình khối u. Olaparib có tác dụng chống khối u khi sử dụng đơn độc, kết hợp với các tác nhân hóa trị liệu hoặc xạ trị. Olaparib ngăn chặn quá trình sửa chữa DNA như một chất gây cảm ứng phóng xạ qua trung gian PARP. Olaparib ức chế poly(ADP-ribose) polymerase, do đó ngăn chặn việc sửa chữa các đứt gãy DNA chuỗi đơn do đó gây chết tổng hợp ở các tế bào ung thư liên quan đến BRCA
- Olaparib là chất ức chế PARP mà chúng là các enzyme tham gia vào các chức năng thiết yếu của tế bào, chẳng hạn như sửa chữa DNA, phiên mã DNA . PARP nhận biết và sửa chữa các tổn thương DNA của tế bào. Olaparib là chất ức chế cạnh tranh chọn lọc lên PARP1, PARP2 và PARP3. Sự ức chế con đường BER của olaparib làm các SSB không được sửa chữa bị tích tụ dẫn đến sự hình thành DSB, đây là dạng tổn thương DNA độc hại nhất. Olaparib có khả năng làm giảm 70% tiến triển bệnh hoặc tử vong
Dược động học
Hấp thu
Olaparib thuốc sau khi uống được hấp thu nhanh chóng. Sau khi dùng một liều duy nhất olaparib 300 mg có AUC là 39,2 μg xh/mL (44%), Cmax là 5,4 μg/mL (32%) và thời gian đạt nồng độ tối đa là 1,5 giờ. Khi dùng Olaparib sau bữa ăn nhiều chất béo không làm thay đổi đáng kể mức độ hấp thu olaparib nhưng làm chậm Tmax.
Chuyển hóa
Olaparib được chuyển hóa bởi cytochrome P450 trải qua các phản ứng oxy hóa cũng như sunfat, liên hợp glucuronide. Có tới 37 chất chuyển hóa của olaparib được phát hiện trong phân, huyết tương, nước tiểu. Các chất chuyển hóa chính của Olaparib là một nhóm piperazin-3-ol mở vòng và hai chất chuyển hóa mono-oxy hóa.
Phân bố
Liều duy nhất 300 mg Olaparib có thể tích phân bố là 158 ± 136 L
Thải trừ
Olaparib có độ thanh thải huyết tương là 4,55 L/giờ, thời gian bán thải là 6,10 giờ.
Ứng dụng trong y học
- Olaparib được dùng đơn trị hoặc kết hợp với bevacizumab để điều trị duy trì cho người lớn bị ung thư phúc mạc nguyên phát, biểu mô ống dẫn trứng, buồng trứng, bị nghi ngờ hoặc có hại có hại do đột biến BRCA, ung thư nguyên phát tiến triển đáp ứng với hóa trị liệu và bệnh ung thư có liên quan đến tình trạng thiếu hụt tái tổ hợp tương đồng. Sự kết hợp giữa olaparib và bevacizumab được FDA chấp thuận như là phương pháp điều trị duy trì đầu tiên cho những bệnh nhân bị ung thư buồng trứng
- Olaparib điều trị bổ trợ cho bệnh nhân trưởng thành đã được điều trị bằng hóa trị tân bổ trợ hoặc bổ trợ mắc bệnh gBRCAm nguy cơ cao
- Olaparib điều trị bệnh ung thư vú di căn gBRCAm, nguy hiểm hoặc nghi ngờ có hại, âm tính HER2
- Olaparib được chỉ định để điều trị ung thư tuyến tiền liệt kháng di căn đột biến gen nghi ngờ có hại hoặc sửa chữa tái tổ hợp tương đồng soma tiến triển sau khi điều trị bằng hormone
Tác dụng phụ
Tác dụng phụ bao gồm: buồn nôn, thiếu máu, thỉnh thoảng mắc bệnh bạch cầu, mệt mỏi, đau cơ và khớp, nôn và chán ăn
Độc tính ở người
Olaparib có thể gây bất thường trong xét nghiệm gan ( không phổ biến). Trong các thử nghiệm ở những bệnh nhân có khối u rắn tiến triển sử dụng olaparib , không có báo cáo về bệnh viêm gan kèm theo vàng da hoặc suy gan.
Tương tác với thuốc khác
- Các chất ức chế chuyển hóa CYP3A có thể làm tăng nồng độ trong huyết thanh của Olaparib
- Hypericum perforatum) có thể làm giảm nồng độ trong huyết thanh của Olaparib
Lưu ý khi sử dụng
- Khi dùng Olaparib cho bệnh nhân suy thận, gan nhẹ và trung bình không cần điều chỉnh liều
- Dùng Olaparib cho bệnh nhân suy gan nặng, suy thận nặng nên điều chỉnh liều theo chỉ định của bác sĩ
- Hiện nay chưa có nghiên cứu chứng minh độ an toàn về việc dùng Olaparib cho trẻ nhỏ, phụ nữ có thai và cho con bú.
Một vài nghiên cứu của Olaparib trong Y học
Olaparib bổ trợ cho bệnh nhân ung thư vú đột biến BRCA1 – hoặc BRCA2
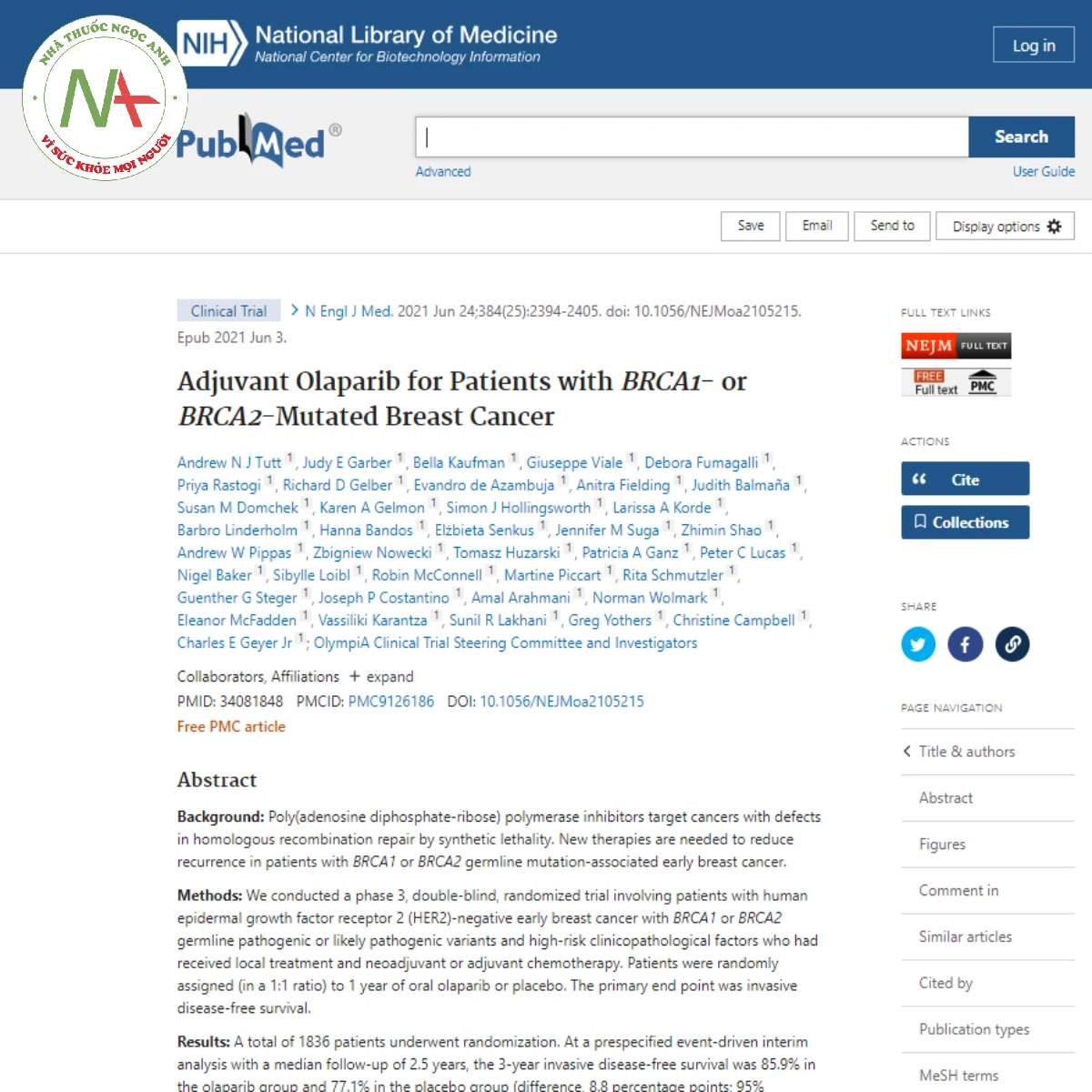
Nghiên cứu tiến hành một thử nghiệm ngẫu nhiên, mù đôi, giai đoạn 3. Bệnh nhân được tham gia nghiên cứu là những bệnh nhân mắc ung thư vú giai đoạn đầu âm tính với HER2 có tiếp xúc với các biến thể dòng mầm BRCA1 hoặc BRCA2 gây bệnh. Bệnh nhân được phân ngẫu nhiên vào 2 nhóm, 1 nhóm cho dùng giả dược và 1 nhóm cho dùng olaparib (tỉ lệ 1:1). Tổng cộng có 1836 bệnh nhân, với thời gian theo dõi trung bình là 2,5 năm cho thấy tỷ lệ sống sót không bệnh xâm lấn trong 3 năm là 85,9% và 77,1% ở nhóm olaparib và ở nhóm giả dược. Tỷ lệ sống sót sau 3 năm là 87,5% là 87,5% ở nhóm olaparib và ở nhóm giả dược. Tỷ lệ tử vong ở nhóm Olaparib ít hơn giả dược (lần lượt là 59 và 86). Kết luận rằng Olaparib bổ trợ cho bệnh nhân ung thư vú đột biến BRCA1 – hoặc BRCA2 có liên quan đến khả năng sống sót lâu hơn đáng kể
Tài liệu tham khảo
- Thư viện y học quốc gia, Olaparib, pubchem. Truy cập ngày 07/10/2023.
- Andrew NJ Tutt 1, Judy E Garber 1, Bella Kaufman 1, Giuseppe Viale 1, Debora Fumagalli (2021),Adjuvant Olaparib for Patients with BRCA1- or BRCA2-Mutated Breast Cancer,pubmed.com. Truy cập ngày 07/10/2023.
