Molnupiravir
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
[(2R,3S,4R,5R)-3,4-dihydroxy-5-[4-(hydroxyamino)-2-oxopyrimidin-1-yl]oxolan-2-yl]methyl 2-methylpropanoate
Molnupiravir thuộc nhóm nào?
Molnupiravir là thuốc gì? Thuốc kháng virus dùng toàn thân
Mã ATC
J – Thuốc chống nhiễm trùng để sử dụng toàn thân
J05 – Thuốc kháng virus dùng toàn thân
J05A – Thuốc kháng virus tác dụng trực tiếp
J05AB – Loại trừ nucleoside và nucleotide. chất ức chế men sao chép ngược
J05AB18 – Molnupiravir
Mã UNII
YA84KI1VEW
Mã CAS
2492423-29-5
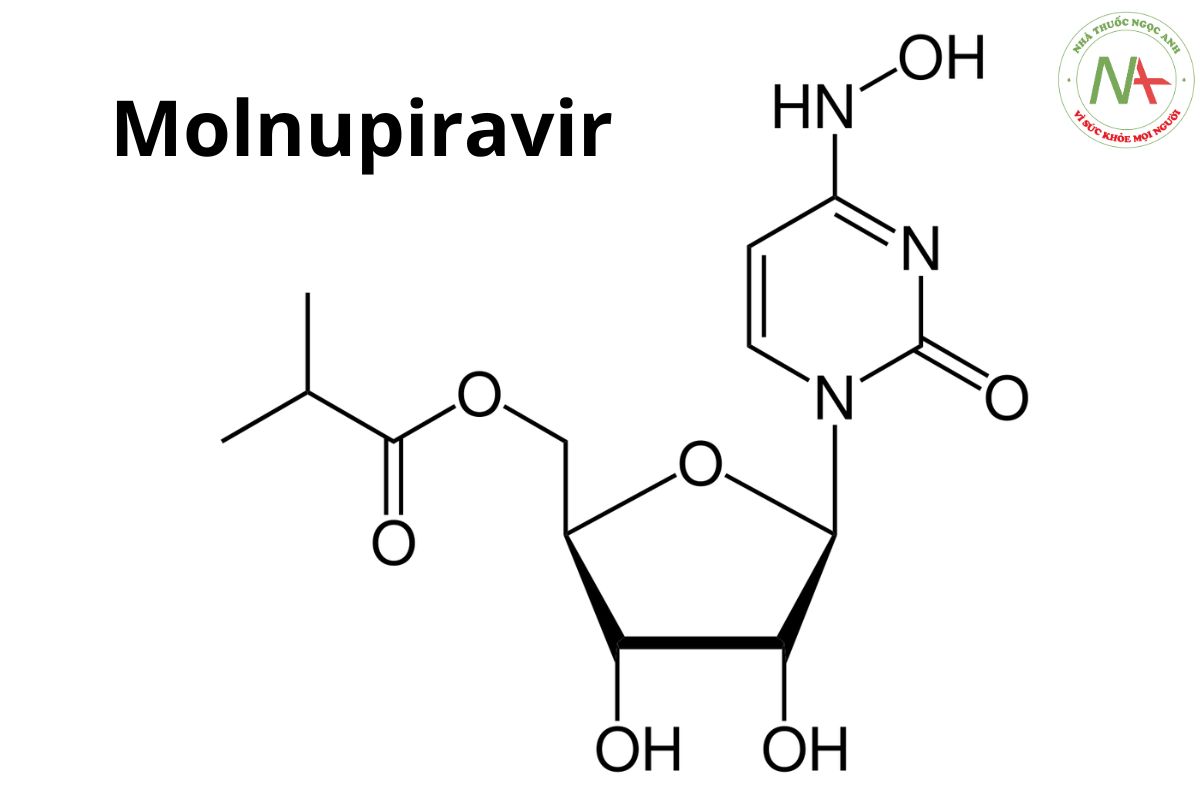
Cấu trúc phân tử
Công thức phân tử
C13H19N3O7
Phân tử lượng
329.31 g/mol
Đặc điểm cấu tạo
Molnupiravir là một chất tương tự nucleoside là N(4)-hydroxycytidine trong đó nhóm 5′-hydroxy được thay thế bằng nhóm oxy (2-methylpropanoyl), là tiền chất của chất tương tự ribonucleoside kháng vi-rút N(4)-hydroxycytidine
Mô hình bóng và que
Các tính chất phân tử
Số liên kết hydro cho: 4
Số liên kết hydro nhận: 7
Số liên kết có thể xoay: 6
Diện tích bề mặt cực tôpô: 141
Số lượng nguyên tử nặng: 23
Số lượng nguyên tử trung tâm xác định được: 4
Liên kết cộng hóa trị: 1
Dạng bào chế
Viên nén: thuốc molnupiravir 400mg,..
Viên nang cứng: thuốc molnupiravir 200mg,..
Nguồn gốc
- Molnupiravir được phát triển tại Đại học Emory. Vào năm 2019, Molnupiravir đã được phê duyệt bởi Viện Dị ứng và Bệnh Truyền nhiễm Quốc gia vào thử nghiệm lâm sàng Giai đoạn I đối với bệnh cúm.
- Vào tháng 3 năm 2020, thuốc chữa covid molnupiravir được nghiên cứu để điều trị các tế bào bị nhiễm loại vi rút Corona mới.
- Vào tháng 11 năm 2022, Viện Sức khỏe và Chăm sóc Xuất sắc Quốc gia Anh đã quyết định không nên sử dụng thuốc đặc trị covid molnupiravir thường xuyên vì Molnupiravir không tạo ra sự khác biệt đáng kể
Dược lý và cơ chế hoạt động
- Molnupiravir dùng để phòng hoặc điều trị các bệnh virus. Cơ chế tác dụng của Molnupiravir là nó liên kết với các thụ thể bề mặt tế bào cụ thể, ức chế DNA polymerase của virus, do đó làm ngăn chặn sự nhân lên của virus và ức chế sự xâm nhập hoặc loại bỏ lớp vỏ của virus; ức chế tổng hợp protein virus; hoặc chặn các giai đoạn cuối của quá trình lắp ráp virus.
- Sau khi bị thủy phân trong cơ thể, Molnupiravir thành N4-hydroxycytidine gây thúc đẩy các đột biến lan rộng trong quá trình sao chép RNA của virus do đó ức chế sự sinh sản của virus thông qua trung gian RNA polymerase hướng RNA.
Dược động học
Hấp thu
Thuốc điều trị covid 19 molnupiravir đạt Cmax là 2970 ng/mL và AUC 0-12h là 8360 h\*ng /mL sau 1,5 giờ khi dùng liều 800 mg/lần/12 giờ theo đường uống
Chuyển hóa
Molnupiravir thuốc bị thủy phân thành N4-hydroxycytidine. Khi vào bên trong tế bào, N4-hydroxycytidine chuyển hóa thành dạng 5′-triphosphate thông qua quá trình phosphoryl hóa.
Phân bố
Molnupiravir phân bố vào các mô.
Thải trừ
3% liều molnupiravir đường uống được thải trừ dưới dạng chất chuyển hóa có hoạt tính N4-hydroxycytidine qua nước tiểu
Tác dụng của thuốc điều trị covid molnupiravir
Chỉ định thuốc molnupiravir như sau:
- Thuốc molnupiravir điều trị covid 19 được sử dụng và được phê duyệt ở Anh để giảm nguy cơ nhập viện và tử vong trong các trường hợp COVID-19 nhẹ đến trung bình
- Molnupiravir chống lại một số bệnh nhiễm vi-rút bao gồm cúm, MERS-CoV
- Tại Hoa Kỳ, thuốc diệt virus covid molnupiravir được phép sử dụng khẩn cấp để điều trị cho người lớn có nguy cơ cao mắc bệnh COVID-19 ở mức độ nhẹ đến trung bình.
Tác dụng phụ của thuốc Molnupiravir
- Thuốc Molnupiravir tác dụng phụ như sau: tiêu chảy, buồn nôn và chóng mặt
- Molnupiravir gây vô sinh: hiện nay chưa có bất kì nghiên cứu đáng tin cậy hay công bố nào về tác dụng phụ này của Molnupiravir
Độc tính ở người
Tác hại của thuốc molnupiravir trong các thử nghiệm lâm sàng cho thấy mức tăng aminotransferase trong huyết thanh không phổ biến và nhẹ và không xảy ra thường xuyên. Molnupiravir cũng Molnupiravir vì vậy tình trạng quá liều Molnupiravir chưa được biết rõ. Tuy nhiên các nghiên cứu trên động vật chứng minh việc dùng Molnupiravir lặp đi lặp lại gây độc tính trên sụn và xương cho bệnh nhân.
Hướng dẫn sử dụng thuốc molnupiravir
Liều dùng Molnupiravir thông thường là 800 mg đường uống mỗi 12 giờ trong 5 ngày, dùng theo đường uống.
Tương tác với thuốc khác
Chưa có dữ liệu
Lưu ý khi sử dụng
- Công dụng của thuốc molnupiravir chưa được chứng minh đầy đủ cho người < 18 tuổi vì vậy không dùng Molnupiravir cho nhóm đối tượng này
- Hiện nay các nghiên cứu về độ an toàn của việc dùng Molnupiravir cho phụ nữ có thai còn hạn chế tuy nhiên trên các thử nghiệm trên động vật cho thấy Molnupiravir gây hại cho thai nhi vì vậy không dùng Molnupiravir cho phụ nữ có thai
- Phụ nữ cho con bú: Không cho con bú trong khi sử dụng thuốc này và trong ít nhất 4 ngày sau liều cuối
- Dùng Molnupiravir càng sớm càng tốt sau khi được chẩn đoán mắc bệnh COVID-19 và trong vòng 5 ngày kể từ khi các triệu chứng đầu tiên xuất hiện.
- Nếu bệnh nhân là phụ nữ khi sử dụng molnupiravir cần có biện pháp tránh thai hiệu quả để tránh mang thai trong khi đang sử dụng thuốc và trong ít nhất 4 ngày sau liều cuối cùng.
- Nếu bệnh nhân là nam giới cần có biện pháp tránh thai hiệu quả để tránh làm bạn tình mang thai, hay bạn tình có khả năng mang thai, đang mang thai, bệnh nhân tiếp tục ít nhất 3 tháng sau liều cuối cùng sử dụng biện pháp tránh thai.
Một vài nghiên cứu của Molnupiravir trong Y học
Nghiên cứu 1
Molnupiravir, một phương pháp điều trị bằng thuốc kháng vi-rút đường uống cho COVID-19

Nghiên cứu được tiến hành báo cáo kết quả của thử nghiệm Giai đoạn 2a đánh giá tính an toàn, khả năng dung nạp và hiệu quả kháng vi-rút của molnupiravir trong điều trị COVID-19. Nghiên cứu bao gồm 202 người tham gia là bệnh nhân ngoại trú được xác nhận nhiễm SARS-CoV-2 và khởi phát triệu chứng trong vòng 7 ngày. Những người tham gia được chọn ngẫu nhiên chia thành 2 nhóm với tỉ lệ 1:1 cho dùng 200 mg molnupiravir hoặc giả dược, hoặc 3:1 dùng molnupiravir (400 hoặc 800 mg) hoặc giả dược, 2 lần/ngày trong 5 ngày. Các kết quả được đánh giá là thời gian để đạt mức RNA vi-rút không thể phát hiện được thông qua phản ứng chuỗi polymerase phiên mã ngược và thời gian để loại bỏ phân lập vi-rút truyền nhiễm từ mẫu phết mũi họng. Kết quả cho thấy việc phân lập vi rút thấp hơn đáng kể ở những người tham gia dùng 800 mg molnupiravir so với giả dược vài ngày thứ 3. Vào ngày thứ 5, virus không được phân lập từ bất kỳ người tham gia nào dùng 400 hoặc 800 mg molnupiravir, nhưng nhóm dùng giả dược thì chỉ đạt kết quả 11,1%. Molnupiravir nhìn chung được dung nạp tốt, với số lượng tác dụng phụ tương tự ở tất cả các nhóm. Từ đó cho thấy Molnupiravir là thuốc đầu tiên được chứng minh là có hiệu quả cao bằng đường uống trong việc giảm vi-rút truyền nhiễm SARS-CoV-2 ở vòm họng và RNA virus, đồng thời có đặc tính an toàn và khả năng dung nạp thuận lợi.
Nghiên cứu 2
Tác dụng phụ của Molnupiravir.
Ngày 23/12/2021, FDA Hoa Kỳ đã quyết định phê duyệt khẩn cấp cho molnupiravir trong điều trị Covid-19 ở người bệnh mức độ nhẹ đến trung bình và có nguy cơ tiến triển nặng, dựa trên kết quả nghiên cứu MOVe-OUT. Ngày 17/02/2022, Cục Quản lý dược (Bộ Y tế) ra quyết định số 69/QĐ-QLD về việc ban hành danh mục 03 thuốc molnupiravir sản xuất trong nước được cấp giấy đăng ký lưu hành [1], đánh dấu việc molnupiravir được phép sản xuất và phân phối chính thức tại Việt Nam sau một thời gian chỉ nằm trong chương trình thử nghiệm quốc gia.
Molnupiravir là tiền thuốc được chuyển hóa thành chất tương tự ribonucleosid N-hydroxycytidin (NHC). NHC phân bố vào các mô và được phosphoryl hóa thành N-hydroxycytidin-5´-triphosphat (NHC-TP) có hoạt tính dược lực. NHC-TP gắn vào ARN của virus bằng enzym ARN polymerase và gây lỗi trong hệ gen của virus dẫn đến ức chế quá trình sao chép.[1]
Các nghiên cứu trên động vật cho thấy molnupiravir gây độc tính trên hệ sinh sản (khả năng gây quái thai), nên mặc dù chưa có dữ liệu ở người, thì các cơ quan quản lý hiện nay đều khuyến cáo không sử dụng thuốc cho phụ nữ có thai.[1], [2]
Đồng thời, người trong độ tuổi sinh sản (cả nam và nữ) đều nên sử dụng biện pháp tránh thai hiệu quả trong suốt thời gian điều trị với thuốc và một khoảng thời gian nữa sau liều điều trị molnupiravir cuối cùng. Tuy nhiên, có sự khác biệt đáng kể trong khuyến cáo giữa nam và nữ về khoảng thời gian cần tránh thai sau điều trị này: với phụ nữ có khả năng mang thai, thì cần tránh thai hiệu quả trong 4 ngày sau khi dùng liều molnupiravir cuối cùng; trong khi ở nam giới có bạn tình có khả năng mang thai, nghiêm ngặt hơn, thì phải tránh thai hiệu quả ít nhất 3 tháng sau liều molnupiravir cuối cùng.
Trong khi dữ liệu nghiên cứu về ảnh hưởng của molnupiravir đối với sức khỏe sinh sản vẫn còn rất hạn chế, có lẽ cách tiếp cận phù hợp nhất để giải thích nguyên nhân cho “sự bất công” ở trên là tiếp cận theo khía cạnh sinh lý học, đó là dựa vào chu kỳ tạo tinh trùng ở nam giới.[3]
Ở nam giới, sự sản sinh tinh trùng xảy ra liên tục trong suốt đời sống sinh dục, kể từ khi bắt đầu dậy thì ở độ tuổi khoảng 15 tuổi [4]. Và một chu kỳ của quá trình tạo ra tinh trùng trưởng thành từ tinh nguyên bào mất khoảng 74 ngày [5], cộng với khoảng thời gian dự trữ trong mào tinh hoàn và ống dẫn tinh, thì khoảng thời gian khuyến cáo ít nhất 3 tháng ~ 90 ngày là khoảng thời gian đủ để “thay máu” lượng tinh binh sẵn có và bị ảnh hưởng bởi việc dùng thuốc molnupiravir kể từ liều cuối cùng (nếu thực sự có ảnh hưởng, câu trả lời còn bỏ ngỏ) [3]. Sau thời gian trên, lực lượng tinh binh mới khỏe mạnh đã được sản sinh ra và sẵn sàng cho nhiệm vụ duy trì nòi giống.
Ngược lại, ở phụ nữ, số lượng trứng là có giới hạn, không sản sinh ra thêm, và xu hướng giảm dần theo thời gian. Ở tuần thứ 30 của thai nhi, cả 2 buồng trứng có khoảng 6 triệu nang trứng nguyên thủy. Sau đó phần lớn bị thoái hóa và chỉ còn lại khoảng 2 triệu nang vào lúc mới sinh, và đến tuổi dậy thì thì chỉ còn lại khoảng 300.000 đến 400.000 nang. Trong suốt thời kỳ sinh sản của phụ nữ (khoảng 30 năm), chỉ có khoảng 400-500 nang này phát triển tới chín và xuất noãn hàng tháng; số còn lại bị thoái hóa. [4], [5]
Trong chu kỳ kinh nguyệt, sau khi rụng trứng, thời gian trứng tồn tại chỉ từ 24-48 giờ [4]. Bên cạnh đó, thời gian sống của tinh trùng ở tử cung cũng chỉ trong 1-2 ngày [5]. Nên thời gian tránh thai 4 ngày với phụ nữ sau điều trị có lẽ là đủ an toàn, để nếu trứng và tinh trùng (nếu có) bị ảnh hưởng bởi thuốc cũng không đủ thời gian sống để dẫn đến sự thụ thai.
Hy vọng góc nhìn này cung cấp một cách hiểu cho khuyến cáo về thời gian tránh thai khác nhau giữa 2 giới, để anh em bớt cảm thấy cuộc đời “bất công” (sinh ra đã vậy, than vãn gì nữa). Khi có nhiều dữ liệu nghiên cứu hơn, thì khoảng thời gian khuyến cáo này có thể sẽ thay đổi (kéo dài hoặc rút ngắn đi) để đảm bảo cả hiệu quả và an toàn của thuốc..
Đặt vấn đề
Molnupiravir là tiền chất kháng virus phân tử nhỏ, đường uống, có hoạt tính chống lại SARS-CoV-2.
Phương pháp
Thử nghiệm pha 3, mù đôi, ngẫu nhiên, đối chứng với giả dược đánh giá hiệu lực và an toàn của việc điều trị bằng Molnupiravir bắt đầu trong vòng 5 ngày sau khi khởi phát các dấu hiệu hoặc triệu chứng ở người trưởng thành
ngoại trú, không được tiêm vaccine, xét nghiệm đã mắc COVID-19 mức độ nhẹ đến trung bình và ít nhất một yếu tố nguy cơ tiến triển COVID-19 nặng. Người tham gia thử nghiệm được chỉ định ngẫu nhiên sử dụng 800 mg Molnupiravir hoặc giả dược 2 lần/ngày trong 5 ngày.
Tiêu chí hiệu lực chính là tỷ lệ nhập viện hoặc tử vong sau 29 ngày, tiêu chí an toàn chính là tỷ lệ mới mắc các biến cố có hại. Một phân tích giữa kỳ được thực hiện khi 50% trong số 1550 người tham gia (số lượng đăng ký mục tiêu) đã được theo dõi đến ngày 29.
Kết quả
1433 BỆNH NHÂN được phân nhóm ngẫu nhiên; 716 BỆNH NHÂN nhóm Molnupiravir và 717 BỆNH NHÂN nhóm giả dược. Ngoại trừ sự mất cân bằng về giới tính, các đặc điểm ban đầu khác ở hai nhóm tương tự nhau.
Tính vượt trội của Molnupiravir đã được đề cao trong phân tích giữa kỳ (xem hình); nguy cơ nhập viện do mọi nguyên nhân hoặc tử vong sau 29 ngày khi dùng Molnupiravir thấp hơn (28 trong 385 người [7,3%]) so với giả dược (53 trong 377 người [14,1%]) (khác biệt nguy cơ: −6,8% ; CI 95%: −11,3 đến −2,4; P = 0,001).
Tuy vậy, phân tích toàn bộ BỆNH NHÂN lại cho thấy hiệu lực thấp hơn phân tích trước đó. Cụ thể, tỷ lệ nhập viện hoặc tử vong sau ngày 29 trong nhóm Molnupiravir thấp hơn so với nhóm giả dược (6,8% [48 trên 709 người] so với 9,7% [68 trên 699 người]; khác biệt nguy cơ: −3,0%; CI 95%: −5,9 đến −0,1).
Kết quả phân tích dưới nhóm phần lớn nhất quán với các kết quả trên; ở một số nhóm nhỏ, ví dụ phân nhóm BỆNH NHÂN đã có bằng chứng nhiễm SARS-CoV-2 trước đó, có tải lượng virus ban đầu thấp và đang mắc đái tháo đường, tỷ lệ nhập viện hoặc tử vong sau 29 ngày thấp hơn ở nhóm dùng thuốc so với giả dược. 1 trường hợp tử vong đã được báo cáo trong nhóm Molnupiravir và 9 trường hợp trong nhóm giả dược cho đến ngày 29.
Các biến cố có hại được báo cáo xảy ra với 216 trong 710 người (30,4%) trong nhóm Molnupiravir và 231 trong 701 người (33,0%) trong nhóm giả dược.
Bàn luận
Điều trị sớm bằng Molnupiravir có thể giảm nguy cơ nhập viện hoặc tử vong ở người trưởng thành mắc COVID-19 chưa được tiêm vaccine, có yếu tố nguy cơ tiến triển bệnh nặng. (Funded by Merck Sharp and Dohme; MOVe-OUT ClinicalTrials.gov number, NCT04575597.) Jayk Bernal A, et al. Molnupiravir for Oral Treatment of COVID-19 in Nonhospitalized Patients [published online ahead of print, 2021 Dec 16]. N Engl J Med. 2021;10.1056/NEJMoa2116044.(doi:10.1056/NEJMoa2116044).
Đầu tháng 10/2021, Merck công bố kết quả phân tích giữa kỳ khả quan về thuốc điều trị COVID-19 đường uống molnupiravir, có thể giúp giảm khoảng 50% nguy cơ tương đối của nhập viện hoặc tử vong trong vòng 30 ngày ở BỆNH NHÂN mắc COVID-19 mức độ nhẹ tới trung bình. Hiệu lực này không bị ảnh hưởng bởi thời gian khởi phát triệu chứng hoặc yếu tố nguy cơ khác. Ngoài ra, từ dữ liệu giải trình tự virus có sẵn ở khoảng 40% người tham gia, Molnupiravir cho thấy hiệu lực nhất quán trên các biến thể virus Gamma, Delta và Mu.
Uỷ ban đánh giá độc lập và FDA đã khuyến nghị việc dừng tuyển thêm BỆNH NHÂN. Nếu được FDA cấp phép cho sử dụng khẩn cấp (EUA), Molnupiravir sẽ là thuốc kháng vi-rút đường uống đầu tiên cho COVID-19. Nguồn tin chi tiết: https://www.businesswire.com/news/home/20211001005189/en/

Cuối tháng 11/2021, Merck công bố kết quả phân tích bổ sung từ thử nghiệm MOVe-OUT cho thấy hiệu lực không cao như phân tích giữa kỳ trước đó. Kết quả đầy đủ trên 1433 BỆNH NHÂN cho thấy Molnupiravir chỉ có thể giúp giảm 30% nguy cơ tương đối của nhập viện và/hoặc tử vong.
Cả châu Âu và Mỹ đều chưa chấp thuận chính thức thuốc này. EMA hiện chỉ cấp phép sử dụng cho mục đích khẩn cấp, FDA vẫn đang chờ đợi và đánh giá dữ liệu. Một số NC khác về Molnupiravir chưa công bố kết quả.

Ngày 22/12/2021, FDA đã cấp phép sử dụng khẩn cấp (EUA) thuốc kháng virus đường uống đầu tiên Paxlovid (bao gồm 2 loại thuốc kháng virus là Nirmatrelvir/Ritonavir). [1] Ngay sau đó, ngày 23/12/2021, FDA cũng đã phê duyệt sử dụng EUA cho thuốc kháng virus molnupiravir. [2]
Dữ liệu các thử nghiệm COVID-19 cho bệnh nhân ngoại trú – Cập nhật ngày 16/01/2022
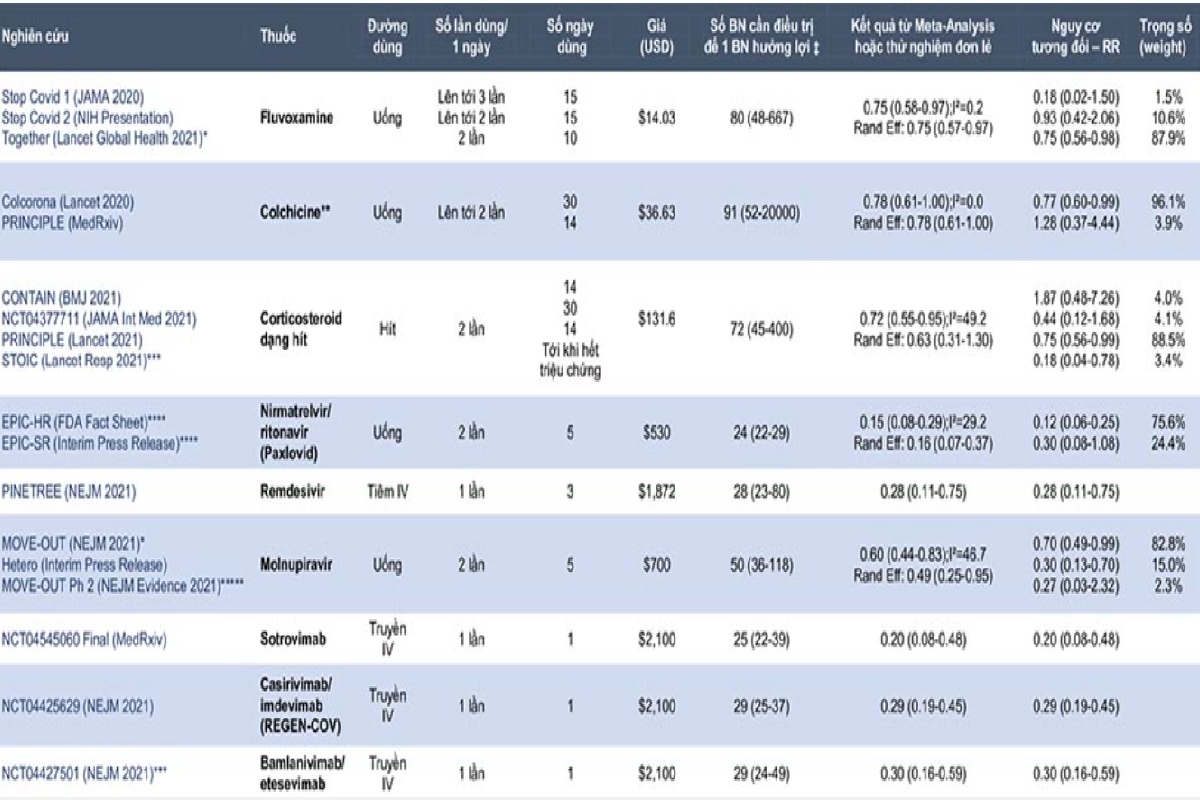
Giá thuốc dựa trên ước tính của GoodRx hoặc các hợp đồng công khai của chính phủ Hoa Kỳ ị Với giả định nguy cơ nhập viện ban đầu là 5%.
* Nhập viện hoặc cấp cứu >24 giờ.
** Giới hạn trên của Cl để tính NNT là 0.999; PRINCIPLE bao gồm nhiều nhóm chứng tiến hành đồng thời; lưu ý ờ PRINCIPLE có 50% BN đã tiêm vaccine *** Bao gồm cả những BN nhập viện khẩn cấp.
**** Không sẵn có nhập viện do mọi nguyên nhân, sử dụng nhập viện do COVID-19 (có thể ước tính quá mức hiệu lực). EPIC-SR gồm những bệnh nhân đã tiêm vaccine ***** Phân nhóm có triệu chứng <5 ngày và ít nhất 1 yếu tố nguy cơ.
Lưu ý: Casirivimab/imdevimab và bamlanivimab/etesevimab – các kháng thẻ dơn dòng sử dụng phồ biến nhát hiện nay có thẻ KHÔNG trung hòa dược omicron.
Sotrovimab được dự đoán là duy trì được một số hoạt tính, tuy nhiên đang trong tình trạng khan hiếm do thiếu nguồn cung. Thuốc kháng virus đường uống nirmatrelvir và molnupiravir chưa có sẵn, và ngay cả khi được phê duyệt thì nguồn cung cũng bị hạn chế nghiêm trọng.
Molnupiravir được báo cáo là có hiệu lực thấp hơn remdesivir, đồng thời có những mối lo ngại về nguy cơ gây đột biến gen
So sánh Molnupiravir với Paxlovid
Molnupiravir và Paxlovid là những thuốc kháng virus điều trị Covid-19 đường uống đầu tiên trên thế giới được phê duyệt sử dụng. Để xem chi tiết so sánh 2 thuốc này mời quý độc giả đọc chi tiết tại đây.
Tài liệu tham khảo
Thư viện y học quốc gia, Molnupiravir, pubchem. Truy cập ngày 08/10/2023.
William Fischer , Joseph J Eron , Wayne Holman , Myron S Cohen , Lôi Phương , Laura J Szewczyk (2021), Molnupiravir, an Oral Antiviral Treatment for COVID-19 , pubmed.com. Truy cập ngày 08/10/2023
[1] Quyết định số 69/QĐ-QLD ngày 17/02/2022 của Cục Quản lý Dược.
[2] FDA Fact Sheet for Healthcare Providers: Emergency Use Authorization for Molnupiravir (02/2022).
[3] Tác giả: AMANDA SHEPPEARD (24/02/2022). Safe sex warning for men taking covid antiviral. Medical Republish. Ngày truy cập: 14/03/2022.
[4] Bộ môn Sinh lý học (ĐH Y Hà Nội) (2005). Sinh lý học (tập II). Nhà xuất bản Y học, Hà Nội.
[5] John E. Hall, Michael E. Hall. (2021) Guyton & Hall Textbook of Medical Physiology 14th edition, Elsevier.
Xuất xứ: Việt Nam
Xuất xứ: Ấn Độ
Xuất xứ: Việt Nam
Xuất xứ: Ấn Độ
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam