Methoxy Polyethylene Glycol - Epoetin Beta
Danh pháp
Tên chung quốc tế
Methoxy Polyethylene Glycol-Epoetin Beta
Nhóm thuốc
Thuốc kích thích tạo máu
Mã ATC
B – Máu và cơ quan tạo máu
B03 – Thuốc chống thiếu máu Sắt
B03X – Các thuốc chống thiếu máu khác
B03XA – Các thuốc chống thiếu máu khác
B03XA03 – methoxy polyethylene glycol-epoetin beta
Phân loại nguy cơ cho phụ nữ có thai
B
Mã UNII
LR3UXN0193
Mã CAS
677324-53-7
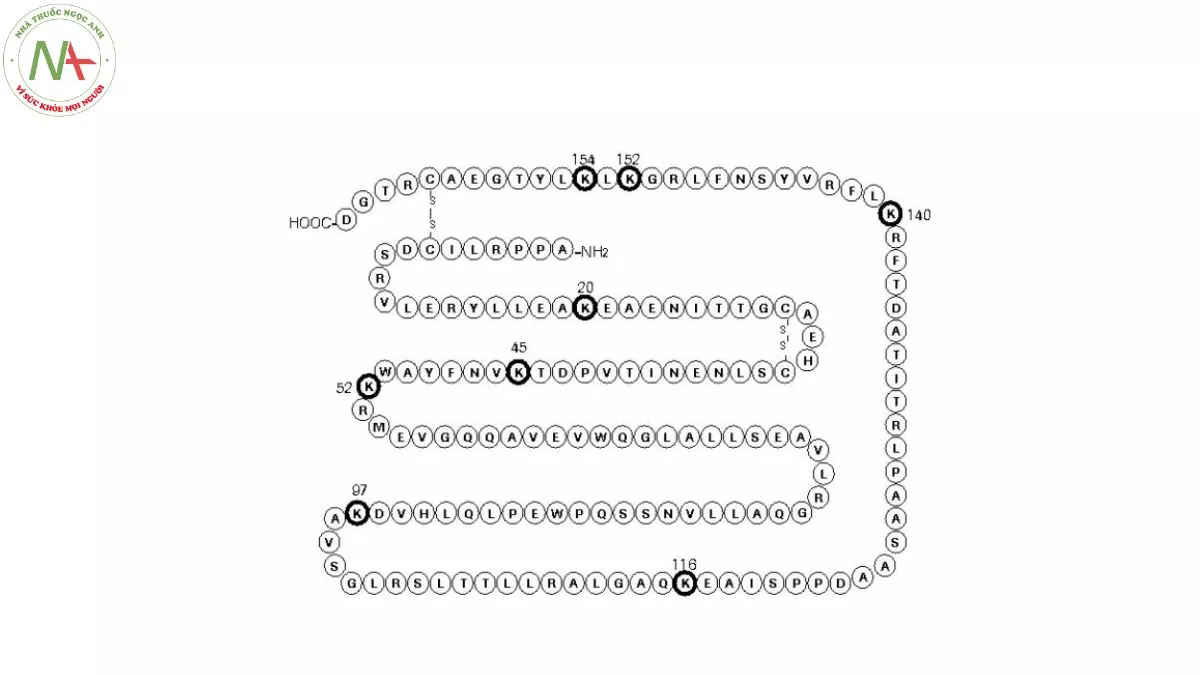
Cấu trúc phân tử
Methoxy polyethylene glycol-epoetin beta là một sự kết hợp đồng hóa trị giữa một protein được tạo ra từ kỹ thuật tái tổ hợp DNA và một chuỗi methoxy-polyethylene glycol (PEG) mạch thẳng
Dạng bào chế
Dung dịch tiêm: 30 ug/0.3mL, 50 ug/0.3mL, 75 μg/0.3ml, 100 mcg / 0.3 mL, 150 ug/0.3mL, 250 mcg / 0.3 mL, 360 ug/0.6mL, 400 mcg / 0.6 mL
Độ ổn định và điều kiện bảo quản
Bảo quản ở nhiệt độ 2 – 8°C (trong tủ lạnh).
Giữ bơm tiêm đóng sẵn thuốc trong hộp giấy để tránh ánh sáng.
Không được làm đông lạnh thuốc.
Đối với bơm tiêm đóng sẵn có thể lấy thuốc từ tủ lạnh để bảo quản ở nhiệt độ phòng (không quá 30°C) cho một liều dùng trong 1 tháng. Sau khi đã lấy ra khỏi tủ lạnh, thuốc phải được sử dụng trong khoảng thời gian này.
Nguồn gốc
Methoxy Polyethylene Glycol-Epoetin Beta (còn được gọi là Mircera – tên thương hiệu) là một dạng biến đổi của hormone erythropoietin, được sử dụng để điều trị thiếu máu và tăng cường sản xuất hồng cầu trong cơ thể. Dạng này có thể kéo dài thời gian hoạt động so với erythropoietin thông thường, cho phép tiêm ít thường xuyên hơn.
Mircera được phát triển bởi hãng dược Roche và đã được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phê duyệt cho sử dụng trong điều trị thiếu máu do suy thận mãn tính hoặc suy thận cấp tính ở người trưởng thành.
Dược lý và cơ chế hoạt động
Erythropoietin, một yếu tố tăng trưởng quan trọng cho sự phát triển của hồng cầu, được tạo ra trong thận và được giải phóng vào hệ tuần hoàn khi cơ thể cảm nhận sự thiếu hụt oxy. Chức năng cốt lõi của nó là tương tác với tế bào tiền thân hồng cầu trong tủy xương, thúc đẩy quá trình sản xuất hồng cầu. Tuy nhiên, ở những người mắc bệnh thận mãn tính (CKD) và các tình trạng liên quan, sự sản xuất tự nhiên của erythropoietin bị giảm sút, gây ra tình trạng thiếu máu. Điều này đặt ra yếu tố nguy cơ cho sức khỏe và sự cần thiết của việc tìm kiếm giải pháp.
Trong bối cảnh này, methoxy polyethylene glycol-epoetin beta (MPG-EPO) nổi lên như một sự lựa chọn đột phá. Thuốc này hoạt động tương tự như erythropoietin tự nhiên bằng cách tương tác với thụ thể erythropoietin trên các tế bào tiền thân hồng cầu trong tủy xương. Một điểm mạnh của MPG-EPO là khả năng duy trì hoạt động kéo dài, giúp hỗ trợ quá trình sản xuất hồng cầu trong khoảng thời gian dài hơn.
Với việc tăng cường quá trình sản xuất hồng cầu, MPG-EPO không chỉ giúp cải thiện tình trạng thiếu máu mà còn cung cấp lợi ích rõ rệt cho sức khỏe tổng thể. Bằng cách cung cấp nguồn cung oxy cần thiết cho các cơ và mô trong cơ thể, thuốc này có thể giúp người bệnh cảm thấy tỉnh táo hơn, giảm mệt mỏi và tăng khả năng hoạt động hàng ngày.
Ứng dụng trong y học
Methoxy Polyethylene Glycol-Epoetin Beta (Mircera) là một thành tựu trong lĩnh vực y học, đóng vai trò quan trọng trong việc điều trị các tình trạng liên quan đến thiếu máu và suy thận. Được phát triển và sản xuất bởi hãng dược phẩm Roche, Mircera đã mang lại nhiều lợi ích thiết thực cho cả bệnh nhân và ngành y học.
Ứng dụng chính của Mircera nằm trong việc điều trị thiếu máu liên quan đến suy thận. Bằng cách thay thế hoặc bổ sung erythropoietin bị thiếu hụt, Mircera kích thích tăng sản xuất hồng cầu, cải thiện tình trạng thiếu máu và làm tăng sự cung cấp oxy cho các cơ và mô trong cơ thể. Điều này có thể cải thiện chất lượng cuộc sống của người bệnh bằng cách giảm mệt mỏi, tăng sức đề kháng và cải thiện khả năng hoạt động hàng ngày.
Một ưu điểm quan trọng của Mircera so với các biến thể khác của erythropoietin là khả năng kéo dài thời gian hoạt động trong cơ thể. Điều này cho phép bệnh nhân chỉ cần tiêm thuốc ít thường xuyên hơn, giảm sự phiền toái và tạo điều kiện thuận lợi hơn cho việc quản lý điều trị.
Dược động học
Hấp thu
Sau khi tiêm chất Methoxy Polyethylene Glycol-Epoetin Beta (MPG-EPO) dưới da cho bệnh nhân mắc bệnh thận mãn tính, quá trình hấp thu diễn ra theo một cách đáng chú ý. Nồng độ tối đa của MPG-EPO trong cơ thể được đạt sau khoảng 72 giờ sau tiêm đối với bệnh nhân có thẩm phân máu, và sau 95 giờ đối với bệnh nhân không có thẩm phân máu. Đây là thời điểm chất này đạt đỉnh độ hiệu quả trong việc kích thích sản xuất hồng cầu.
Khả năng hấp thu tuyệt đối của MPG-EPO sau tiêm cho bệnh nhân có thẩm phân máu là khoảng 62%, trong khi đối với bệnh nhân không thẩm phân máu là 54%. Điều này cho thấy chất này được cơ thể tiếp nhận và sử dụng một cách hiệu quả, đặc biệt là ở những người có thẩm phân máu tốt hơn.
Phân bố
Methoxy Polyethylene Glycol-Epoetin Beta có khả năng phân bố rộng trong cơ thể, với thể tích phân bố ước tính khoảng 5 L. Điều này cho thấy sự lan tỏa của chất trong nhiều vùng khác nhau trong cơ thể sau khi tiêm.
Chuyển hóa
MPG-EPO không trải qua quá trình chuyển hóa. Chất này duy trì cấu trúc ban đầu và hoạt tính của nó sau khi tiêm, giúp duy trì hiệu quả trong quá trình điều trị.
Thải trừ
Trong trường hợp tiêm tĩnh mạch, thời gian bán thải của MPG-EPO là khoảng 134 giờ (tương đương 5,6 ngày). Tốc độ thải trừ toàn thân được xác định là 0,494 ml/giờ/kg, cho thấy sự thải trừ khỏi cơ thể diễn ra chậm và có kiểm soát.
Khi tiêm dưới da, thời gian bán thải của MPG-EPO là khoảng 139 giờ đối với bệnh nhân có thẩm phân máu và 142 giờ đối với bệnh nhân không có thẩm phân máu. Điều này cho thấy sự duy trì tác động kéo dài sau khi tiêm.
Độc tính ở người
Các phản ứng không mong muốn phổ biến nhất (xuất hiện ở hơn 10% trường hợp) khi sử dụng Methoxy Polyethylene Glycol-Epoetin Beta thường bao gồm tăng huyết áp, triệu chứng tiêu chảy và viêm mũi họng. Đây là những biểu hiện thông thường mà người ta thường gặp khi sử dụng thuốc.
Việc xác định liều dùng methoxy polyethylene glycol-epoetin beta là một phần quan trọng của quá trình điều trị. Liều dùng phải được điều chỉnh phù hợp với từng bệnh nhân, và điều này thường đòi hỏi sự quan tâm và theo dõi thường xuyên từ phía bác sĩ.
Việc sử dụng liều quá mức có thể dẫn đến tình trạng quá liều, có thể biểu hiện qua các tác dụng dược lực học cường độ cao, ví dụ như tạo ra số lượng hồng cầu vượt quá mức cần thiết. Trong trường hợp hemoglobin tăng quá mức, việc ngưng sử dụng methoxy polyethylene glycol-epoetin beta là cần thiết để duy trì sự cân bằng và tránh tác động không mong muốn.
Tính an toàn
Hiện chưa có đủ dữ liệu về việc sử dụng Methoxy Polyethylene Glycol-Epoetin Beta đối với phụ nữ mang thai. Các thử nghiệm trên động vật cho thấy không có tác động có hại trực tiếp hoặc gián tiếp của loại thuốc này đối với thai kỳ, sự phát triển của phôi thai/thai nhi, quá trình sinh nở hoặc phát triển sau khi sinh. Tuy nhiên, cần thận trọng khi quyết định sử dụng Methoxy Polyethylene Glycol-Epoetin Beta cho phụ nữ mang thai.
Hiện vẫn chưa rõ liệu Methoxy Polyethylene Glycol-Epoetin Beta có tiết vào sữa mẹ hay không. Một thử nghiệm trên động vật đã chỉ ra rằng chất này xuất hiện trong sữa mẹ. Vì vậy, việc đưa ra quyết định có nên tiếp tục cho con bú trong thời gian dùng Methoxy Polyethylene Glycol-Epoetin Beta cần được xem xét kỹ, đặc biệt là khi cân nhắc giữa lợi ích của việc cho con bú đối với trẻ và lợi ích của việc sử dụng Methoxy Polyethylene Glycol-Epoetin Beta cho mẹ.
Tính an toàn và hiệu quả của Methoxy Polyethylene Glycol-Epoetin Beta đã được chứng minh trong việc điều trị thiếu máu do bệnh thận mãn ở nhóm bệnh nhi từ 5 đến 17 tuổi đang sử dụng thận nhân tạo, sau khi nồng độ hemoglobin của họ đã ổn định bằng phương pháp điều trị khác. Sự hỗ trợ cho việc sử dụng Methoxy Polyethylene Glycol-Epoetin Beta ở nhóm tuổi này dựa trên các nghiên cứu đầy đủ và kiểm soát tốt từ các nghiên cứu trên người lớn, cũng như nghiên cứu xác định liều cho 64 bệnh nhi từ 5 đến 17 tuổi mắc bệnh thận mãn khi đang sử dụng thận nhân tạo. Các hồ sơ phản ứng bất lợi quan sát được ở nhóm bệnh nhi này phù hợp với hồ sơ an toàn tương tự ở người lớn.
Tính an toàn và hiệu quả của Methoxy Polyethylene Glycol-Epoetin Beta chưa được xác định ở bệnh nhân dưới 5 tuổi hoặc ở những tình huống cụ thể như tiêm dưới da, điều trị thiếu máu cho bệnh nhân mắc bệnh thận mãn chưa được lọc máu, và trong trường hợp chưa ổn định hemoglobin bằng phương pháp điều trị khác.
Các nghiên cứu lâm sàng về Methoxy Polyethylene Glycol-Epoetin Beta chưa đủ về số lượng tham gia từ 65 tuổi trở lên để xác định sự tương tác với đối tượng trẻ hơn. Mặc dù không có sự khác biệt rõ rệt về phản ứng giữa bệnh nhân trẻ và bệnh nhân cao tuổi, việc sử dụng cho bệnh nhân cao tuổi nên thận trọng hơn và thường bắt đầu bằng liều thấp, phản ánh tần suất suy giảm chức năng gan, thận, tim và tình trạng điều trị khác.
Tương tác với thuốc khác
Khi sử dụng cùng lúc Methoxy Polyethylene Glycol-Epoetin Beta và belzutifan, cần lưu ý rằng việc kết hợp này có thể tăng nguy cơ mắc các tác dụng phụ nghiêm trọng, bao gồm cả nguy cơ tử vong.
Đối với sự kết hợp giữa Methoxy Polyethylene Glycol-Epoetin Beta và các thuốc carfilzomib hoặc pomalidomide, cần cảnh giác về khả năng tăng nguy cơ gây ra cục máu đông trong cơ thể.
Trong trường hợp sử dụng cùng lúc Methoxy Polyethylene Glycol-Epoetin Beta và lenalidomide hoặc thalidomide, nguy cơ hình thành cục máu đông sẽ tăng lên. Đặc biệt là khi kết hợp chúng với dexamethasone để điều trị bệnh đau tủy. Nguy cơ tăng sẽ lớn hơn so với khi chỉ sử dụng một trong những hoạt chất này để điều trị các tình trạng khác.
Lưu ý khi sử dụng Methoxy Polyethylene Glycol-Epoetin Beta
Những nguyên nhân phổ biến của việc không đáp ứng đầy đủ với yếu tố kích thích tạo hồng cầu thường liên quan đến thiếu sắt và tình trạng viêm nhiễm. Mất máu mãn tính, xơ hóa tủy xương, quá tải nhôm nặng do suy thận, thiếu acid folic hoặc vitamin B12 và sự tan huyết cũng có thể giảm hiệu quả điều trị.
Đề xuất sử dụng liệu pháp bổ sung sắt cho những bệnh nhân có trị số ferritin huyết thanh dưới 100 µg/L hoặc độ bão hòa transferin dưới 20%. Trước và trong quá trình điều trị, cần đánh giá tình trạng sắt của bệnh nhân để đảm bảo hiệu quả của liệu pháp.
Trong trường hợp bệnh nhân có giảm hemoglobin đột ngột, giảm hồng cầu lưới và có kháng thể chống erythropoietin, cần xem xét xét nghiệm tủy xương để loại trừ hội chứng bất sản đơn thuần dòng hồng cầu (PRCA). Nếu xác định là PRCA, cần ngưng sử dụng Methoxy Polyethylene Glycol-Epoetin Beta và không chuyển sang yếu tố kích thích tạo hồng cầu khác.
Trong quá trình điều trị với Methoxy Polyethylene Glycol-Epoetin Beta, huyết áp có thể tăng. Việc kiểm soát huyết áp cần được thực hiện đầy đủ và thường xuyên. Trong trường hợp huyết áp cao không thể kiểm soát bằng thuốc hoặc biện pháp tiết thực, cân nhắc giảm liều hoặc ngưng sử dụng Methoxy Polyethylene Glycol-Epoetin Beta.
Methoxy Polyethylene Glycol-Epoetin Beta là một yếu tố tăng trưởng kích thích quá trình tạo hồng cầu. Thụ thể erythropoietin hiện diện trên bề mặt nhiều tế bào ung thư. Do đó, tương tự như các yếu tố tăng trưởng khác, Methoxy Polyethylene Glycol-Epoetin Beta cũng có khả năng kích thích sự phát triển của các khối u ác tính.
Hiện vẫn chưa có dữ liệu về tính an toàn và hiệu quả của Methoxy Polyethylene Glycol-Epoetin Beta đối với những bệnh nhân bị bệnh hemoglobin, bệnh gan nặng, bệnh động kinh hoặc có số lượng tiểu cầu cao hơn 500 x 109/L. Khi dùng thuốc cho những bệnh nhân này, cần tuân thủ thận trọng và theo dõi chặt chẽ.
Hiện chưa có nghiên cứu về tác động của Methoxy Polyethylene Glycol-Epoetin Beta lên khả năng lái xe và vận hành máy móc. Tuy nhiên, dựa trên cơ chế tác dụng và dữ liệu an toàn đã biết, thuốc không gây ảnh hưởng đáng kể đến khả năng này.
Một vài nghiên cứu của Methoxy Polyethylene Glycol-Epoetin Beta trong Y học
An toàn tim mạch và tử vong do mọi nguyên nhân của Methoxy Polyethylene Glycol-Epoetin Beta và các chất kích thích tạo hồng cầu khác trong bệnh thiếu máu ở bệnh thận mạn
Bối cảnh và mục tiêu: Các chất kích thích tạo hồng cầu điều chỉnh tình trạng thiếu máu ở bệnh nhân suy thận nhưng có thể làm tăng nguy cơ tim mạch. Chúng tôi so sánh kết cục tim mạch và tử vong do mọi nguyên nhân liên quan đến methoxy polyethylene glycol-epoetin beta hàng tháng với kết quả của các thuốc tác dụng ngắn hơn epoetin alfa/beta và darbepoetin alfa ở bệnh nhân thiếu máu BTM.
Thiết kế, bố trí, người tham gia và đo lường: Chúng tôi đã tiến hành một thử nghiệm đa trung tâm, nhãn mở, không thua kém, trong đó bệnh nhân được chọn ngẫu nhiên để nhận methoxy polyethylene glycol-epoetin beta hoặc các thuốc kích thích tạo hồng cầu tham chiếu, được phân tầng theo tình trạng điều trị duy trì hoặc điều chỉnh và C- mức protein phản ứng.
Thử nghiệm có giới hạn không thua kém được xác định trước là 1,20 cho tỷ số nguy cơ (HR) đối với tiêu chí chính (tổng hợp tử vong do mọi nguyên nhân, nhồi máu cơ tim không tử vong hoặc đột quỵ, được đánh giá bởi một ủy ban mù độc lập). Thử nghiệm này được đăng ký với ClinicTrials.gov, số NCT00773513.
Kết quả: Tổng cộng có 2818 bệnh nhân được chọn ngẫu nhiên, nhận methoxy polyethylene glycol-epoetin beta hoặc một chất tham chiếu và được theo dõi trong thời gian trung bình là 3,4 năm (tối đa là 8,4 năm). Trong phân tích theo ý định điều trị đã được sửa đổi, biến cố về điểm cuối chính xảy ra ở 640 (45,4%) bệnh nhân ở nhánh methoxy polyethylene glycol-epoetin beta và 644 (45,7%) ở nhánh tham chiếu (HR 1,03; độ tin cậy 95%). khoảng [95% CI], 0,93 đến 1,15, P=0,004 đối với mức độ không thua kém).
Tỷ lệ tử vong do mọi nguyên nhân không khác nhau giữa các nhóm điều trị (HR 1,06; KTC 95%, 0,94 đến 1,19). Kết quả ở các phân nhóm bệnh nhân chạy thận nhân tạo hoặc được điều trị trong môi trường điều chỉnh hoặc duy trì đều có thể so sánh được với phân tích ban đầu.
Kết luận: Ở những bệnh nhân bị thiếu máu do bệnh thận mạn, methoxy polyethylene glycol-epoetin beta dùng một lần mỗi tháng không thua kém các thuốc kích thích tạo hồng cầu thông thường, tác dụng ngắn về tỷ lệ các biến cố tim mạch nặng hoặc tử vong do mọi nguyên nhân.
Tài liệu tham khảo
- Drugbank, Methoxy Polyethylene Glycol-Epoetin Beta, truy cập ngày 24 tháng 8 năm 2023.
- Locatelli, F., Hannedouche, T., Fishbane, S., Morgan, Z., Oguey, D., & White, W. B. (2019). Cardiovascular Safety and All-Cause Mortality of Methoxy Polyethylene Glycol-Epoetin Beta and Other Erythropoiesis-Stimulating Agents in Anemia of CKD: A Randomized Noninferiority Trial. Clinical journal of the American Society of Nephrology : CJASN, 14(12), 1701–1710. https://doi.org/10.2215/CJN.01380219
- Pubchem, Methoxy Polyethylene Glycol-Epoetin Beta, truy cập ngày 24 tháng 8 năm 2023.
- Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội
Xuất xứ: Đức
Xuất xứ: Đức
Xuất xứ: Thụy Sĩ