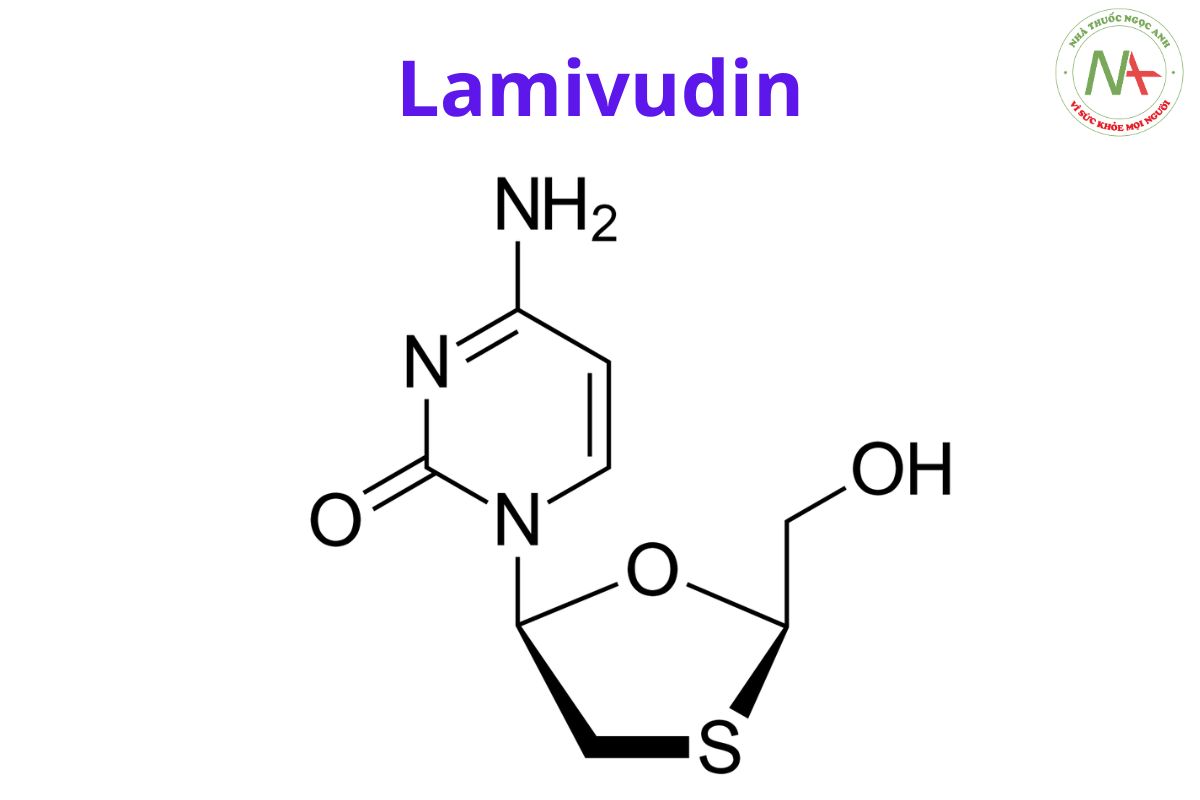
Lamivudin
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
4-amino-1-[(2R,5S)-2-(hydroxymethyl)-1,3-oxathiolan-5-yl]pyrimidin-2-one
Nhóm thuốc
Lamivudine thuốc nhóm chống nhiễm trùng
Mã ATC
J – Thuốc chống nhiễm trùng dùng toàn thân
J05 – Thuốc kháng virus dùng toàn thân
J05A – Thuốc kháng vi-rút tác động trực tiếp
J05AF – Chất ức chế men sao chép ngược nucleoside và nucleotide
J05AF05 – Lamivudin
Mã UNII
2T8Q726O95
Mã CAS
134678-17-4
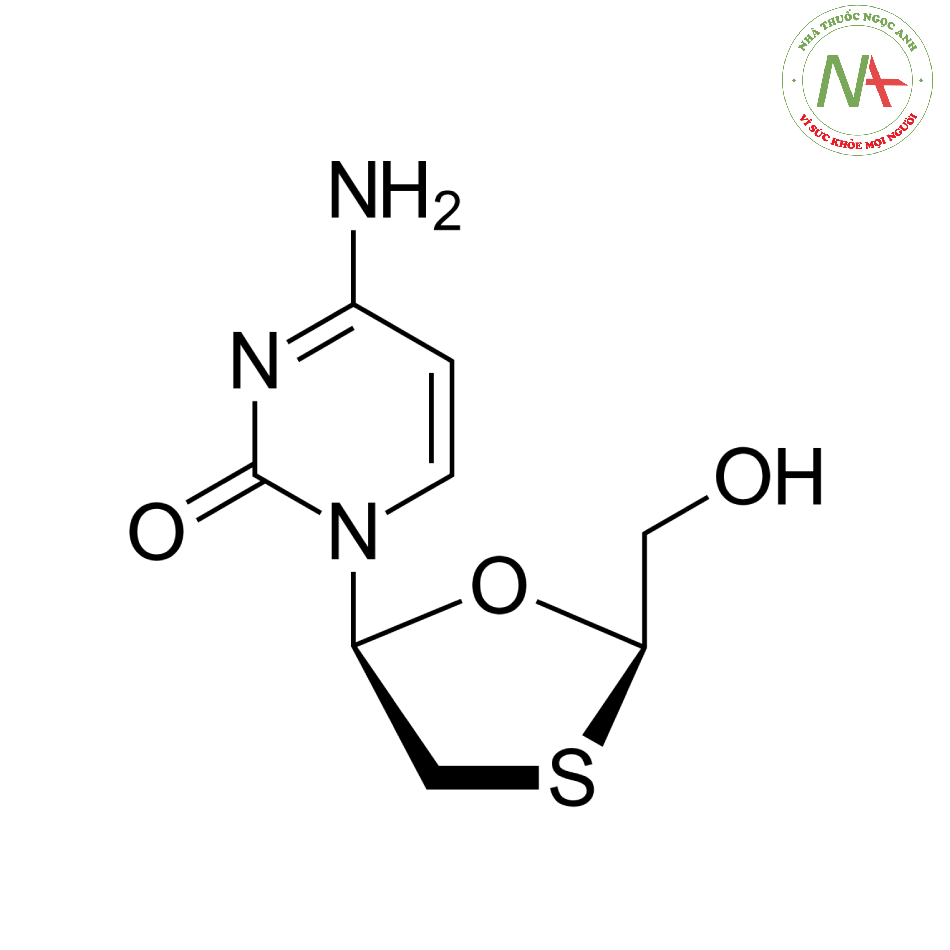
Cấu trúc phân tử
Công thức phân tử
C8H11N3O3S
Phân tử lượng
229,26 g/mol
Cấu trúc phân tử
Các tính chất phân tử
Số liên kết hydro cho: 2
Số liên kết hydro nhận: 4
Số liên kết có thể xoay: 2
Diện tích bề mặt cực tôpô: 113
Số lượng nguyên tử nặng: 15
Số lượng nguyên tử trung tâm xác định được: 2
Liên kết cộng hóa trị: 1
Các tính chất đặc trưng
Lamivudine là một monothioacetal bao gồm cytosine có gốc (2R,5S)-2-(hydroxymethyl)-1,3-oxathiolan-5-yl gắn ở vị trí 1
Nguồn gốc
Lamivudine được phát minh bởi Bernard Belleau khi đang làm việc tại Đại học McGill và Paul Nguyen-Ba tại phòng thí nghiệm IAF BioChem International, Inc. có trụ sở tại Montreal vào năm 1988 và chất đối quang trừ được phân lập vào năm 1989.Các mẫu đầu tiên được gửi đến Yung-Chi Cheng của Đại học Yale để nghiên cứu độc tính của nó. [15] Khi được sử dụng kết hợp với AZT, ông phát hiện ra rằng dạng âm tính của lamivudine làm giảm tác dụng phụ và tăng hiệu quả của thuốc trong việc ức chế men sao chép ngược. [16]Sự kết hợp giữa lamivudin và AZT làm tăng hiệu quả ức chế enzym mà HIV sử dụng để tái tạo vật chất di truyền của nó. Kết quả là, lamivudine được xác định là một tác nhân ít độc hơn đối với DNA ty thể so với các loại thuốc retrovirus khác.
Lamivudine đã được Cục Quản lý Thực phẩm và Dược phẩm (FDA) phê duyệt vào ngày 17 tháng 11 năm 1995, để sử dụng cùng với zidovudine (AZT) và một lần nữa vào năm 2002 dưới dạng thuốc dùng một lần mỗi ngày.
Tính chất
Lamivudine dược thư là chất rắn. Điểm nóng chảy 160-162°C. Độ hòa tan 70 mg/ml
Dạng bào chế
Viên nén bao phim: thuốc Lamivudin 100mg
Viên nén: Lamivudin 150mg
Viên nén phân tán
Cơ chế hoạt động
Lamivudine đi vào tế bào bằng cách khuếch tán thụ động và được phosphoryl hóa thành chất chuyển hóa có hoạt tính của nó, lamivudine triphosphate. Lamivudine triphosphate cạnh tranh với deoxycytidine triphosphate để liên kết với enzyme phiên mã ngược, và sự kết hợp vào DNA dẫn đến kết thúc chuỗi. Lamivudin có ái lực rất thấp đối với men alpha và omega DNA polymerase của người, ái lực vừa phải với beta DNA polymerase và ái lực cao hơn với gamma DNA polymerase.
Dược động học
Hấp thu
Sau khi uống, Lamivudine được hấp thu nhanh chóng với sinh khả dụng khoảng 86%. Lamivudine đạt nồng độ đỉnh trong huyết thanh 0,5 đến 1,5 giờ
Chuyển hóa
Lamivudine được chuyển hóa thành chất chuyển hóa chủ yếu là trans-sulfoxide thông qua con đường chuyển hóa thứ yếu, quá trình chuyển hóa này của Lamivudine được xúc tác bởi sulfotransferase.
Phân bố
Thể tích phân bố biểu kiến của Lamivudine dao động khoảng 1,3 ± 0,4 L/kg. .Lamivudine có khả năng đi qua nhau thai.
Thải trừ
Lamivudine được bài tiết chủ yếu qua nước tiểu dưới dạng không thay đổi với thời gian bán thảo 5-7 giờ.
Ứng dụng trong y học
- Lamivudine được chỉ định kết hợp với các thuốc kháng vi-rút khác để điều trị nhiễm HIV-1. Lamivudine (Epivir HBV) được chỉ định để điều trị nhiễm vi-rút viêm gan B mãn tính.
- Lamivudine đã được sử dụng để điều trị viêm gan B mãn tính với liều thấp hơn so với điều trị HIV/AIDS. Nó cải thiện chuyển đổi huyết thanh của viêm gan B dương tính với kháng nguyên và cải thiện giai đoạn mô học của gan. Sử dụng lamivudine trong thời gian dài dẫn đến sự xuất hiện đột biến của vi rút viêm gan B (YMDD) kháng thuốc.
Tác dụng phụ
Tác dụng phụ nghiêm trọng của Lamivudine bao gồm:
- Viêm tụy, đặc biệt ở trẻ em
- gan mất bù
- Bệnh lý thần kinh ngoại biên
- Đau cơ
- Yếu đuối
- Thiếu máu không tái tạo
- Nhiễm axit lactic với gan to và nhiễm mỡ
- Hội chứng Stevens-Johnson*
- Hội chứng tái tạo miễn dịch
Bệnh nhân nhiễm HIV đã có nguy cơ mắc hội chứng Stevens-Johnson (SJS) cao hơn. Các liệu pháp kết hợp cũng gây khó khăn cho việc phân biệt liệu một loại thuốc đơn lẻ có góp phần gây ra SJS hay không. Không có trường hợp trực tiếp xuất hiện trong tài liệu.
Tác dụng phụ nghiêm trọng xảy ra ở khoảng 5% bệnh nhân tham gia vào tất cả các thử nghiệm lâm sàng. Trẻ em dường như có tỷ lệ sốt và viêm tụy cao hơn bệnh nhân người lớn.
Một số trường hợp nghiên cứu đã chỉ ra rằng lamivudine có thể gây ra tác dụng phụ bất thường như giảm tiểu cầu và viêm quanh móng.
Tác dụng phụ thường gặp:
- Đau đầu
- buồn nôn
- nôn mửa
- Bệnh tiêu chảy
- Giảm cân
- Đau bụng
- Sốt
- Các dấu hiệu và triệu chứng ho và mũi
Độc tính ở người
Lamivudine thường được dung nạp tốt với độc tính nhẹ hơn so với các NRTI khác. Nếu xảy ra quá liều lamivudine, cần theo dõi và chăm sóc hỗ trợ. Lọc máu không phải là phương pháp điều trị đáng tin cậy khi dùng quá liều lamivudine.
Cho đến nay, không có thử nghiệm nào trên người cung cấp bằng chứng về khả năng gây ung thư, đột biến hoặc suy giảm khả năng sinh sản.
Nồng độ ALT huyết thanh tăng cao xảy ra ở một tỷ lệ bệnh nhân bị viêm gan B mãn tính được điều trị bằng lamivudine. Sự gia tăng này dường như là do đợt bùng phát thoáng qua của bệnh viêm gan B mãn tính tiềm ẩn và xảy ra trong ba tình huống trong và sau khi điều trị: khi bắt đầu điều trị (đợt điều trị), khi phát triển kháng thuốc (đợt bùng phát đột phá) và ngay sau khi ngừng điều trị (rút pháo sáng). Các đợt bùng phát điều trị thường xảy ra trong vài tháng đầu điều trị và được đánh dấu bằng sự gia tăng nồng độ aminotransferase huyết thanh không có triệu chứng và hiếm khi có vàng da hoặc triệu chứng (Trường hợp 1). Những đợt bùng phát này xảy ra trong quá trình nồng độ HBV DNA giảm nhanh chóng khi bắt đầu điều trị. Đợt cấp của viêm gan cũng thường xảy ra sau khi phát triển kháng lamivudine, một vài tuần hoặc vài tháng sau khi xuất hiện lần đầu chủng HBV đột biến và nồng độ HBV DNA tăng lên (Trường hợp 2). Cuối cùng, các cơn bùng phát hội chứng cai xảy ra trong khoảng từ 4 đến 12 tuần sau khi ngừng lamivudine và có thể nghiêm trọng, có triệu chứng và thậm chí dẫn đến mất bù trên lâm sàng, suy gan cấp và tử vong hoặc cần ghép gan khẩn cấp. Các đợt bùng phát kháng thuốc và cai nghiện thường xảy ra khi nồng độ HBV DNA cao hoặc tăng lên.
Các dạng nhiễm độc gan khác từ lamivudine là cực kỳ hiếm nếu chúng xảy ra. Lamivudine là một nguyên nhân hiếm gặp gây bất thường xét nghiệm gan hoặc tổn thương gan rõ ràng trên lâm sàng ở bệnh nhân nhiễm HIV mà không bị viêm gan B. Mặc dù một số trường hợp nhiễm axit lactic với gan nhiễm mỡ và suy gan đã được báo cáo ở những bệnh nhân dùng lamivudine, trong mọi trường hợp, các chất tương tự nucleoside khác nhiều hơn rõ ràng liên quan đến tổn thương ty lạp thể [ didanosine , stavudine , zalcitrabine , zidovudine ] cũng được dùng. Không có trường hợp thuyết phục nào về nhiễm toan lactic với mỡ vi nang được báo cáo ở những bệnh nhân viêm gan B thường dùng lamivudine đơn độc hoặc kết hợp với adefovir hoặctenofovir .
Tính an toàn
Lamivudine tự do đi qua nhau thai, thường xuất hiện với nồng độ cực cao và dễ dàng được tìm thấy trong sữa mẹ. Vì vậy không dùng Lamivudine cho phụ nữ có thai và cho con bú.
Tương tác với thuốc khác
- Sử dụng đồng thời lamivudine 150 mg hai lần một ngày, indinavir 800 mg cứ sau 8 giờ và zidovudine 200 mg cứ sau 8 giờ làm giảm 6% AUC của lamivudine, không thay đổi AUC của indinavir và tăng 36% AUC của zidovudin ; không cần điều chỉnh liều.
- Lamivudine và viên phối hợp liều cố định zidovudine không nên dùng đồng thời với viên nén lamivudine hoặc dung dịch uống lamivudine.
- Trong một nghiên cứu nhỏ, sử dụng đồng thời sulfamethoxazole và phối hợp trimethoprim làm tăng AUC của lamivudine 44%, và giảm 29% độ thanh thải lamivudine đường uống và giảm 30% độ thanh thải lamivudine thận; các đặc tính dược động học của sulfamethoxazole và trimethoprim không bị thay đổi khi dùng đồng thời lamivudine; không cần điều chỉnh liều trừ khi bệnh nhân bị suy giảm chức năng thận.
- Lamivudine và zalcitabine có thể ức chế quá trình phosphoryl hóa lẫn nhau và không nên dùng đồng thời.
Lưu ý khi sử dụng
- Nhiễm toan lactic, một độc tính thông thường, không xảy ra thường xuyên với lamivudin; tuy nhiên, những phụ nữ béo phì và đã điều trị bằng liệu pháp miễn dịch trong một thời gian dài dường như có nguy cơ cao hơn. Nếu một bệnh nhân có các triệu chứng, nên ngừng sử dụng lamivudine ngay lập tức. Ngoài ra, nên xem xét chức năng gan của bệnh nhân trước khi bắt đầu dùng lamivudine; những người mắc bệnh gan nên được xếp hạng có nguy cơ cao.
- Bệnh nhân được điều trị bằng thuốc ức chế interferon-alpha có hoặc không có ribavirin khi họ đồng nhiễm HCV nên được theo dõi chặt chẽ về độc tính trên gan, đặc biệt là gan mất bù, do tác dụng giảm phosphoryl hóa pyrimidine của chúng. Nếu tình trạng mất bù hoặc tăng độc tính gan xảy ra, nên giảm hoặc ngừng sử dụng các chất ức chế interferon-alpha có hoặc không có ribavirin.
- Bệnh nhân sử dụng lamivudine để điều trị HBV nên được xét nghiệm HIV-1 và bệnh nhân nhiễm HIV-1 nên được xét nghiệm HBV. Nếu bệnh nhân bị đồng nhiễm, liều lamivudine (EPIVIR-HBV) thấp hơn là không đủ cho bệnh nhân và có thể dẫn đến tăng khả năng kháng vi-rút của một trong hai loại vi-rút cho cả người lớn và trẻ em. Bệnh nhân không nên ngưng dùng lamivudine khi đồng nhiễm HIV-1 và HBV. Đợt cấp viêm gan B nặng, cấp tính có thể xảy ra. Chức năng gan (mức ALT) nên được theo dõi chặt chẽ trong vài tháng sau khi ngừng điều trị và việc bắt đầu điều trị viêm gan B có thể phù hợp với việc ngừng điều trị theo hướng dẫn của bác sĩ.
- Số lượng tế bào CD4+ và tải lượng vi-rút nên được kiểm tra thường xuyên để xác định tiến triển của bệnh HIV-1 và hiệu quả cũng như mức độ thất bại về vi-rút dẫn đến kháng lamivudine trong liệu pháp phối hợp. Bệnh nhân cũng nên được theo dõi sự phát triển của các phản ứng viêm đối với các bệnh nhiễm trùng cơ hội thường thấy ở bệnh nhân HIV (mycobacterium avium, CMV, PCP, TB) cũng như các rối loạn tự miễn dịch trong vài tháng đầu sau khi bắt đầu điều trị bằng thuốc kháng vi-rút kết hợp, bao gồm cả lamivudine. như các triệu chứng của hội chứng phục hồi miễn dịch.
- Cần theo dõi các chỉ số về thận trong suốt quá trình điều trị, đặc biệt ở bệnh nhân mắc bệnh thận mãn tính (CKD). CKD là một sự xuất hiện tự nhiên khi chúng ta già đi, vì vậy có thể cần phải đặc biệt chú ý đến việc điều trị bệnh nhân lớn tuổi.
- Bệnh nhi có tiền sử điều trị bằng thuốc kháng vi-rút hoặc tiền sử viêm tụy cần theo dõi viêm tụy do lamivudine. Bệnh nhân nhi cũng nên biết để tránh các loại thuốc có chứa sorbitol khi sử dụng lamivudine đường uống vì kháng thuốc kháng vi-rút và tỷ lệ ức chế vi-rút thấp hơn có thể xảy ra do tiếp xúc với lamivudine trong huyết tương thấp hơn.
Nghiên cứu về Lamivudine
Hiệu quả và độ an toàn lâu dài của lamivudine, entecavir và tenofovir trong điều trị xơ gan do virus viêm gan B

Bối cảnh & mục đích: Dữ liệu còn hạn chế về hiệu quả và độ an toàn của tenofovir và entecavir khi dùng hơn 1 năm cho bệnh nhân xơ gan liên quan đến viêm gan B. Nghiên cứu đã nghiên cứu tính an toàn và hiệu quả lâu dài của các loại thuốc kháng vi-rút này ở những bệnh nhân nhiễm vi-rút viêm gan B mãn tính (HBV), xơ gan còn bù hoặc mất bù, và so sánh kết quả với những kết quả từ lamivudine.
Phương pháp: Nghiên cứu đã thực hiện phân tích hồi cứu dữ liệu từ 227 bệnh nhân trưởng thành bị nhiễm HBV mạn tính được chẩn đoán xơ gan, bắt đầu từ năm 2005, tại 18 trung tâm trên khắp Thổ Nhĩ Kỳ. Có 104 bệnh nhân xơ gan mất bù, 197 bệnh nhân trước đó chưa điều trị. 72 bệnh nhân dùng tenofovir (theo dõi trong 21,4 ± 9,7 tháng), 77 bệnh nhân dùng entecavir (theo dõi trong 24,0 ± 13,3 tháng) và 74 bệnh nhân dùng lamivudin (theo dõi trong 36,5 ± 24,1 tháng). Nghiên cứu đã thu thập dữ liệu về nhân khẩu học của bệnh nhân và các đặc điểm cơ bản. Kết quả xét nghiệm trong phòng thí nghiệm, kết quả lâm sàng và tác dụng phụ liên quan đến thuốc được so sánh giữa các nhóm.
Kết quả: Mức HBV DNA dưới 400 bản sao/mL đạt được ở 91,5%, 92,5% và 77% bệnh nhân dùng tenofovir, entecavir hoặc lamivudine tương ứng. Mức alanine aminotransferase bình thường hóa ở 86,8%, 92,1% và 71,8% bệnh nhân dùng tenofovir, entecavir và lamivudine tương ứng. Điểm Child-Turcotte-Pugh tăng trong số 8,5% bệnh nhân dùng tenofovir, 15,6% dùng entecavir và 27,4% dùng lamivudine. Tần suất biến chứng do xơ gan, bao gồm bệnh não gan, chảy máu do giãn tĩnh mạch, ung thư biểu mô tế bào gan và tỷ lệ tử vong, là tương tự nhau giữa các nhóm. Lamivudin phải đổi sang thuốc khác ở 32,4% bệnh nhân.
Kết luận: Tenofovir và entecavir hiệu quả và an toàn khi sử dụng lâu dài ở bệnh nhân xơ gan còn bù hoặc xơ gan mất bù do nhiễm HBV.
Tài liệu tham khảo
- Thư viện y học quốc gia, Lamivudine, pubchem. Truy cập ngày 14/08/2023.
- Katherine Taylor; Kristina Fritz; Mayur Parma, Lamivudine,pubmed.com. Truy cập ngày 14/08/2023.
- Metin Küçükazman, Erdem Akbal, Osman Yüksel (2013), Long-term efficacy and safety of lamivudine, entecavir, and tenofovir for treatment of hepatitis B virus-related cirrhosis,pubmed.com. Truy cập ngày 14/08/2023.
Xuất xứ: Ấn Độ
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Điều trị viêm gan B
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Ấn Độ
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt nam
Xuất xứ: Việt Nam
Xuất xứ: Ấn Độ