Eribulin
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
(1S,3S,6S,9S,12S,14R,16R,18S,20R,21R,22S,26R,29S,31R,32S,33R,35R,36S)-20-[(2S)-3-amino-2-hydroxypropyl]-21-methoxy-14-methyl-8,15-dimethylidene-2,19,30,34,37,39,40,41-octaoxanonacyclo[24.9.2.13,32.13,33.16,9.112,16.018,22.029,36.031,35]hentetracontan-24-one
Nhóm thuốc
Thuốc chống ung thư
Mã ATC
L – Chất chống ung thư và điều hòa miễn dịch
L01 – Thuốc chống ung thư
L01X – Thuốc chống ung thư khác
L01XX – Thuốc chống ung thư khác
L01XX41 – Eribulin
Phân loại nguy cơ cho phụ nữ có thai
D
Mã UNII
LR24G6354G
Mã CAS
253128-41-5
Cấu trúc phân tử
Công thức phân tử
C40H59NO11
Phân tử lượng
729.9 g/mol
Cấu trúc phân tử
Eribulin là một chất tương tự xeton macrocycle, một polyether, một ete đa vòng, một xeton tuần hoàn, một hợp chất amino bậc một và một ketal tuần hoàn.
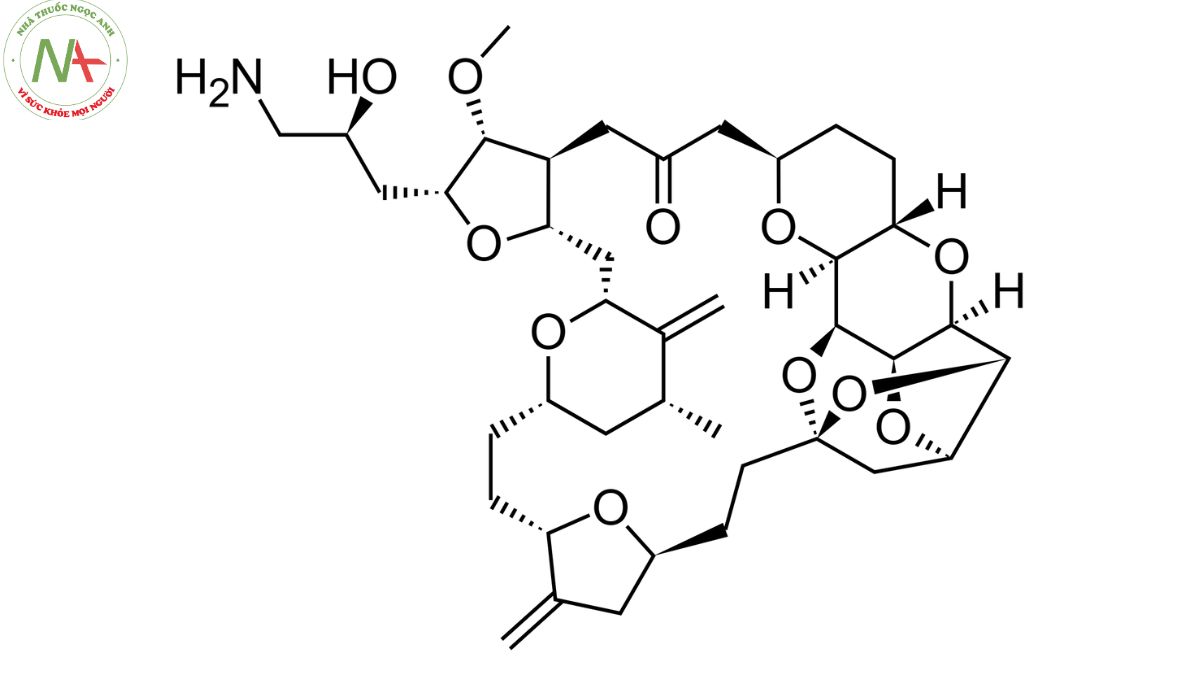
Các tính chất phân tử
Số liên kết hydro cho: 2
Số liên kết hydro nhận: 12
Số liên kết có thể xoay: 4
Diện tích bề mặt tôpô: 146Ų
Số lượng nguyên tử nặng: 52
Các tính chất đặc trưng
Tỷ trọng riêng: 1.3±0.1 g/cm3
Độ tan trong nước: 0.0798 mg/mL
Hằng số phân ly pKa: 9.56
Chu kì bán hủy: 40 giờ
Khả năng liên kết với Protein huyết tương: 49 – 65%
Dạng bào chế
Dung dịch tiêm: 0.44 mg/1mL, 0.5 mg/1mL

Độ ổn định và điều kiện bảo quản
Khuyến khích bảo quản thuốc Eribulin ở nơi khô ráo, thoáng mát, nhiệt độ không quá 30 độ C, không tiếp xúc trực tiếp với ánh sáng cường độ cao. Nên để thuốc cách xa tầm tay trẻ em.
Nguồn gốc
Eribulin là thuốc gì? Eribulin, một chất ức chế vi ống tiên tiến, được biết đến với khả năng hỗ trợ điều trị ung thư vú di căn cho những bệnh nhân đã trải qua ít nhất hai liệu pháp hóa trị trước đó. Sản phẩm này bắt nguồn từ Halichondria okadai, một loài bọt biển, và mở ra một hướng mới trong việc tiếp cận điều trị cho các loại ung thư nghiêm trọng. Không chỉ dừng lại ở đó, Eribulin còn đang được khám phá để mở rộng phạm vi ứng dụng trong việc chống lại các loại khối u rắn khác nhau.
Công trình nghiên cứu và phát triển eribulin đã đạt được bước tiến quan trọng khi phương pháp tổng hợp của nó được công bố lần đầu vào năm 2001, tiếp theo đó là việc giới thiệu một phương pháp tổng hợp mới vào năm 2009, mở đường cho những tiến bộ đáng kể trong lĩnh vực này.
Dược lý và cơ chế hoạt động
Eribulin có tác dụng gì? Eribulin mang đặc điểm là một chất tương tự của halichondrin B, một hợp chất tự nhiên từ biển có khả năng ức chế phân bào mạnh mẽ, với cơ chế hoạt động nổi bật và độc đáo. Được tổng hợp hoàn toàn trong phòng thí nghiệm, Eribulin cơ chế tác động đặc biệt qua việc kết nối với vị trí có ái lực cao trên đầu cộng của vi ống, thể hiện qua cả hành động độc hại và không độc hại đối với tế bào. Nó làm chậm quá trình phân chia tế bào một cách đáng kể và không thể đảo ngược, kích thích quá trình tự tiêu của tế bào ung thư, dựa trên khả năng chống vi khuẩn của mình.
Ngoài ra, nghiên cứu tiền lâm sàng đã phát hiện ra rằng Eribulin còn ảnh hưởng đến môi trường sinh học của các tế bào ung thư và khối u còn lại mà không chỉ giới hạn ở khả năng chống vi khuẩn. Các tác động này bao gồm việc tái cấu trúc mạch máu, cải thiện sự nuôi dưỡng máu cho khối u, giảm tình trạng thiếu oxy trong khối u, thay đổi kiểu hình để đảo ngược quá trình chuyển tiếp biểu mô – trung mô (EMT), và giảm khả năng di chuyển và xâm lấn, qua đó giảm khả năng di căn trong một số mô hình tiền lâm sàng. Đặc biệt, Eribulin còn được chứng minh là tăng biểu hiện của các kháng nguyên đặc trưng cho tế bào cơ trơn và tế bào mỡ trong điều trị tế bào leiomyosarcoma và liposarcoma.
Tuy nhiên, các trường hợp ung thư kháng lại hoạt chất taxane thường không nhạy cảm với Eribulin, điều này được một nghiên cứu gần đây chỉ ra rằng liên quan đến sự biểu hiện của protein đa kháng thuốc 1 (MDR1). Để nâng cao hiểu biết về cách thức Eribulin tác động đến cấp độ tế bào, các nghiên cứu sử dụng Eribulin có nhãn huỳnh quang đã cung cấp cái nhìn sâu sắc vào dược động học và dược lực học của nó trên tế bào đơn lẻ in vivo.
Ứng dụng trong y học
Eribulin chỉ định như một lựa chọn điều trị quan trọng cho bệnh nhân bị ung thư vú di căn hoặc tiến triển cục bộ, cũng như cho những người lớn bị ung thư mỡ không thể phẫu thuật.
Hiện tại, eribulin đang được khám phá tiềm năng trong việc điều trị một loạt các loại khối u rắn, từ ung thư vú đến ung thư phổi không phải tế bào nhỏ, ung thư tuyến tiền liệt, ung thư não, ung thư cổ tử cung, và nhiều loại ung thư khác như ung thư tiết niệu, khối u ác tính, khối u sợi và các loại sarcoma đa dạng.
Trong quá trình phát triển và nghiên cứu, hai biệt dược mới dựa trên eribulin đã được chú trọng: một là công thức liposome và hai là phương pháp điều trị kết hợp với kháng thể.
Công thức liposome của eribulin, được biết đến với tên liposome E7389, đang được thử nghiệm lâm sàng ở Giai đoạn I, và đã cho thấy một số kết quả ban đầu hứa hẹn, bao gồm việc giảm đỉnh nồng độ tối đa và kéo dài thời gian bán hủy của thuốc. Một dự án hợp tác giữa Eisai và Merck đã mang đến một phương pháp điều trị kết hợp mới, sử dụng eribulin cùng với pembrolizumab, một loại chất ức chế PD-1, nhằm mục đích điều trị cho ung thư vú và các loại bệnh ung thư khác đang tiến triển.
Các thử nghiệm lâm sàng này mở ra hướng đi mới trong việc tận dụng hiệu quả của eribulin trong lĩnh vực y học, đặc biệt là trong việc chống lại bệnh ung thư.
Dược động học
Hấp thu và phân bố
Eribulin có một quá trình hấp thu và phân bố đặc trưng với thể tích phân bố dao động từ 43 L/m^2 đến 114 L/m^2, cho thấy sự phân bố rộng rãi trong cơ thể.
Chuyển hóa
Về mặt chuyển hóa, eribulin đặc biệt vì không có chất chuyển hóa chính ở người, và quá trình chuyển hóa bởi CYP3A4 trong ống nghiệm là tối thiểu, chỉ ra rằng eribulin có một lộ trình chuyển hóa đặc biệt.
Thải trừ
Đối với việc thải trừ, eribulin chủ yếu được loại bỏ qua đường phân dưới dạng không thay đổi, với thời gian bán thải khoảng 40 giờ, phản ánh một quá trình thải trừ có tính chất ổn định và kéo dài.
Độc tính ở người
Trong quá trình sử dụng eribulin, bệnh thần kinh ngoại biên là phản ứng phụ phổ biến nhất, đôi khi yêu cầu phải dừng điều trị, với tỷ lệ khoảng 5%.
Các tác dụng phụ của eribulin khác mà bệnh nhân có thể gặp phải bao gồm tình trạng thiếu máu, suy giảm số lượng bạch cầu gây tăng nguy cơ nhiễm trùng nghiêm trọng có khả năng dẫn đến tử vong, rụng tóc, mệt mỏi liên tục, cảm giác tê, ngứa, hoặc cảm giác nóng rát ở tay và chân, ảnh hưởng xấu tới thai nhi, và biến đổi nhịp tim có thể nguy hiểm đến mạng sống.
Về vấn đề quá liều eribulin, có trường hợp được báo cáo khi dùng liều lượng 7,6 mg Eribulin, và không có phương pháp giải độc cụ thể cho tình trạng này. Người bệnh cần được giám sát chặt chẽ và nhận sự can thiệp y tế kịp thời cho đến khi hồi phục.
Tính an toàn
Trong quá trình điều trị bằng eribulin, một loại thuốc hóa trị có tác dụng độc hại đối với tế bào, việc tăng cường aminotransferase và phosphatase kiềm trong huyết thanh là một hiện tượng thường gặp ở bệnh nhân ung thư vú và liposarcoma. Có sự biến đổi rộng lớn trong tỷ lệ tăng ALT, từ 8% đến 83%, với những trường hợp tăng lên hơn 5 lần giới hạn trên của mức bình thường (ULN) chiếm khoảng 2% đến 5%.
Trong các nghiên cứu lâm sàng về eribulin, thuật ngữ “viêm gan nhiễm độc” đã được nhắc đến; tuy nhiên, thông tin chi tiết về nguyên nhân, đặc điểm lâm sàng và tiến trình của các trường hợp này không được rõ ràng, làm cho việc xác định vai trò cụ thể của eribulin trong những phản ứng này trở nên không chắc chắn. Dù có sự gia tăng men huyết thanh, nhưng các báo cáo về tổn thương gan cụ thể và rõ ràng trong lâm sàng sau khi sử dụng eribulin vẫn còn hiếm và chưa được mô tả đầy đủ.
Tương tác với thuốc khác
Khi kết hợp eribulin với các thuốc như Alfentanil, Cyclosporine, Ergotamine, Fentanyl, Pimozide, Quinidin, Sirolimus, và Tacrolimus, cần phải thận trọng và thực hiện theo dõi cẩn thận. Trong trường hợp sử dụng đồng thời với eribulin, việc giám sát chặt chẽ sẽ giúp đảm bảo an toàn và hiệu quả của quá trình điều trị.
Về mặt tương tác enzyme, eribulin không làm ức chế các enzyme CYP1A2, 2B6, 2C8, 2C9, 2C19, 2D6 hoặc 2E1, cho thấy khả năng tương tác thuốc giảm thiểu với các chất chuyển hóa qua đường này.
Lưu ý khi sử dụng Eribulin
Eribulin được quản lý qua đường tiêm tĩnh mạch, và chỉ nên được kê đơn bởi những bác sĩ có kinh nghiệm và chuyên môn sâu về lĩnh vực này. Quy trình tiêm nên được thực hiện bởi nhân viên y tế để đảm bảo an toàn.
Trong quá trình điều trị, việc giám sát công thức máu cẩn thận là bắt buộc, bao gồm việc kiểm tra số lượng bạch cầu và tiểu cầu, vì có thể xảy ra các biến chứng như sốt do giảm bạch cầu trung tính và nhiễm trùng huyết.
Cần đặc biệt chú ý đến các triệu chứng của bệnh lý thần kinh ngoại biên; nếu có dấu hiệu của tình trạng này, có thể cần phải hoãn liệu pháp hoặc điều chỉnh liều lượng giảm dần.
Sử dụng eribulin ở những bệnh nhân có tiền sử về QT kéo dài bẩm sinh nên được tránh, và cần lưu ý rằng thuốc chứa một lượng nhỏ ethanol. Đồng thời, không sử dụng thuốc nếu quá hạn sử dụng hoặc dung dịch tiêm có sự thay đổi về màu sắc.
Sự cẩn trọng cũng nên được áp dụng khi điều trị cho bệnh nhân mắc bệnh suy thận.
Không có thông tin đầy đủ về an toàn khi sử dụng eribulin cho phụ nữ mang thai; do đó, nên tránh sử dụng trong thai kỳ trừ khi nó là tuyệt đối cần thiết, với việc cân nhắc lợi ích và rủi ro cho cả mẹ và thai nhi. Phụ nữ đang cho con bú cũng nên tránh sử dụng eribulin.
Vì thuốc có thể gây mệt mỏi, người bệnh nên thận trọng khi lái xe hoặc vận hành máy móc sau khi tiêm.
Một vài nghiên cứu của Eribulin trong Y học
Đánh giá có hệ thống về hiệu quả thực tế của eribulin đối với bệnh ung thư vú di căn hoặc tiến triển cục bộ

Thông tin cơ bản: Eribulin mesylate (eribulin) được chỉ định cho những bệnh nhân ung thư vú di căn (MBC) trước đây đã nhận được ít nhất hai đợt hóa trị liệu ở Hoa Kỳ và cho những bệnh nhân ung thư vú tiến triển cục bộ (LABC) hoặc MBC đã tiến triển sau ít nhất một đợt hóa trị tại Liên minh châu Âu (EU).
Trong cả hai chỉ định, liệu pháp điều trị trước đó nên bao gồm anthracycline và taxane trong điều trị bổ trợ hoặc di căn. Nhiều nghiên cứu đã đánh giá eribulin ở quần thể ung thư vú trong thế giới thực (RW) để củng cố hiệu quả nhất quán của nó ngoài các thử nghiệm ngẫu nhiên có kiểm soát (RCT) đã đăng ký cho thấy thời gian sống sót trung bình (OS) là 13,1 và 15,9 tháng.
Trong tổng quan tài liệu có hệ thống (SLR) này, chúng tôi tóm tắt bằng chứng tích lũy về hiệu quả RW của eribulin trong LABC/MBC.
Phương pháp: Chúng tôi đã tìm kiếm thông qua cơ sở dữ liệu Medline/PubMed và Embase từ năm 2012 đến năm 2019 để tìm các bài báo báo cáo việc sử dụng RW eribulin trong cài đặt LABC/MBC dòng thứ hai hoặc thứ ba hoặc cao hơn. Vì eribulin cho thấy lợi ích OS lớn nhất trong bệnh ung thư vú âm tính bộ ba (TNBC) trong RCT, nên chúng tôi cũng đã xem xét phân nhóm khối u này. OS và khả năng sống sót không tiến triển (PFS) là kết quả hiệu quả được quan tâm.
Kết quả: Nhìn chung, 34 bài báo hoặc bài tóm tắt đáp ứng các tiêu chí lựa chọn. OS trung bình dao động trong khoảng từ 6,9 đến 28,0 tháng; PFS trung bình thay đổi từ 2,3 đến 14,7 tháng. Tám nghiên cứu đã báo cáo kết quả OS cho bệnh nhân TNBC và OS trung bình dao động trong khoảng từ 3,0 đến 23,0 tháng.
Kết luận: SLR cho thấy độ biến thiên cao trong OS và ở mức độ thấp hơn trong PFS liên quan đến việc sử dụng eribulin trong cài đặt RW. Mặc dù có sự không đồng nhất trong cách sử dụng và phân nhóm bệnh nhân, máy ảnh SLR này hỗ trợ hiệu quả của eribulin đối với LABC/MBC trong thực hành lâm sàng.
Tài liệu tham khảo
- Chabot I, Zhao Q, Su Y. Systematic review of Real-World effectiveness of eribulin for locally advanced or metastatic breast cancer. Curr Med Res Opin. 2020 Dec;36(12):2025-2036. doi: 10.1080/03007995.2020.1835853. Epub 2020 Oct 26. PMID: 33044090.
- Drugbank, Eribulin, truy cập ngày 9 tháng 3 năm 2024.
- Pubchem, Eribulin, truy cập ngày 9 tháng 3 năm 2024.
- Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội.
