Daratumumab
Đặc điểm của Daratumumab
Danh pháp quốc tế
Daratumumab
Dạng bào chế
- Dạng bột đông khô pha tiêm truyền: 1800mg/lọ
- Dung dịch tiêm: 100mg/5mL (20mg/mL), 400mg/20mL (20mg/mL) Daratumumab
Bảo quản
Bảo quản Daratumumab trong tủ lạnh ở nhiệt độ 2-8°C, tránh ánh sáng trực tiếp, không để thuốc bị đông băng.
Daratumumab có tác dụng gì?
Dược lực học
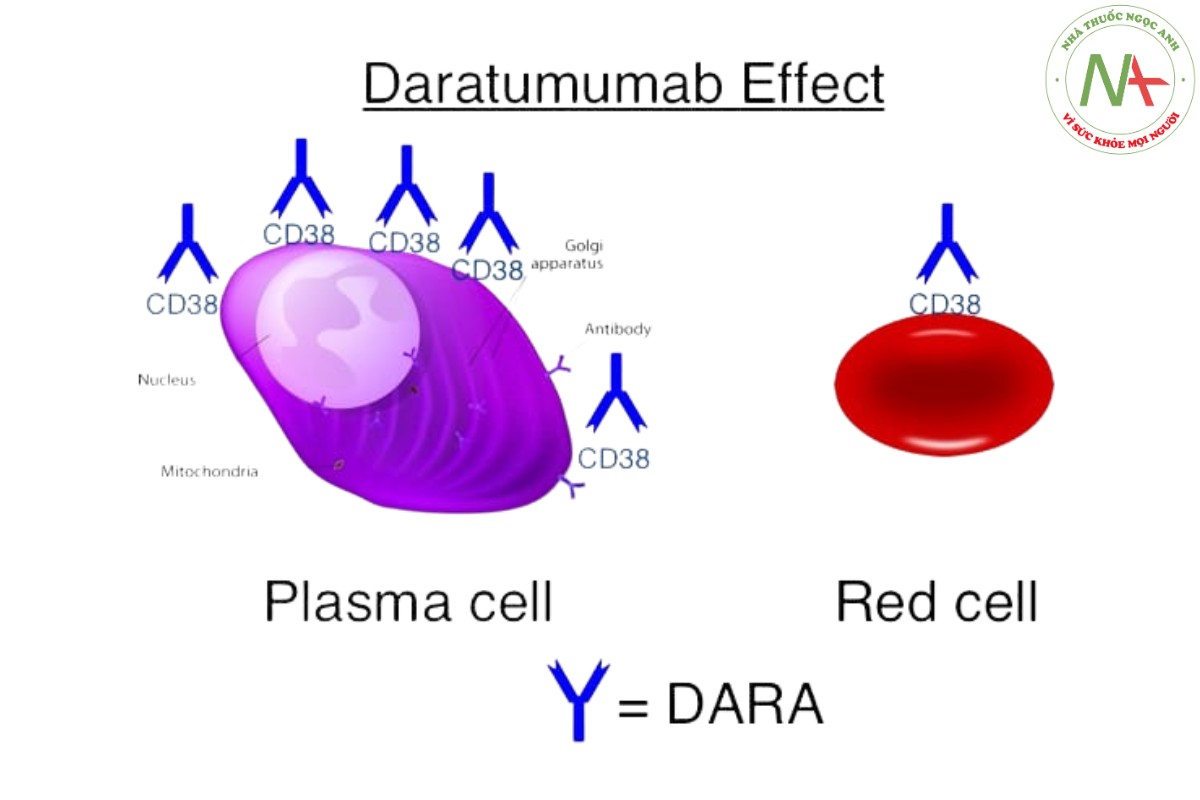
- Trong bệnh đa u tủy xương (multiple myeloma – MM), tế bào ác tính thường mang trên bề mặt protein CD38. CD38 tham gia vào các con đường tín hiệu thúc đẩy sự tăng sinh mạch máu và phát triển tế bào ung thư.
- Daratumumab là một kháng thể đơn dòng được thiết kế đặc biệt để gắn kết với ái lực cao vào protein CD38 trên tế bào ung thư. Khi gắn kết, daratumumab kích hoạt các cơ chế gây độc tế bào phụ thuộc kháng thể (Antibody-Dependent Cell-mediated Cytotoxicity – ADCC) trên các dòng tế bào MM có biểu hiện CD38, thông qua các tế bào miễn dịch tự nhiên (NK cells) có trong tế bào đơn nhân máu ngoại vi. Điểm đáng chú ý là daratumumab không gây độc tính đáng kể trên các tế bào không biểu hiện CD38.
Dược động học
- Hấp thu: Sau khi tiêm dưới da, nồng độ đỉnh trong huyết tương (Cmax) đạt khoảng 592 µg/mL. Khi tiêm tĩnh mạch, Cmax là khoảng 688 µg/mL. Diện tích dưới đường cong (AUC) tương đương nhau giữa hai đường dùng, khoảng 4017 µg/mLngày đối với tiêm dưới da và 4019 µg/mLngày đối với tiêm tĩnh mạch.
- Phân bố: Thể tích phân bố ở trạng thái ổn định sau khi tiêm tĩnh mạch là khoảng 4,7 ± 1,3 lít. Khi tiêm dưới da, thể tích phân bố ở khoang trung tâm ước tính là 5,2 lít.
- Chuyển hóa: Daratumumab chủ yếu bị giáng hóa bởi các enzym trong tế bào thành các peptide và amino acid nhỏ hơn.
- Thải trừ: Thuốc được thải trừ chủ yếu qua đường thận. Thời gian bán thải trung bình là khoảng 20 ngày sau khi tiêm dưới da và khoảng 18 ± 9 ngày sau khi tiêm truyền tĩnh mạch.
Ứng dụng trong y học
Chỉ định
- Daratumumab được chỉ định để điều trị bệnh đa u tủy ở người lớn, có thể sử dụng đơn độc hoặc phối hợp với các thuốc khác như bortezomib, melphalan và prednisone.
- Ngoài ra, thuốc còn được dùng trong điều trị bệnh amyloidosis chuỗi nhẹ (light chain amyloidosis) khi kết hợp với các thuốc khác.
Liều dùng và cách dùng
Liều dùng
Liều dùng khuyến cáo cho người lớn mắc đa u tủy tùy thuộc vào phác đồ điều trị cụ thể:
- Đơn trị liệu và phối hợp với lenalidomide hoặc pomalidomide (chu kỳ 4 tuần) và dexamethasone liều thấp:
- Tuần 1 – 8: 16 mg/kg tiêm tĩnh mạch mỗi tuần (tổng cộng 8 liều).
- Tuần 9 – 24: 16 mg/kg tiêm tĩnh mạch mỗi 2 tuần (tổng cộng 8 liều), liều đầu tiên vào tuần 9.
- Từ tuần 25 trở đi: 16 mg/kg tiêm tĩnh mạch mỗi 4 tuần, liều đầu tiên vào tuần 25.
- Phối hợp với bortezomib, melphalan và dexamethasone:
- Tuần 1 – 6: 16 mg/kg tiêm tĩnh mạch mỗi tuần (tổng cộng 6 liều).
- Tuần 7 – 54: 16 mg/kg tiêm tĩnh mạch mỗi 3 tuần (tổng cộng 16 liều), liều đầu tiên vào tuần 7.
- Từ tuần 55 trở đi: 16 mg/kg tiêm tĩnh mạch mỗi 4 tuần, liều đầu tiên vào tuần 55.
- Phối hợp với bortezomib, thalidomide và dexamethasone:
- Giai đoạn khởi đầu (Tuần 1 – 16):
- Tuần 1 – 8: 16 mg/kg tiêm tĩnh mạch mỗi tuần (tổng cộng 8 liều).
- Tuần 9 – 16: 16 mg/kg tiêm tĩnh mạch mỗi 2 tuần (tổng cộng 4 liều), liều đầu tiên vào tuần 9, sau đó tiến hành hóa trị liều cao và ghép tế bào gốc tự thân (ASCT).
- Giai đoạn củng cố (bắt đầu lại sau ASCT):
- Tuần 1 – 8: 16 mg/kg tiêm tĩnh mạch mỗi 2 tuần, liều đầu tiên vào tuần 1 sau khi tái thiết lập điều trị.
- Phối hợp với bortezomib và dexamethasone:
- Tuần 1 – 9: 16 mg/kg tiêm tĩnh mạch mỗi tuần (tổng cộng 9 liều).
- Tuần 10 – 24: 16 mg/kg tiêm tĩnh mạch mỗi 3 tuần (tổng cộng 5 liều), liều đầu tiên vào tuần 10.
- Từ tuần 25 trở đi: 16 mg/kg tiêm tĩnh mạch mỗi 4 tuần, liều đầu tiên vào tuần 25.
- Phối hợp với carfilzomib và dexamethasone:
- Tuần 1: 8 mg/kg tiêm tĩnh mạch vào Ngày 1 và Ngày 2 (tổng cộng 2 liều).
- Tuần 2 – 8: 16 mg/kg tiêm tĩnh mạch mỗi tuần (tổng cộng 7 liều).
- Tuần 9 – 24: 16 mg/kg tiêm tĩnh mạch mỗi 2 tuần (tổng cộng 8 liều), liều đầu tiên vào tuần 9.
- Từ tuần 25 trở đi: 16 mg/kg tiêm tĩnh mạch mỗi 4 tuần, liều đầu tiên vào tuần 25.
Cách dùng
Thuốc được dùng bằng đường tiêm truyền tĩnh mạch hoặc tiêm dưới da và phải được thực hiện bởi nhân viên y tế có chuyên môn tại các cơ sở y tế được cấp phép.
Chống chỉ định
Chống chỉ định sử dụng Daratumumab ở bệnh nhân có tiền sử quá mẫn với bất kỳ thành phần nào của thuốc.
Tác dụng không mong muốn
Khi điều trị bằng Daratumumab đơn độc, các tác dụng phụ có thể bao gồm giảm số lượng tế bào lympho, giảm bạch cầu trung tính, các phản ứng liên quan đến truyền dịch, giảm tiểu cầu, thiếu máu, mệt mỏi, buồn nôn, đau lưng, sốt, ho, nhiễm trùng đường hô hấp trên, nghẹt mũi, đau khớp, táo bón, tiêu chảy, đau ở các chi, viêm mũi họng, khó thở, giảm cảm giác thèm ăn, nôn mửa, đau đầu và viêm phổi.
Tương tác thuốc
- Abciximab: Sự phối hợp này có thể làm các tác dụng ngoại ý trở nên trầm trọng hơn hoặc xuất hiện thường xuyên hơn.
- Adalimumab: Việc dùng đồng thời có thể làm tăng xác suất gặp phải các phản ứng bất lợi.
- Aducanumab: Khi hai thuốc này được sử dụng cùng nhau, mức độ nghiêm trọng của các tác dụng phụ có thể tăng lên.
- Alemtuzumab: Việc kết hợp điều trị có thể làm tăng khả năng bệnh nhân trải qua các tác dụng không mong muốn.
- Alirocumab: Sự phối hợp này có thể làm tăng nguy cơ hoặc làm gia tăng mức độ của các tác dụng ngoại ý.
Tài liệu tham khảo
Kyeongmin Kim, Mitch A Phelps (2023) Clinical Pharmacokinetics and Pharmacodynamics of Daratumumab. Truy cập ngày 19/04/2025.
