Crizotinib

Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
3-[(1R)-1-(2,6-dichloro-3-fluorophenyl)ethoxy]-5-(1-piperidin-4-ylpyrazol-4-yl)pyridin-2-amine
Nhóm thuốc
Thuốc chống ung thư
Mã ATC
L – Thuốc chống ung thư và điều hòa miễn dịch
L01 – Chất chống ung thư
L01E – Chất ức chế protein kinase
L01ED – Chất ức chế kinase (alk) ung thư hạch bạch huyết
L01ED01 – Crizotinib
Mã UNII
53AH36668S
Mã CAS
877399-52-5
Cấu trúc phân tử
Công thức phân tử
C21H22Cl2FN5O
Phân tử lượng
450,3 g/mol
Cấu trúc phân tử
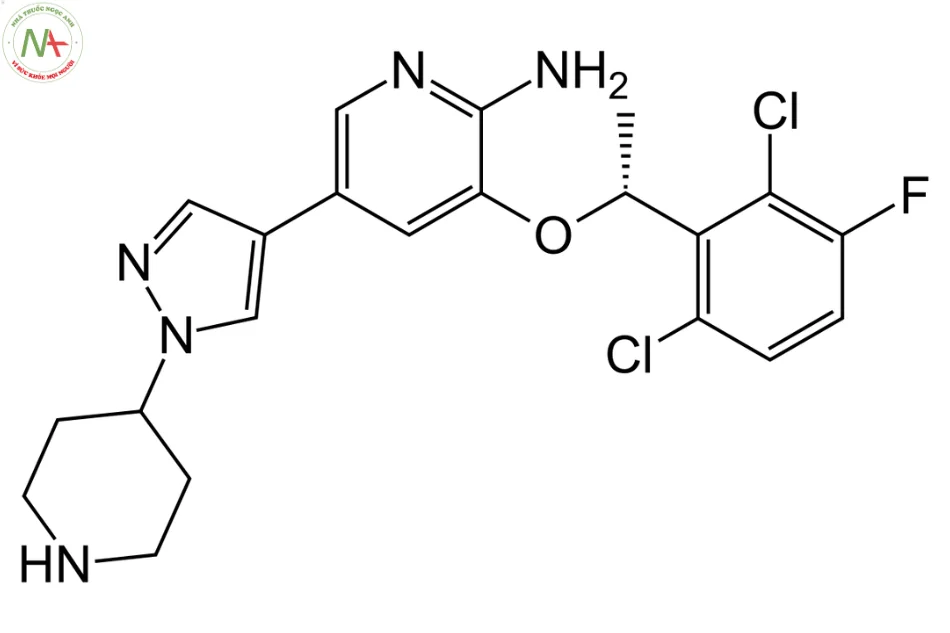
Crizotinib là một 3-[1-(2,6-dichloro-3-fluorophenyl)ethoxy]-5-[1-(piperidin-4-yl)pyrazol-4-yl]pyridin-2-amine có cấu hình R tại trung tâm
Các tính chất phân tử
Số liên kết hydro cho: 2
Số liên kết hydro nhận: 6
Số liên kết có thể xoay: 5
Diện tích bề mặt tôpô: 78 Ų
Số lượng nguyên tử nặng: 30
Các tính chất đặc trưng
Điểm sôi: 599,2±50,0 °C ở 760 mmHg
Tỷ trọng riêng: 1,5±0,1 g/cm3
Độ tan trong nước: 0,00611 mg/mL
Hằng số phân ly pKa: 9.4 và 5.6
Chu kì bán hủy: 42 giờ
Khả năng liên kết với Protein huyết tương: 91%
Dạng bào chế

Viên nang: 200 mg, 250 mg
Độ ổn định và điều kiện bảo quản
Crizotinib nên được bảo quản ở nhiệt độ phòng và tránh ánh sáng trực tiếp. Nhiệt độ và độ ẩm cao có thể ảnh hưởng đến độ ổn định của thuốc.
Nguồn gốc
Crizotinib là một chất ức chế tyrosine kinase được phát triển để điều trị bệnh nhân mắc ung thư phổi không tế bào nhỏ (NSCLC) có biến đổi gen ALK (anaplastic lymphoma kinase).
Nguồn gốc phát hiện Crizotinib liên quan đến nghiên cứu về biến đổi gen trong ung thư phổi. Vào năm 2007, một nhóm nghiên cứu tại Massachusetts General Hospital Cancer Center đã phát hiện ra một biến đổi gen gọi là sự hoán đổi giữa EML4 và ALK trong một số bệnh nhân mắc bệnh ung thư phổi không tế bào nhỏ. Biến đổi này dẫn đến sự kích hoạt không ngừng nghỉ của kinase ALK, góp phần vào sự phát triển của ung thư.
Crizotinib được phát triển như một chất ức chế của kinase ALK, nhằm ngăn chặn sự kích hoạt không kiểm soát của enzyme này và giảm sự phát triển của tế bào ung thư.
Sau khi thực hiện các thử nghiệm lâm sàng, Crizotinib được chấp thuận bởi FDA vào năm 2011 dưới tên thương hiệu Xalkori để điều trị bệnh nhân mắc NSCLC có biến đổi gen ALK.
Dược lý và cơ chế hoạt động
Trong một thử nghiệm giai đoạn 1, 37 bệnh nhân mắc nhiều dạng ung thư đã được điều trị bằng liều crizotinib từ 50 đến 300 mg mỗi ngày hoặc hai lần mỗi ngày.
Trong số họ, hai người mắc ung thư phổi không tế bào nhỏ (NSCLC) có đột biến EML4-ALK đã phản ứng tốt với thuốc, dẫn đến việc tập trung nghiên cứu tiếp theo vào bệnh nhân NSCLC dương tính với ALK.
Ở những người này, 72% sống không tiến triển trong 6 tháng khi sử dụng crizotinib. So với những người không dùng thuốc, bệnh nhân dùng crizotinib có tỷ lệ sống sót sau hai năm cao hơn (54% so với 36%).
Crizotinib có thể gây ra một số biến cố không mong muốn như nhiễm độc gan, bệnh phổi kẽ và mất thị lực nghiêm trọng, đặc biệt ở trẻ em và thanh thiếu niên mắc ung thư hạch tế bào lớn (ALCL) hoặc khối u nguyên bào sợi cơ viêm (IMT).
Về mặt cơ chế, crizotinib là một chất ức chế mục tiêu nhiều thụ thể tyrosine kinase như ALK, HGFR (c-MET), ROS1 và RON. ALK khi kích hoạt có thể ngăn chặn quá trình chết tế bào và thúc đẩy tăng sinh tế bào. Một số bệnh nhân NSCLC có khối u dương tính với ALK, thường xuất hiện do sự kết hợp của ALK với EML4.
Crizotinib hoạt động bằng cách ức chế ALK, giảm sự gia tăng của tế bào mang đột biến này và khả năng sống sót của khối u. Thử nghiệm trên tế bào và chuột đã chứng minh hiệu quả của crizotinib đối với ALK, ROS1 và c-Met.
Ứng dụng trong y học
Crizotinib, một chất ức chế kinase tyrosin, đã mở ra một kỷ nguyên mới trong việc điều trị ung thư với sự hiểu biết sâu rộng về gen học. Đặc biệt trong y học, Crizotinib đã thể hiện vai trò quan trọng của mình trong việc đối phó với một số dạng ung thư cụ thể, đặc biệt là ung thư phổi không tế bào nhỏ (NSCLC).
NSCLC là một trong những dạng ung thư phổ biến nhất trên toàn cầu. Trong nhiều thập kỷ qua, việc điều trị NSCLC chủ yếu dựa vào phẫu thuật, xạ trị và hóa trị. Tuy nhiên, sự xuất hiện của Crizotinib đã cung cấp một lựa chọn điều trị mới cho bệnh nhân NSCLC có biến thể gen anaplastic lymphoma kinase (ALK). ALK là một gen đã được biết đến là nguyên nhân gây ra nhiều dạng bệnh lý khác nhau, bao gồm cả ung thư. Đối với những bệnh nhân NSCLC dương tính với biến thể ALK, Crizotinib đã thể hiện hiệu quả đáng kể trong việc kiểm soát và giảm tiến trình bệnh.
Một trong những điểm nổi bật của Crizotinib là khả năng tác động mục tiêu vào đúng các tế bào ung thư mà không ảnh hưởng nhiều đến các tế bào khỏe mạnh. Điều này giúp giảm thiểu tác dụng phụ thường gặp ở các phương pháp điều trị ung thư truyền thống. Mặc dù vẫn còn một số tác dụng phụ liên quan đến việc sử dụng Crizotinib, nhưng so với lợi ích mà nó mang lại, những tác dụng phụ này thường được coi là có thể chấp nhận được.
Không chỉ hiệu quả đối với NSCLC, Crizotinib cũng đã được chỉ định để điều trị u lympho tế bào lớn anaplastic hệ thống (ALCL) dương tính với ALK. Đối với các bệnh nhi và thanh thiếu niên mắc phải dạng ung thư này, Crizotinib đã mang lại hi vọng và cơ hội cho cuộc sống.
Ngoài ra, thuốc cũng đã cho thấy triển vọng trong việc điều trị một số dạng khối u khác, như khối u nguyên bào sợi cơ (IMT). Mặc dù nghiên cứu về ứng dụng của Crizotinib trong các dạng ung thư khác vẫn đang tiếp tục, nhưng những kết quả tích cực đã đánh dấu một bước tiến quan trọng trong lĩnh vực y học.
Tuy nhiên, như mọi phát minh trong y học, việc sử dụng Crizotinib không phải lúc nào cũng thuận lợi. Việc tìm hiểu rõ về cơ chế tác động, tác dụng phụ, cũng như các tương tác thuốc khác là điều cần thiết. Hơn nữa, việc phát triển sự kháng cự với Crizotinib cũng là một thách thức đối với các nhà nghiên cứu.
Dược động học
Hấp thu
Ở bệnh nhân mắc các bệnh như ung thư tuyến tụy, đại trực tràng, sarcoma, u lympho tế bào lớn anaplastic và ung thư phổi không tế bào nhỏ (NSCLC) khi dùng crizotinib từ 100 mg mỗi ngày đến 300 mg hai lần mỗi ngày, AUC và Cmax trung bình tăng tỷ lệ theo liều lượng. Crizotinib sau một liều duy nhất có Tmax trung bình từ 4-6 giờ.
Với liều crizotinib 250 mg hai lần mỗi ngày (n=167), AUC trung bình đạt 2321,00 ng⋅hr/mL, Cmax là 99,60 ng/mL và Tmax khoảng 5 giờ. Sinh khả dụng tuyệt đối của thuốc trung bình là 43%, có biến động từ 32% đến 66%. Bữa ăn giàu chất béo làm giảm khoảng 14% AUC0-INF và Cmax của crizotinib.
Tuổi, giới tính và dân tộc (như so sánh giữa bệnh nhân châu Á và không châu Á) không ảnh hưởng đến dược động học của crizotinib một cách đáng kể. Đối với bệnh nhân dưới 18 tuổi, trọng lượng cơ thể lớn hơn liên quan đến mức tiếp xúc thấp hơn với crizotinib.
Phân bố
Sau một lần tiêm tĩnh mạch, thể tích phân bố trung bình của crizotinib đạt 1772 L. Thuốc này liên kết 91% với protein trong huyết tương và độ liên kết này không bị biến đổi theo nồng độ thuốc.
Chuyển hóa
Ở gan, crizotinib chủ yếu bị chuyển hóa bởi CYP3A4 và CYP3A5 và sau đó trải qua quá trình khử O-dealkyl và liên hợp ở giai đoạn 2. Có một phần thuốc không chuyển hóa có thể được đào thải, như thông qua bài tiết mật.
PF-06260182, chất chuyển hóa chính của crizotinib, bao gồm hai chất đồng phân, PF-06270079 và PF-06270080. Khi so sánh với crizotinib, chúng có hiệu quả thấp hơn trong việc ức chế kinase.
Thải trừ
Sau một lần dùng 250 mg crizotinib đánh dấu bằng phóng xạ, khoảng 63% liều được tìm thấy trong phân và 22% trong nước tiểu. Trong phân và nước tiểu, crizotinib gốc chiếm khoảng 53% và 2,3% liều, tương ứng. Khi ổn định với liều 250 mg hai lần mỗi ngày, độ thanh thải của crizotinib là 60 L/giờ, thấp hơn sau một lần dùng 250 mg.
Sau một lần dùng crizotinib, thời gian bán huỷ cuối cùng trong huyết tương là 42 giờ.
Độc tính ở người
Liều lượng tối ưu cho crizotinib tương đương với liều khuyến nghị (250 mg hai lần mỗi ngày). Quyết định này dựa trên các nghiên cứu giai đoạn 1 với bệnh nhân mắc các loại khối u rắn đang phát triển.
Khi xảy ra tình trạng quá liều, nên áp dụng các biện pháp can thiệp triệu chứng và hỗ trợ bổ sung. Hiện không có phương pháp trị liệu cụ thể cho việc quá liều crizotinib.
Dựa trên các nghiên cứu trong phòng thí nghiệm và trên động vật, crizotinib được xác định có khả năng gây độc cho gen, nhưng thử nghiệm Ames cho thấy nó không gây biến dị.
Chưa có nghiên cứu chính thức về mối liên giữa crizotinib và nguy cơ mắc bệnh ung thư.
Tính an toàn
Không có thông tin về việc sử dụng lâm sàng crizotinib trong thời gian cho con bú. Vì crizotinib liên kết 91% với protein huyết tương nên lượng trong sữa có thể thấp. Tuy nhiên, thời gian bán hủy của nó là khoảng 42 giờ và nó có thể tích lũy ở trẻ sơ sinh. Nhà sản xuất khuyến cáo nên ngừng cho con bú trong khi điều trị bằng crizotinib và trong 45 ngày sau liều cuối cùng.
Tương tác với thuốc khác
Thuốc ức chế CYP3A4: Vì crizotinib chủ yếu được chuyển hóa bởi CYP3A4 trong gan, việc sử dụng cùng lúc với các thuốc ức chế CYP3A4 mạnh (như ketoconazole, itraconazole, clarithromycin, ritonavir, vv.) có thể làm tăng nồng độ của crizotinib trong huyết tương và tăng nguy cơ gặp phản ứng không mong muốn.
Thuốc kích thích CYP3A4: Thuốc kích thích CYP3A4 (như rifampin, phenytoin, carbamazepine, vv.) có thể giảm nồng độ của crizotinib và giảm hiệu quả của nó.
Thuốc ức chế và kích thích CYP2C8: Việc sử dụng chung với các thuốc ức chế hoặc kích thích CYP2C8 có thể ảnh hưởng đến nồng độ của crizotinib.
Thuốc kéo dài khoảng QT: Crizotinib có thể tạo ra giai đoạn QT dài trên điện tâm đồ, do đó sử dụng đồng thời với các thuốc khác cũng có khả năng kéo dài giai đoạn QT (như quinidine, procainamide, amiodarone, sotalol) có thể tăng nguy cơ gặp các bất thường về nhịp tim.
Thuốc có khả năng gây tác động trên dạ dày: Crizotinib nên được dùng cùng với thức ăn để tăng cường hấp thu. Do đó, việc sử dụng chung với các thuốc ảnh hưởng đến độ acid của dạ dày, như thuốc chống axit hoặc thuốc ức chế proton, có thể ảnh hưởng đến hấp thu crizotinib.
Lưu ý khi sử dụng Crizotinib
Giống như nhiều thuốc khác, Crizotinib cũng có thể gây ra các tác dụng phụ. Các tác dụng phụ thường gặp bao gồm tiêu chảy, buồn nôn, nổi mẩn, và giảm tiết nước bọt. Nếu bạn gặp các tác dụng phụ nghiêm trọng như rối loạn thị giác, tăng cân nhanh, hay khó thở, bạn cần liên hệ với bác sĩ ngay lập tức.
Crizotinib có thể tương tác với một số thuốc khác, đặc biệt là các thuốc ức chế hoặc kích thích CYP3A4. Hãy thông báo cho bác sĩ về tất cả các thuốc, thảo dược, và bổ sung dinh dưỡng bạn đang sử dụng.
Trong quá trình điều trị, bạn nên thường xuyên theo dõi các chỉ số sức khỏe như chức năng gan, thận và huyết áp. Điều này giúp đảm bảo an toàn khi sử dụng crizotinib.
Crizotinib có thể gây kéo dài khoảng QT dài trên điện tâm đồ, làm tăng nguy cơ các vấn đề nhịp tim. Tránh sử dụng cùng lúc với các thuốc có khả năng kéo dài khoảng QT.
Nên dùng Crizotinib cùng với thức ăn để tăng cường hấp thu.
Nếu bạn đang mang thai, dự định mang thai, hoặc đang cho con bú, hãy thảo luận với bác sĩ trước khi sử dụng Crizotinib.
Hạn chế lái xe hoặc tham gia các hoạt động đòi hỏi sự tập trung cao cho đến khi biết được cơ thể phản ứng với thuốc như thế nào.
Một vài nghiên cứu của Crizotinib trong Y học
Ảnh hưởng của alectinib so với crizotinib đối với khả năng sống sót không tiến triển, hiệu quả của hệ thần kinh trung ương và các tác dụng phụ trong ung thư phổi không phải tế bào nhỏ dương tính với ALK
Cơ sở: Ung thư phổi là khối u ác tính phổ biến nhất và nó vẫn là nguyên nhân chính gây tử vong liên quan đến ung thư trên toàn thế giới. Ung thư phổi tế bào không nhỏ (NSCLC) tái sắp xếp gen tổng hợp tế bào lympho kinase phân hóa (ALK dương tính) là một phân nhóm duy nhất chiếm 3-7% các trường hợp NSCLC.
Trong vài năm qua, việc giới thiệu một số chất ức chế ALK đã thay đổi hoàn toàn việc điều trị NSCLC dương tính với ALK tiên tiến và cải thiện đáng kể tiên lượng cho bệnh nhân.
Crizotinib là chất ức chế ALK đầu tiên được phát triển và nó đã chứng minh hiệu quả toàn thân và kết quả cải thiện mạnh mẽ ở bệnh nhân NSCLC dương tính với ALK khi so sánh với hóa trị liệu.
Alectinib được thiết kế đặc biệt để trở thành một tác nhân trị liệu chống ALK mạnh hơn và chọn lọc hơn, có thể vượt qua tình trạng kháng crizotinib.
Phương pháp: Chúng tôi đã tìm kiếm tài liệu liên quan trong bốn cơ sở dữ liệu điện tử: PubMed, EMBASE, Thư viện Cochrane và Web of Science. Tỷ lệ rủi ro (HR) đã được tính toán và tác động của alectinib và crizotinib đối với PFS đã được đánh giá.
Chất lượng của các nghiên cứu được đánh giá bằng công cụ Cochrane Risk of Bias. Xu hướng xuất bản được đánh giá bằng cách sử dụng bài kiểm tra tương quan xếp hạng Begg và bài kiểm tra hồi quy tuyến tính có trọng số Egger. Chúng tôi đã thực hiện phân tích độ nhạy bằng phương pháp “loại bỏ một nghiên cứu”. Tất cả các phân tích đã được thực hiện trong STATA.
Kết quả: Mười nghiên cứu đã được đưa vào và tổng cỡ mẫu là 2.377. Alectinib cho thấy sự vượt trội đáng kể về PFS so với crizotinib. HR gộp = 0,41 (KTC 95%: 0,29-0,53) chỉ ra rằng nhóm điều trị bằng alectinib có PFS dài hơn đáng kể so với nhóm điều trị bằng crizotinib.
Dựa trên 5 thử nghiệm lâm sàng, tỷ lệ tích lũy tiến triển CNS đối với bệnh nhân được điều trị bằng alectinib sau 6 tháng (10%, KTC 95%: 5-16%) và 12 tháng (16%, KTC 95%: 9-24%) đã được tính toán.
Dựa trên 7 nghiên cứu lâm sàng, nguy cơ AE liên quan đến điều trị bằng alectinib đã được xác định: alectinib có liên quan đến 28 trường hợp AE cấp độ ≤2 và 9 trường hợp cấp độ AE ≥3; trong số 4 trường hợp mắc AE cấp độ ≥3, là creatine phosphokinase trong máu tăng 5,6%, ALT tăng 2,5%, AST tăng 2,4% và Thiếu máu 1,8%.
Kết luận: Alectinib kéo dài đáng kể PFS và nó kiểm soát di căn CNS tốt hơn so với crizotinib và các đặc tính độc tính tốt trong điều trị đầu tay cho bệnh nhân NSCLC dương tính với ALK.
Tài liệu tham khảo
- Drugbank, Crizotinib, truy cập ngày 10 tháng 8 năm 2023.
- Pubchem, Crizotinib, truy cập ngày 10 tháng 8 năm 2023.
- Yang YL, Xiang ZJ, Yang JH, Wang WJ, Xiang RL. Effect of alectinib versus crizotinib on progression-free survival, central nervous system efficacy and adverse events in ALK-positive non-small cell lung cancer: a systematic review and meta-analysis. Ann Palliat Med. 2020 Jul;9(4):1782-1796. doi: 10.21037/apm-19-643. Epub 2020 Jun 8. PMID: 32527124.
- Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội
