Bimatoprost
Biên soạn và Hiệu đính
Dược sĩ Phan Hữu Xuân Hạo – Khoa Dược, Trường Y Dược – Đại học Duy Tân.
Danh pháp
Tên chung quốc tế
Bimatoprost ophthalmic solution
Tên danh pháp theo IUPAC
( Z ) -7 – [(1 R , 2 R , 3 R , 5 S ) -3,5-dihydroxy-2 – [( E , 3 S ) -3-hydroxy-5-phenylpent-1-enyl] cyclopentyl ] – N -etylhept-5-men
Nhóm thuốc
Thuốc có tác dụng hạ nhãn áp
Mã ATC
S01EE03
S: Thuốc dùng cho các giác quan
S01:Thuốc dùng cho mắt
S01E:Thuốc dùng điều trị Glaucoma và co đồng tử
S01EE: Các thuốc có bản chất tương tự Prostaglandin
S01EE03: Bimatoprost (Bimatoprost )
Mã UNII
QXS94885MZ
Mã CAS
155206-00-1
Phân loại cho phụ nữ có thai của Bimatoprost
Phân loại thai kỳ ( theo FDA): loại C
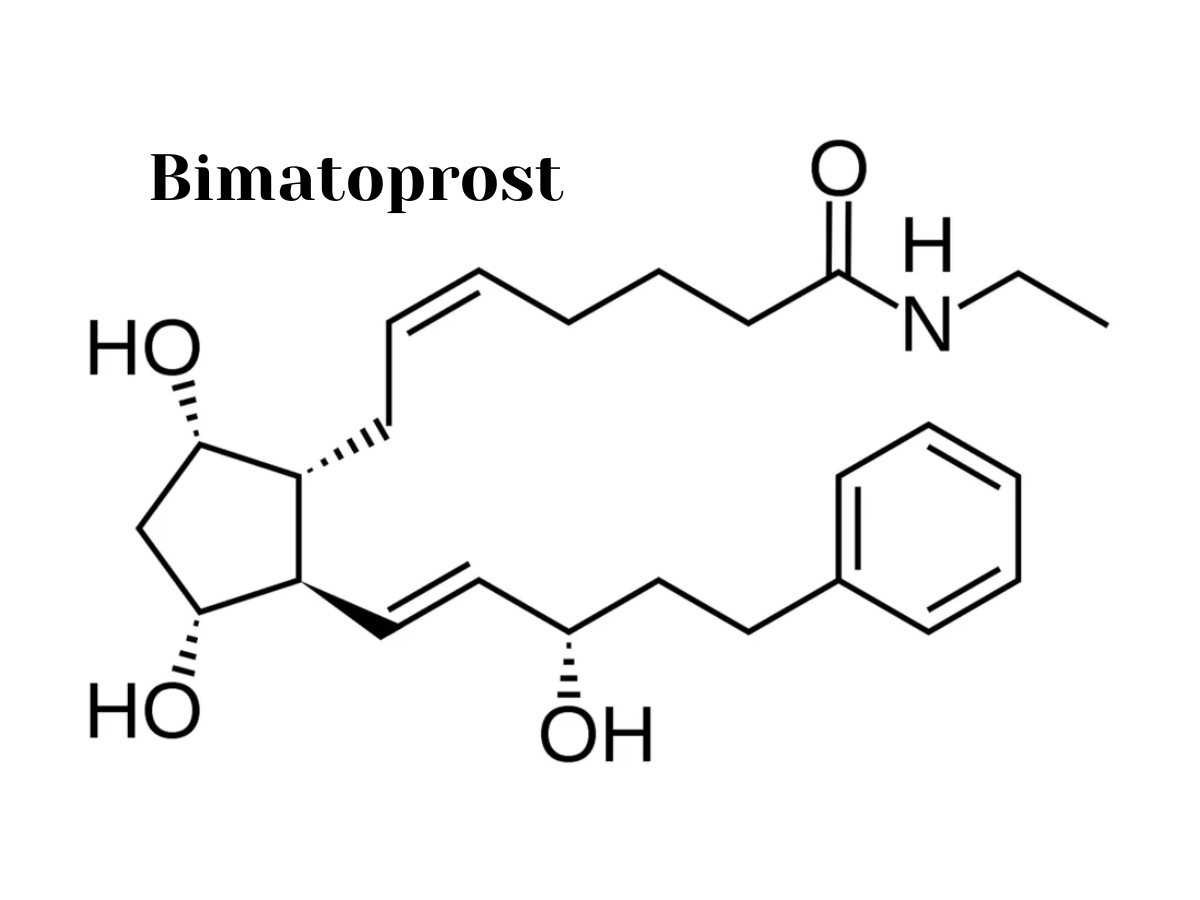
Cấu trúc phân tử
Công thức phân tử
C25H37NO4
Phân tử lượng
415,6 g/mol
Cấu trúc phân tử
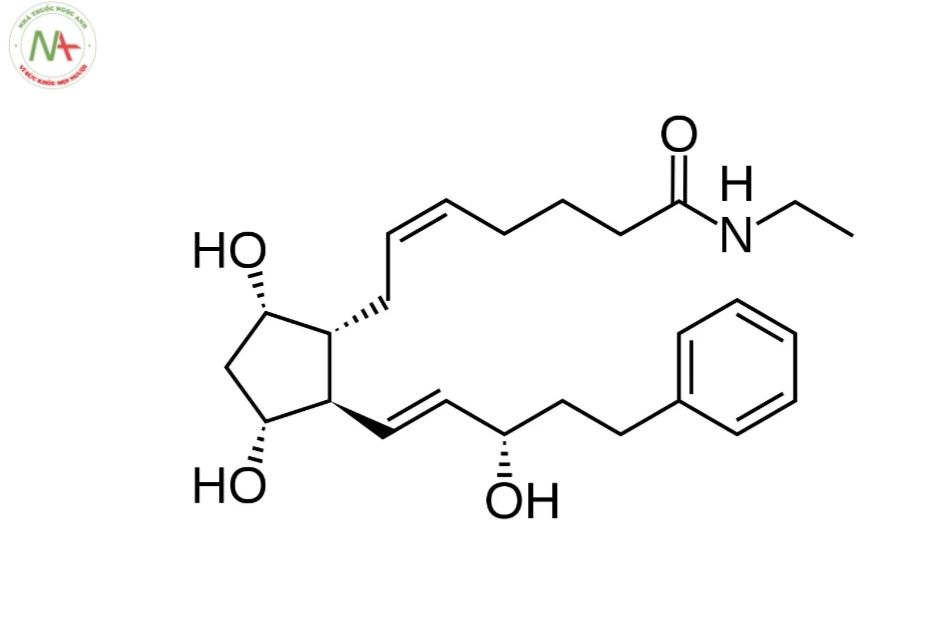
Các tính chất phân tử
Số liên kết hydro cho: 4
Số liên kết hydro nhận: 4
Số liên kết có thể xoay: 12
Diện tích bề mặt tôpô: 89.8 Ų
Số lượng nguyên tử nặng: 30
Phần trăm các nguyên tử: C 72.26%, H 8.97%, N 3.37%, O 15.40%
Các tính chất đặc trưng
Điểm nóng chảy (° C): 66-68 ℃
Điểm sôi (° C): 629,8 ℃ ở 760 mmHg
Chỉ số khúc xạ: 1.591
Áp suất hơi: 0,0 mmHg ở 25 ° C
LogP: 3.53780
Độ hòa tan trong nước: 1,87e-02 g / L
Hằng số phân ly (pKa): 14.3, – 0.23
Chu kì bán hủy: khoảng 45 phút
Cảm quan
Bimatoprost có dạng bột rắn màu trắng đến trắng nhạt.
Bimatoprost tan được trong nước. Tan tốt trong Chloroform, tan một ít trong Dichloromethane và Methanol.
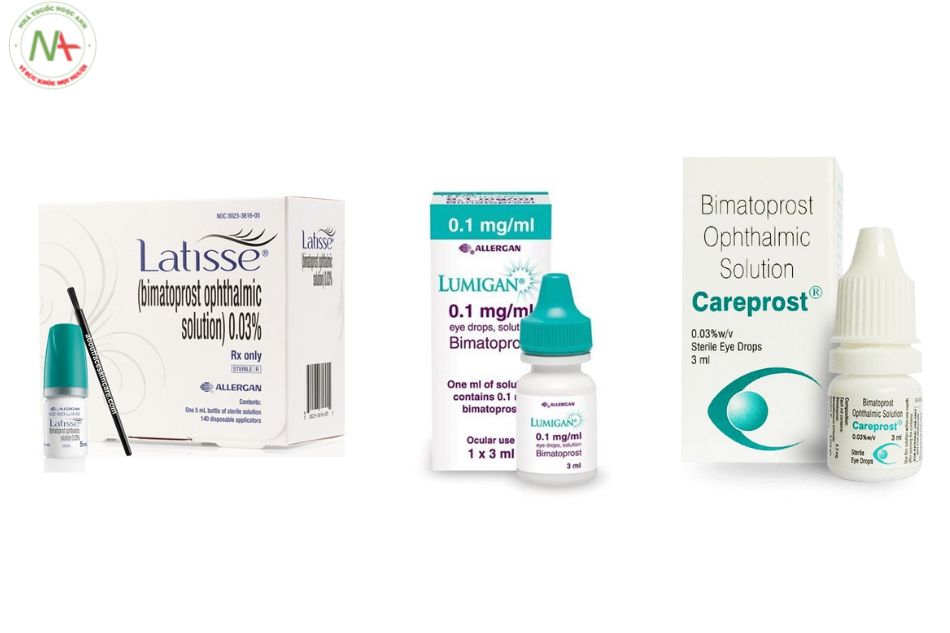
Dạng bào chế
Bimatoprost có dạng que cấy giác mạc với hàm lượng 10 mcg
Bimatoprost có dạng dung dịch nhỏ mắt dung tích 0,1 mg/ml; 0,3 mg/ml
Và dung dịch nhỏ mắt phối hợp dung tích 0,3 mg/ml và timolol – 5 mg/ml.
Độ ổn định và điều kiện bảo quản của Bimatoprost
Bảo quản Bimatoprost ở điều kiện thường (15-30oC).
Tránh để Bimatoprost ở nơi ẩm ướt, tránh ánh sáng trực tiếp từ mặt trời.
Để Bimatoprost xa tầm tay trẻ em.
Nguồn gốc
Bimatoprost , còn được gọi là Bimatoprost hoặc Lumigan, thuộc về một nhóm thuốc được gọi là prostamide, là chất tương tự cấu trúc tổng hợp của prostaglandin. Bimatoprost , do Allergan tiếp thị, được sử dụng ở cả dạng dung dịch nhỏ mắt và dạng cấy ghép. Nó có khả năng làm giảm chứng hạ huyết áp ở mắt, chứng tỏ hiệu quả trong các tình trạng như tăng huyết áp ở mắt và bệnh tăng nhãn áp. Bimatoprost cũng được sử dụng để điều trị chứng rụng lông mi, hoặc lông mi mọc thưa thớt.
Ban đầu, Bimatoprost đã được FDA phê duyệt để sử dụng trong y tế tại Hoa Kỳ vào năm 2001 cho chứng tăng nhãn áp.
Sau đó, Bimatoprost được chấp thuận cho chứng loạn mi vào năm 2008, vì sự phát triển của lông mi trở thành một tác dụng phụ mong muốn đối với những bệnh nhân sử dụng thuốc này.
Năm 2018, Bimatoprost là loại thuốc được kê đơn phổ biến thứ 274 ở Hoa Kỳ, với hơn 2 triệu đơn thuốc.
Dược lý và cơ chế hoạt động
Nhãn áp cao là một yếu tố nguy cơ chính gây mất thị trường liên quan đến bệnh tăng nhãn áp. Một mối quan hệ tuyến tính tồn tại giữa nhãn áp và nguy cơ làm tổn thương dây thần kinh thị giác, có thể dẫn đến suy giảm thị lực đáng kể. Do đó, các tình trạng như tăng nhãn áp và tăng nhãn áp có thể gây ra tăng nhãn áp nguy hiểm.
Bimatoprost là một prostamide – một chất tổng hợp có cấu trúc tương tự như prostaglandin. Bimatoprost có tác dụng làm hạ nhãn áp ở người bằng cách làm tăng thoát thuỷ dịch qua vùng bè và màng mạch – củng mạc. Tăng áp suất nội nhãn là nguy cơ chính gây ra mất thị trường. Do đó, Bimatoprost có khả năng làm giảm nguy cơ mất thị trường từ nhiều nguyên nhân khác nhau.
Các tác dụng khác của thuốc này có thể bao gồm thay đổi dần dần sắc tố mí mắt, thay đổi sắc tố mống mắt, thay đổi sắc tố lông mi, tăng trưởng và độ dày. Bệnh nhân nên được thông báo về những tác dụng có thể xảy ra này, đặc biệt nếu thuốc này chỉ được sử dụng cho một mắt, có thể thay đổi rõ rệt về hình thức khi điều trị bằng chất quang học.
Bimatoprost sao chép lại tác dụng của các prostamit, cụ thể là prostaglandin F2α. Bimatoprost kích thích nhẹ sự chảy ra của thủy dịch, làm giảm áp lực nội nhãn tăng cao và giảm nguy cơ tổn thương dây thần kinh thị giác.
Người ta cho rằng Bimatoprost làm giảm áp lực nội nhãn (IOP) ở người bằng cách gây ra sự gia tăng dòng chảy của thủy dịch thông qua các đường lưới trabecular và các đường dẫn truyền qua màng bồ đào. Nó đạt được các hiệu ứng trên bằng cách giảm khả năng chống tonographic đối với sự chảy ra của dung dịch nước.
Bimatoprost không ảnh hưởng đến quá trình sản xuất thủy dịch.
Ứng dụng trong y học của Bimatoprost
Bimatoprost được sử dụng để giảm nhãn áp tăng cao ở những bệnh nhân bị tăng nhãn áp góc mở hoặc tăng huyết áp ở mắt. Những bệnh nhân này được chỉ định dùng Bimatoprost khi không dung nạp với các thuốc hạ nhãn áp khác hoặc không đáp ứng tốt với các phương pháp điều trị khác.
Bimatoprost cũng được chỉ định để điều trị chứng rụng lông mi. Hiện tại, trên thị trường thuốc Bimatoprost đã được FDA Hoa Kỳ chấp nhận trong điều trị cho các trường hợp lông mi bị thưa. Bimatoprost có khả năng làm hàng lông mi phía trên phát triển, mọc dài hơn, dày hơn và sẫm màu hơn. Để đạt hiệu quả, người bệnh cần sử dụng thuốc Bimatoprost hằng ngày trong ít nhất 2 tháng. Miễn là người bệnh vẫn đang sử dụng các thuốc dưỡng lông mi thì sự cải thiện của lông mi sẽ vẫn được tiếp tục. Đến khi ngừng sử dụng Bimatoprost , lông mi sẽ trở lại như bình thường
Dược động học
Hấp thu
Bimatoprost có khả năng thâm nhập tốt vào giác mạc và màng cứng mắt của người. Sau khi nhỏ 0,3 mg/ml (tương đương 1 giọt) Bimatoprost x 1 lần/ngày cho hai mắt trong vòng hai tuần, nồng độ thuốc trong máu đo được đạt đỉnh trong vòng 10 phút sau khi dùng thuốc và giảm xuống dưới giới hạn phát hiện dưới ( khoảng 0,025 mg/ml) trong vòng 1,5 giờ.
Nồng độ Bimatoprost đạt ổn định ngay trong tuần đầu tiên dùng thuốc nhỏ mắt.
Phân bố
Bimatoprost phân bố trung bình vào các mô cơ thể. Thể tích phân bố khắp cơ thể ở trạng thái ổn định là 0,67 L/kg.
Khoảng 88% Bimatoprost liên kết với protein huyết tương.
Chuyển hóa
Bimatoprost là là hoạt chất lưu thông chính trong máu khi nó đến được hệ tuần hoàn sau khi dùng thuốc nhỏ mắt. Bimatoprost sau đó được trải qua quá trình oxy hóa, glucuronid hóa và N-deetyl hóa để tạo thành nhiều loại chất chuyển hóa khác nhau.
Thải trừ
Bimatoprost được thải trừ chủ yếu qua qua thận, chiếm 67% liều tiêm tĩnh mạch. Khoảng 25% liều dùng Bimatoprost được thải trừ qua phân.
Thời gian bán hủy của Bimatoprost được xác định sau khi tiêm tĩnh mạch là vào khoảng 45 phút.
Tổng độ thanh thải trong máu là khoảng 1,5 L/giờ/kg.
Độc tính của Bimatoprost
Chưa có báo cáo về độc tính khi dùng quá liều Bimatoprost ở người.
Lưu ý và thận trọng khi dùng Bimatoprost
Lưu ý và thận trọng chung
Trên mắt
Bimatoprost có khả năng kích thích mọc lông mi, sạm da mí mắt và tăng sắc tố trên mống mắt. Khả năng tăng sắc tố trên mống mắt có khả năng sẽ tồn tại vĩnh viễn. Sự thay đổi sắc tố của cơ thể là do tăng hàm lượng melamine trong tế bào sắc tố. Tuy nhiên, tăng sắc tố mô xung quanh mắt có thể hồi phục ở một số bệnh nhân.
Ở những bệnh nhân dùng Bimatoprost 0,3 mg/ml có thể sẽ mắc phù hoàng điểm dạng nang. Do đó, nên sử dụng Bimatoprost một cách thận trọng cho những bệnh nhân có nguy cơ mắc phù hoàng điểm (như bệnh nhân sử dụng thủy tinh thể giả có bao sau bị vỡ hay bệnh nhân không có thủy tinh thể tự nhiên…).
Thận trọng khi sử dụng Bimatoprost 0,3 mg/ml cho bệnh nhân có tiền sử bị nhiễm virus ở mắt (như herpes simplex) hoặc viêm màng bồ đào hay viêm mống mắt vì nguy cơ thâm nhiễm giác mạc hoặc nhiễm trùng mắt.
Trên da
Ở những vùng da mà dung dịch Bimatoprost tiếp xúc nhiều lần có thẻ làm tăng khả năng lông mọc. Vì vậy, tránh để Bimatoprost chảy lên má hoặc các vùng da lân cận khác.
Trên hô hấp
Bimatoprost có khả năng gây ra đợt cấp của cơn hen suyễn, khó thở và bệnh phổi tắc nghẽn mạn tính (COPD). Bệnh nhân COPD, hen suyễn hoặc chức năng hô hấp bị tổn thương do các bệnh lý khác nên được điều trị thận trọng.
Trên tim mạch
Bimatoprost nồng độ 0,3 mg/ ml có thể gây chậm nhịp tim hoặc gây hạ huyết áp. Vì vậy phải sử dụng thật thận trọng Bimatoprost cho những bệnh nhân dễ bị nhịp tim chậm hoặc huyết áp thấp.
Chất bảo quản Benzalkonium chloride
Thuốc nhỏ mắt Bimatoprost t thường chứa chất bảo quản benzalkonium chloride. Chất này có thể làm đổi màu kính áp tròng. Ngoài ra, benzalkonium chloride cũng có thể gây kích ứng mắt cũng như viêm giác mạc chấm nông và viêm loét giác mạc nhiễm độc nên cần theo dõi chặt chẽ khi sử dụng Bimatoprost thường xuyên hoặc kéo dài ở các bệnh nhân bị khô mắt hoặc giác mạc bị tổn thương.
Nếu bệnh nhân có dùng kính áp tròng thì bệnh nhân nên tháo kính áp tròng mềm trước khi nhỏ thuốc và đợi sau 15 phút sử dụng mới được đeo vào.
Bệnh nhân cần tránh để đầu của chai thuốc tiếp xúc với mắt hoặc các cấu trúc xung quanh khi nhỏ mắt để ngăn chặn nguy cơ bị nhiễm bẩn dung dịch dẫn đến nhiễm trùng mắt.
Lưu ý dùng Bimatoprost cho phụ nữ đang mang thai
Không khuyến cáo sử dụng Bimatoprost cho phụ nữ đang mang thai trừ khi thật cần thiết hoặc bắt buộc phải sử dụng.
Lưu ý dùng Bimatoprost cho phụ nữ đang cho con bú
Không khuyến cáo sử dụng Bimatoprost cho phụ nữ đang cho con bú. Nếu trường hợp bắt buộc phải sử dụng, nên cân nhắc ngưng cho con bú hoặc đổi sang thuốc khác.
Lưu ý khi dùng Bimatoprost cho người lái xe hoặc vận hành máy móc
Bimatoprost ảnh hưởng không đáng kể đến khả năng lái xe hay vận hành máy móc.
Tuy nhiên, như dùng các thuốc nhỏ mắt khác, khi dùng Bimatoprost có thể gây mờ mắt nhẹ. Vì thế, bệnh nhân khi đã sử dụng Bimatoprost nên đợi cho đến khi thị lực khôi phục bình thường trước khi lái xe hay vận hành máy móc.
Tương tác với thuốc khác
Sử dụng đồng thời Bimatoprost với các chất tương tự prostaglandin khác có thể làm giảm hiệu quả hạ nhãn áp của thuốc Bimatoprost .
Tương tác với các loại thuốc dùng cho toàn thân (ví dụ như đường uống) được xem là không thể xảy ra vì chất phản ứng sinh học không đạt được nồng độ tương ứng trong máu.
Ngoài ra, vẫn chưa có thông tin về tương tác với các thuốc khác khi dùng chung với Bimatoprost .
Một vài nghiên cứu của Bimatoprost trong Y học
Thử nghiệm lâm sàng giai đoạn I / II trong 24 tháng về Cấy ghép phát hành bền vững Bimatoprost (Bimatoprost SR) ở bệnh nhân tăng nhãn áp
Mục tiêu
Mục tiêu của nghiên cứu này là đánh giá tính an toàn và tác dụng làm chậm nhãn áp (IOP) trong 24 tháng của cấy ghép giải phóng bền vững sinh học phân hủy sinh học (Bimatoprost SR) so với sử dụng Bimatoprost tại chỗ 0,03% ở những bệnh nhân bị bệnh tăng nhãn áp góc mở (OAG ).
Phương pháp
Đây là một thử nghiệm lâm sàng đối chứng bằng mắt có đối chứng ở giai đoạn I / II, tương lai, kéo dài 24 tháng, theo liều lượng, có đối chứng. Tại thời điểm ban đầu sau khi rửa trôi, bệnh nhân người lớn mắc bệnh OAG (N = 75) được tiêm Bimatoprost SR (6, 10, 15, hoặc 20 µg) trong mắt nghiên cứu; mắt của đồng nghiệp được tiêm Bimatoprost 0,03% tại chỗ một lần mỗi ngày. Cho phép dùng thuốc làm giảm IOP tại chỗ hoặc dùng lặp lại một lần với thiết bị cấy ghép. Điểm cuối chính là thay đổi IOP so với ban đầu. Các biện pháp an toàn bao gồm các sự kiện bất lợi (AE).
Kết quả
Vào tháng thứ 24, mức giảm IOP trung bình so với ban đầu là 7,5, 7,3, 7,3 và 8,9 mmHg ở mắt được điều trị bằng Bimatoprost SR 6, 10, 15 và 20 µg, so với 8,2 mmHg ở mắt đồng bộ; 68, 40 và 28% mắt nghiên cứu gộp đã không được cứu sống / rút lui lần lượt ở các tháng 6, 12 và 24. AE trong mắt nghiên cứu xảy ra ≤ 2 ngày sau thủ thuật thường là thoáng qua. Sau 2 ngày sau thủ thuật, tỷ lệ mắc AE tổng thể là tương tự giữa các mắt nghiên cứu và đồng nghiệp, với một số biến cố thường liên quan đến các chất tương tự prostaglandin tại chỗ có tỷ lệ mắc bệnh thấp hơn ở mắt nghiên cứu.
Kết luận
Bimatoprost SR cho thấy hiệu quả thuận lợi và hồ sơ an toàn lên đến 24 tháng, với tất cả các cường độ liều được đánh giá đều cho thấy tác dụng giảm IOP tổng thể tương đương với tác dụng của Bimatoprost tại chỗ. Phân phối có mục tiêu và liên tục của chất dẻo sinh học dẫn đến giảm IOP kéo dài, cho thấy rằng Bimatoprost SR có thể đại diện cho một cách tiếp cận mới mang tính chuyển đổi đối với liệu pháp điều trị bệnh tăng nhãn áp.
Tài liệu tham khảo
- 1. Drugbank, Bimatoprost , truy cập ngày 14 tháng 8 năm 2022.
- 2. Pubchem, Bimatoprost , truy cập ngày 14 tháng 8 năm 2022.
- 3. Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội
- 4. Craven, E. R., Walters, T., Christie, W. C., Day, D. G., Lewis, R. A., Goodkin, M. L., … & Bejanian, M. (2020). 24-month phase I/II clinical trial of Bimatoprost sustained-release implant (Bimatoprost SR) in glaucoma patients. Drugs, 80(2), 167-179.
Xuất xứ: Pháp
Xuất xứ: Ireland
Xuất xứ: Ireland
Xuất xứ: Ba Lan