Baloxavir Marboxil
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
[(3R)-2-[(11S)-7,8-difluoro-6,11-dihydrobenzo[c][1]benzothiepin-11-yl]-9,12-dioxo-5-oxa-1,2,8-triazatricyclo[8.4.0.03,8]tetradeca-10,13-dien-11-yl]oxymethyl methyl carbonate
Nhóm thuốc
Thuốc kháng virus
Mã ATC
J – Thuốc chống nhiễm trùng dùng toàn thân
J05 – Thuốc kháng virus dùng toàn thân
J05A – Thuốc kháng vi-rút tác động trực tiếp
J05AX – Thuốc kháng virus khác
J05AX25 – Baloxavir marboxil
Mã UNII
505CXM6OHG
Mã CAS
1985606-14-1
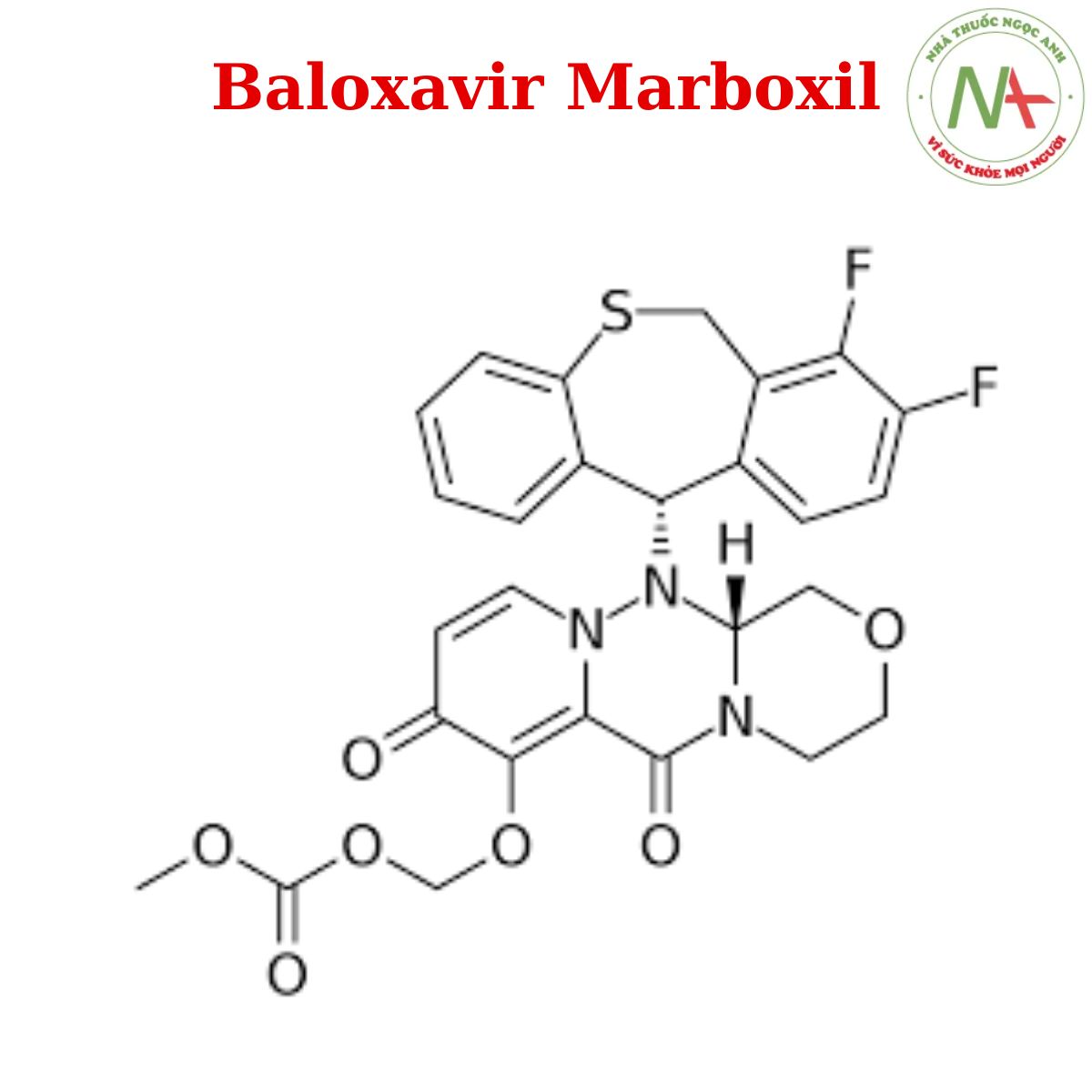
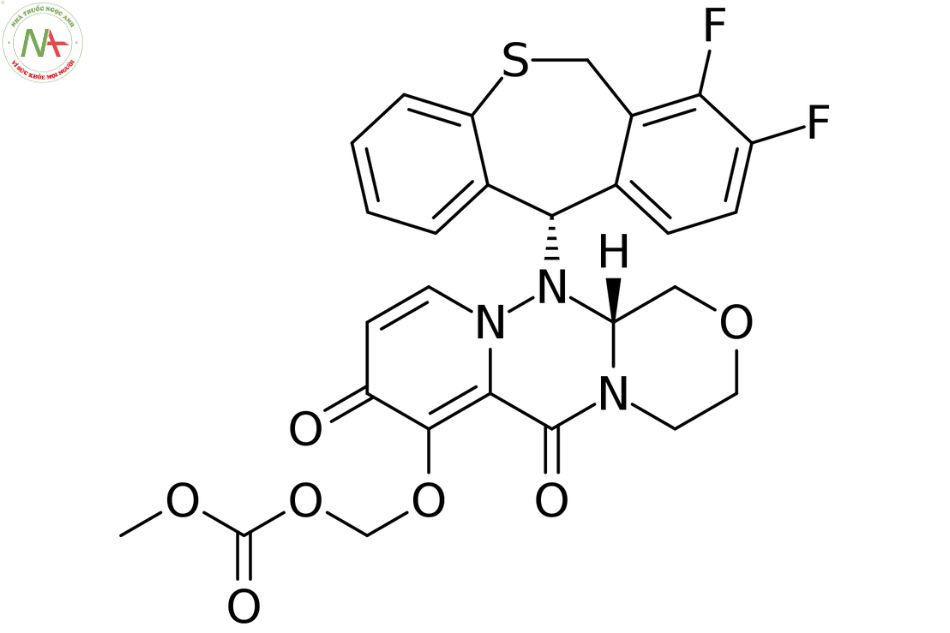
Cấu trúc phân tử
Công thức phân tử
C27H23F2N3O7S
Phân tử lượng
571.6 g/mol
Cấu trúc phân tử
Baloxavir marboxil là một dẫn xuất pyridone thay thế của một nhóm cấu trúc đa vòng
Các tính chất phân tử
Số liên kết hydro cho: 0
Số liên kết hydro nhận: 12
Số liên kết có thể xoay: 6
Diện tích bề mặt tôpô: 123Ų
Số lượng nguyên tử nặng: 40
Các tính chất đặc trưng
Điểm sôi: 712.8±70.0 °C ở 760 mmHg
Tỷ trọng riêng: 1.6±0.1 g/cm3
Độ tan trong nước: 0.015mg/mL
Hằng số phân ly pKa: -0.6
Chu kì bán hủy: 79,1 giờ
Khả năng liên kết với Protein huyết tương: 92,9–93,9%
Dạng bào chế
Viên nén: 20 mg, 40 mg, 80 mg
Hỗn dịch: 2 mg/ml
Độ ổn định và điều kiện bảo quản
Baloxavir marboxil là một loại thuốc khá ổn định trong điều kiện bình thường và được sản xuất theo quy trình chất lượng cao. Như với bất kỳ loại thuốc nào, baloxavir marboxil cần được bảo quản đúng cách để đảm bảo độ ổn định và hiệu quả của nó. Theo hướng dẫn của nhà sản xuất, baloxavir marboxil nên được bảo quản ở nhiệt độ phòng, trong điều kiện khô ráo và tránh ánh sáng mặt trời trực tiếp.
Nguồn gốc
Baloxavir marboxil là một loại thuốc chống cúm được phát triển bởi công ty dược phẩm Shionogi & Co., Ltd., có trụ sở tại Nhật Bản. Nghiên cứu và phát triển baloxavir marboxil đã được tiến hành trong một quá trình hợp tác giữa Shionogi và công ty dược phẩm Roche.
Baloxavir marboxil được phát hiện dựa trên việc nghiên cứu cấu trúc và hoạt tính của virus cúm. Nó hoạt động bằng cách ức chế hoạt động của endonucleaza flu, một enzym chủ chốt trong chu kỳ sao chép của virus cúm. Bằng cách ngăn chặn hoạt động của enzym này, baloxavir marboxil làm giảm khả năng virus cúm sao chép và lây lan trong cơ thể.
Sau khi hoàn thành các thử nghiệm và nghiên cứu lâm sàng, baloxavir marboxil đã được phê duyệt và được tiếp thị dưới tên thương mại là Xofluza. Nó đã được chấp thuận sử dụng cho điều trị cúm A và B ở một số quốc gia trên thế giới, bao gồm cả Hoa Kỳ, Nhật Bản và nhiều quốc gia châu Âu.
Dược lý và cơ chế hoạt động
Baloxavir marboxil là một loại thuốc kháng vi-rút được thiết kế để chống lại sự nhân lên của vi-rút cúm. Nó có tác dụng chủ động đối với các vi-rút cúm A và cúm B bằng cách ức chế hoạt động của một enzym gọi là endonuclease axit polymerase (PA). Các nghiên cứu đã chỉ ra rằng baloxavir marboxil có nồng độ ức chế 50% (IC50) từ 1,4 đến 3,1 nM đối với vi-rút cúm A và từ 4,5 đến 8,9 nM đối với vi-rút cúm B trong xét nghiệm endonuclease.
Trong các thí nghiệm trên chuột và gia cầm cúm A, baloxavir đã được chứng minh là có khả năng làm giảm tải lượng vi-rút trong phổi và tăng tỷ lệ sống sót của chuột. Sự giảm hiệu giá vi-rút được quan sát trong khoảng 24 giờ sau khi sử dụng thuốc, và hiệu quả này phụ thuộc vào liều lượng được sử dụng.
Vi-rút cúm có một phức hợp enzym gọi là RNA polymerase, bao gồm ba tiểu đơn vị protein: protein cơ bản polymerase 1 (PB1), protein cơ bản polymerase 2 (PB2) và protein axit polymerase (PA). Phức hợp polymerase này là một enzym quan trọng cho quá trình sao chép và phiên mã gen của vi-rút. Các tiểu đơn vị trong phức hợp này có vai trò khác nhau trong quá trình tổng hợp mRNA của vi-rút.
Tiểu đơn vị PB2 liên kết với mảnh tin RNA tiền truyền tin của tế bào chủ, cho phép tiểu đơn vị PA (một endonuclease phụ thuộc vào mảnh tin) tách mảnh tin có nắp của RNA tiền truyền tin. Bước này, gọi là “quá trình giật nắp”, cung cấp một mẩu RNA mồi cho tiểu đơn vị PB1, tiểu đơn vị này có chức năng RNA polymerase để tổng hợp mRNA của vi-rút.
Sau khi được dùng, baloxavir marboxil gần như hoàn toàn bị chuyển hóa bởi các esterase trong dạ dày, ruột, gan và máu thành một chất chuyển hóa hoạt động được gọi là baloxavir. Baloxavir có khả năng ức chế chọn lọc protein PA, ngăn chặn quá trình khởi đầu tổng hợp mRNA và cuối cùng là sự phát triển của vi-rút cúm.
Endonuclease phụ thuộc vào mảnh tin là một khu vực có tính chất bảo tồn cao trong các chủng cúm. Tuy nhiên, vi-rút có thể phát triển kháng thuốc với baloxavir do sự thay thế các axit amin trong protein PA có thể làm giảm tính nhạy cảm của vi-rút đối với baloxavir.
Ứng dụng trong y học
Baloxavir marboxil (hay còn được biết đến với tên thương mại Xofluza) là một loại thuốc có ứng dụng quan trọng trong lĩnh vực y học, đặc biệt là trong việc điều trị cúm. Đây là một tiến bộ đáng chú ý trong việc kiểm soát và ứng phó với cúm, một bệnh truyền nhiễm phổ biến và có thể gây ra tác động nghiêm trọng đến sức khỏe cộng đồng.
Baloxavir marboxil hoạt động bằng cách ức chế một enzym quan trọng trong chu kỳ sao chép của virus cúm, gọi là endonucleaza flu. Điều này ngăn chặn khả năng sao chép và phát triển của virus trong cơ thể. Một điểm mạnh của baloxavir marboxil so với các loại thuốc chống cúm khác là khả năng hoạt động nhanh chóng và hiệu quả sau một liều duy nhất. Điều này giúp giảm nguy cơ lây nhiễm và giảm thời gian mắc bệnh.
Ứng dụng của baloxavir marboxil trong y học là đặc biệt quan trọng trong các trường hợp cúm A và B, đặc biệt là trong những trường hợp mắc cúm sớm và cần điều trị sớm. Bằng cách khống chế virus cúm, baloxavir marboxil giúp giảm triệu chứng và thời gian bệnh, đồng thời ngăn chặn sự lây lan của virus từ người này sang người khác.
Một ứng dụng tiềm năng khác của baloxavir marboxil là trong việc phòng ngừa cúm. Nghiên cứu đã chỉ ra rằng việc sử dụng baloxavir marboxil như một biện pháp phòng ngừa sau tiếp xúc với người mắc cúm có thể giúp ngăn chặn sự lây lan của virus trong cộng đồng. Điều này có thể đóng vai trò quan trọng trong việc kiểm soát đợt bùng phát cúm và giảm tác động xã hội và kinh tế của nó.
Dược động học
Hấp thu
Sau khi được uống 40 mg baloxavir marboxil ở thanh thiếu niên và người lớn từ 12 tuổi trở lên, AUC (diện tích dưới đường cong) đạt 5520 ng x giờ/mL và Cmax (nồng độ đỉnh) đạt 68,9 ng/mL. Khi sử dụng liều 80 mg, AUC là 6930 ng x giờ/mL và Cmax là 82,5 ng/mL. Thời gian đạt Cmax (Tmax) khoảng bốn giờ sau khi dùng thuốc. Việc ăn uống cùng thức ăn làm giảm Cmax 48% và AUC0-inf (diện tích dưới đường cong từ thời điểm 0 đến vô hạn) 36%.
Ở bệnh nhi từ 5 đến 12 tuổi có cân nặng dưới 20 kg, AUCinf là 5830 ng x giờ/mL và Cmax là 148 ng/mL sau khi dùng liều 2 mg/kg. Trong bệnh nhi có cân nặng từ 20 kg trở lên, AUCinf là 4360 ng x giờ/mL và Cmax là 81,1 ng/mL sau khi sử dụng liều 40 mg. Thời gian đạt Cmax dao động từ 3,5 đến 4,5 giờ.
Phân bố
Baloxavir có thể phân bố rộng rãi với thể tích phân bố đạt 1180 L. Chất chuyển hóa của nó, baloxavir, có tỷ lệ liên kết với protein huyết thanh người là 92,9–93,9%. Tỷ lệ trong tế bào máu chiếm khoảng 48,5–54,4%.
Chuyển hóa
Quá trình chuyển hóa chính của baloxavir là thông qua trung gian UGT1A3 để tạo thành liên kết axit glucuronic. Sau đó, nó được chuyển hóa bởi CYP3A4 thành dạng sulfoxide.
Thải trừ
Baloxavir chủ yếu được thải qua mật. Khoảng 80,1% tổng liều được bài tiết qua phân. Khoảng 14,7% liều dùng được bài tiết qua nước tiểu, trong đó có 3,3% liều thu hồi dưới dạng thuốc gốc không đổi. Tốc độ thanh thải của baloxavir là 10,3 L/giờ. Thời gian bán hủy biểu kiến cuối cùng của baloxavir là 79,1 giờ.
Độc tính ở người
Các tác dụng phụ thông thường sau khi sử dụng một liều duy nhất baloxavir marboxil bao gồm tiêu chảy, viêm phế quản, cảm lạnh thông thường, nhức đầu và buồn nôn. Tuy nhiên, thông tin về kinh nghiệm lâm sàng với quá liều baloxavir còn hạn chế. Trong một nghiên cứu đơn liều tăng dần trên những người tình nguyện khỏe mạnh, đã sử dụng liều baloxavir lên đến 80 mg mà không có mối lo ngại đáng kể.
Tính an toàn
Dữ liệu về việc sử dụng baloxavir marboxil ở phụ nữ mang thai để dự đoán hoặc thông báo về nguy cơ phát triển bất lợi liên quan đến thuốc hiện chưa có. Tuy nhiên, việc nhiễm virút cúm khi mang thai có thể gây rủi ro cho cả người mẹ và thai nhi. Trên cơ sở các nghiên cứu sinh sản trên động vật, không tìm thấy bất kỳ tác động phát triển bất lợi nào ở chuột hoặc thỏ khi sử dụng baloxavir marboxil qua đường uống với mức phơi nhiễm xấp xỉ 5 (đối với chuột) và 7 (đối với thỏ) so với mức phơi nhiễm baloxavir marboxil toàn thân ở liều khuyến cáo tối đa ở con người.
Về việc nuôi con bằng sữa mẹ, không có dữ liệu về sự hiện diện của baloxavir marboxil trong sữa mẹ, tác động lên trẻ bú mẹ hoặc ảnh hưởng đến sản xuất sữa. Trong nghiên cứu trên chuột cho con bú, baloxavir và các chất chuyển hóa có liên quan đã được tìm thấy trong sữa.
Tuy nhiên, vì không có đủ thông tin về tính an toàn khi sử dụng baloxavir marboxil trong thai kỳ và khi cho con bú, các quyết định sử dụng thuốc nên được thực hiện sau sự tư vấn của bác sĩ và cân nhắc kỹ lưỡng các lợi ích và rủi ro tiềm năng.
Tương tác với thuốc khác
Khi sử dụng baloxavir marboxil, không nên dùng đồng thời với các sản phẩm sữa, đồ uống tăng cường canxi, thuốc nhuận tràng, thuốc kháng axit hoặc chất bổ sung đường uống chứa canxi, sắt, magiê, selen, nhôm hoặc kẽm.
Lưu ý khi sử dụng Baloxavir marboxil
Khi điều trị quá liều baloxavir marboxil, cần áp dụng các biện pháp hỗ trợ chung, bao gồm theo dõi các dấu hiệu sống còn và quan sát tình trạng sức khỏe của bệnh nhân. Hiện chưa có thuốc giải độc đặc hiệu khi quá liều baloxavir marboxil. Baloxavir, thành phần hoạt chất, gắn kết chặt với protein huyết thanh, do đó khó có thể loại bỏ nhanh chóng bằng quá trình lọc qua thận.
Thuốc nên được sử dụng càng sớm càng tốt sau khi bệnh nhân bắt đầu xuất hiện các triệu chứng cúm (trong vòng 48 giờ sau khi xuất hiện triệu chứng).
Cần thận trọng khi sử dụng thuốc này cho bệnh nhân mắc các loại di truyền hiếm gặp không thể hấp thụ được một số loại đường.
Một vài nghiên cứu của Baloxavir marboxil trong Y học
So sánh các thuốc kháng vi-rút đối với hậu quả của bệnh cúm theo mùa ở người lớn khỏe mạnh và trẻ em
Tầm quan trọng: Điều trị cúm bằng thuốc kháng vi-rút được khuyến nghị cho những bệnh nhân mắc bệnh giống cúm trong thời kỳ vi-rút cúm và SARS-CoV-2 đồng lưu hành trong cộng đồng; tuy nhiên, vẫn còn câu hỏi về phương pháp điều trị nào mang lại kết quả tốt nhất và ít tác dụng phụ nhất.
Mục tiêu: So sánh hiệu quả và độ an toàn của thuốc ức chế neuraminidase và thuốc ức chế endonuclease trong điều trị cúm theo mùa ở người lớn và trẻ em khỏe mạnh.
Nguồn dữ liệu: Medline, Embase và Sổ đăng ký thử nghiệm lâm sàng Cochrane đã được tìm kiếm từ khi bắt đầu đến tháng 1 năm 2020 (lần tìm kiếm cuối cùng được cập nhật vào tháng 10 năm 2020).
Lựa chọn nghiên cứu: Các nghiên cứu được đưa vào là các thử nghiệm lâm sàng ngẫu nhiên được tiến hành ở những bệnh nhân ở mọi lứa tuổi bị cúm được điều trị bằng thuốc ức chế neuraminidase (ví dụ: oseltamivir, peramivir, zanamivir hoặc laninamivir) hoặc thuốc ức chế endonuclease (ví dụ: baloxavir) so với các thuốc có hoạt tính khác hoặc giả dược.
Khai thác và tổng hợp dữ liệu: Hai nhà điều tra đã xác định các nghiên cứu và dữ liệu trừu tượng hóa độc lập. Các phân tích tổng hợp mạng thường xuyên đã được thực hiện; xếp hạng tương đối của các tác nhân được thực hiện bằng cách sử dụng xác suất điểm P. Chất lượng của bằng chứng được đánh giá bằng cách sử dụng các tiêu chí Phân loại Khuyến nghị, Đánh giá, Phát triển và Đánh giá. Dữ liệu được phân tích vào tháng 10 năm 2020.
Các kết quả và biện pháp chính: Thời gian giảm bớt các triệu chứng cúm (TTAS), các biến chứng của bệnh cúm và các tác dụng phụ (tổng số tác dụng phụ, buồn nôn và nôn).
Kết quả: Tổng cộng có 26 thử nghiệm được xác định là điều tra thuốc kháng vi-rút ở liều cao hoặc thấp; những thử nghiệm này bao gồm 11 897 người tham gia, trong đó 6294 (52,9%) là nam giới và tuổi trung bình (SD) là 32,5 (16,9) tuổi. Trong tất cả các phương pháp điều trị so sánh với giả dược về kết quả hiệu quả, bằng chứng chất lượng cao chỉ ra rằng zanamivir có liên quan đến TTAS ngắn nhất (tỷ lệ rủi ro, 0,67; 95% CI, 0,58-0,77), trong khi baloxavir có liên quan đến nguy cơ lbiến chứng cúm thấp nhất (tỷ lệ rủi ro [RR], 0,51; 95% CI, 0,32-0,80) dựa trên bằng chứng chất lượng trung bình.
Về kết quả an toàn, baloxavir có nguy cơ thấp nhất về tổng số tác dụng phụ (RR, 0,84; 95% CI, 0,74-0,96) so với giả dược dựa trên bằng chứng chất lượng trung bình. Không có bằng chứng mạnh mẽ về mối liên quan với nguy cơ buồn nôn hoặc nôn trong tất cả các so sánh, ngoại trừ oseltamivir 75 mg, có liên quan đến sự xuất hiện nhiều hơn của buồn nôn (RR, 1,82; 95% CI, 1,38-2,41) và nôn (RR, 1,88 ; KTC 95%, 1,47-2,41).
Kết luận và mức độ phù hợp: Trong đánh giá hệ thống và phân tích tổng hợp mạng lưới này, tất cả 4 thuốc kháng vi-rút được đánh giá đều có liên quan đến việc rút ngắn TTAS; zanamivir có liên quan đến TTAS ngắn nhất và baloxavir có liên quan đến việc giảm tỷ lệ các biến chứng liên quan đến cúm.
Tài liệu tham khảo
- Drugbank, Baloxavir marboxil, truy cập ngày 8 tháng 7 năm 2023.
- Liu, J. W., Lin, S. H., Wang, L. C., Chiu, H. Y., & Lee, J. A. (2021). Comparison of Antiviral Agents for Seasonal Influenza Outcomes in Healthy Adults and Children: A Systematic Review and Network Meta-analysis. JAMA network open, 4(8), e2119151. https://doi.org/10.1001/jamanetworkopen.2021.19151
- Pubchem, Baloxavir marboxil, truy cập ngày 8 tháng 7 năm 2023.
- Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội
Xuất xứ: Nhật Bản
Xuất xứ: Nhật Bản