Azilsartan
Biên soạn và Hiệu đính
Dược sĩ Xuân Hạo
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
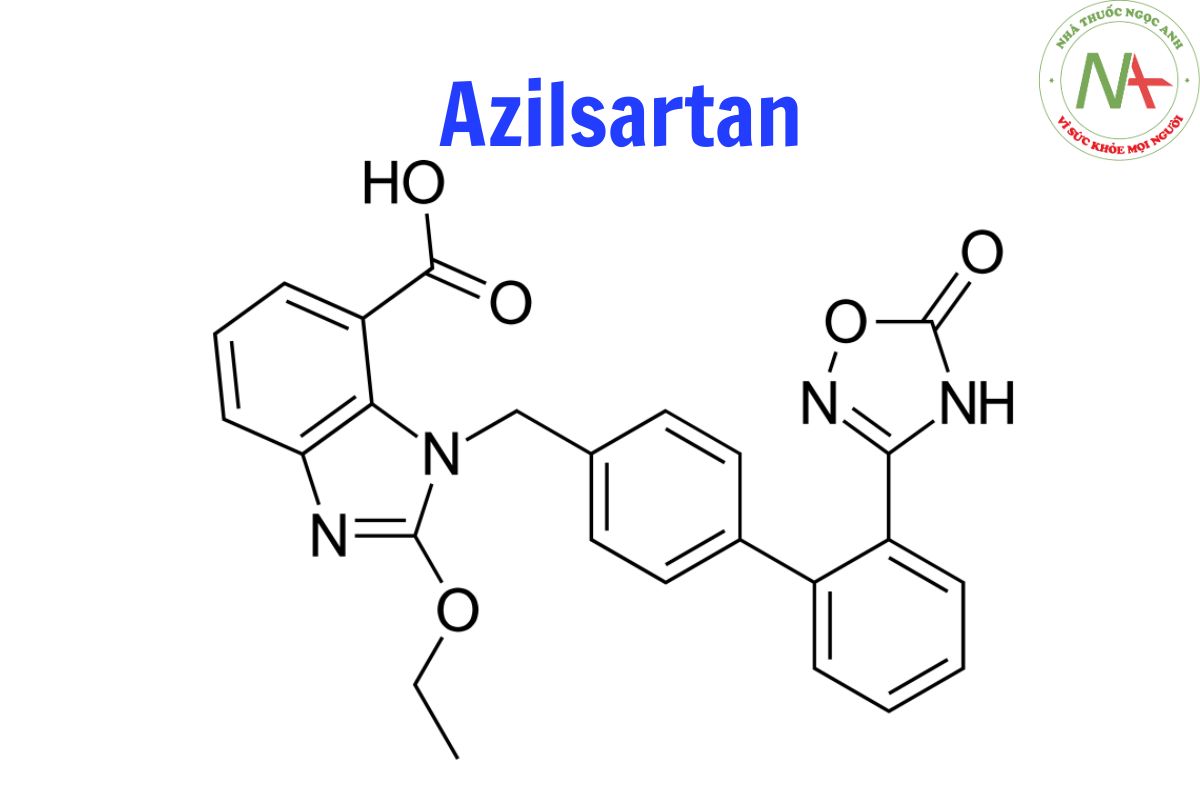
2-ethoxy-3-[[4-[2-(5-oxo-4H-1,2,4-oxadiazol-3-yl)phenyl]phenyl]methyl]benzimidazole-4-carboxylic acid
Nhóm thuốc
Thuốc đối kháng Angiotensin II
Mã ATC
C – Hệ tim mạch
C09 – Thuốc có tác dụng trên hệ Renin – Angiotensin
C09C – Các chất đối kháng Angiotensin II, đơn chất
C09CA – Các chất đối kháng Angiotensin II, đơn chất
C09CA09 – Azilsartan medoxomil
C – Hệ tim mạch
C09 – Thuốc có tác dụng trên hệ Renin – Angiotensin
C09D – Các chất đối kháng Angiotensin II, phối hợp
C09DA – Thuốc đối kháng Angiotensin II và thuốc lợi tiểu
C09DA09 – azilsartan medoxomil và diuretics
Phân loại nguy cơ cho phụ nữ có thai
D
Mã UNII
F9NUX55P23
Mã CAS
147403-03-0
Cấu trúc phân tử
Công thức phân tử
C25H20N4O5
Phân tử lượng
456.4
Cấu trúc phân tử
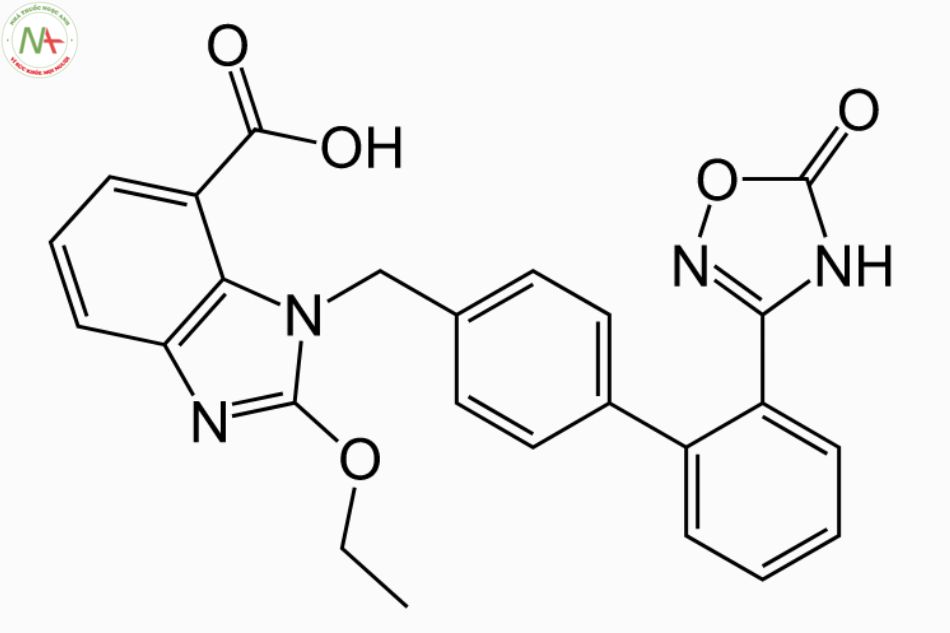
Azilsartan là một axit benzimidazolecarboxylic, có cấu trúc axit benzimidazole-7-carboxylic được thế ở vị trí 2 bởi một nhóm methoxy và ở vị trí 1 bởi một 2′-[(5-oxo-4,5-dihydro-1,2,4-oxadiazol- nhóm 3-yl)biphenyl-4-yl]metyl.
Các tính chất phân tử
Số liên kết hydro cho: 2
Số liên kết hydro nhận: 7
Số liên kết có thể xoay: 7
Diện tích bề mặt tôpô: 115 Ų
Số lượng nguyên tử nặng: 34
Các tính chất đặc trưng
Điểm nóng chảy: 212-214 °C
Điểm sôi: 748.0 ± 70.0 °C ở 760 mmHg
Tỷ trọng riêng: 1.5 ± 0.1 g/cm3
Độ tan trong nước: 4,28 x 10-3 mg/L ở 25 °C
Hằng số phân ly pKa: 6.1
Chu kì bán hủy: 11 giờ
Khả năng liên kết với Protein huyết tương: >99%
Cảm quan
Azilsartan có dạng bột kết tinh màu trắng, tan được trong methanol và không tan trong nước.
Dạng bào chế
Viên nén: 20 mg; 40 mg; 80 mg.
Độ ổn định và điều kiện bảo quản
Viên nén azilsartan nên được bảo quản trong bao bì gốc của nhà sản xuất, ở nhiệt độ phòng và tránh ánh nắng trực tiếp.
Nguồn gốc
Azilsartan được phát triển bởi Takeda và được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phê duyệt để điều trị huyết áp cao ở người lớn vào tháng 2 năm 2011. Hiện nay, azilsartan có sẵn như một loại thuốc generic.
Dược lý và cơ chế hoạt động
Hệ thống renin-angiotensin-aldosterone có vai trò điều hòa huyết áp. Trong đó, angiotensin II là một hormone peptide, là tác nhân tăng huyết áp chính trong hệ thống này.
Angiotensin II là một chất co mạch mạnh và trực tiếp, thông qua liên kết với thụ thể angiotensin II loại 1 (thụ thể AT1) để kích thích tổng hợp và giải phóng aldosterone, dẫn đến thúc đẩy kích thích tim.
Hơn nữa, angiotensin II thúc đẩy tái hấp thu natri ở ống thận, dẫn đến giữ nước và nó cũng ức chế tiết thêm renin. Các thụ thể AT1 hiện diện cao ở cơ trơn mạch máu và tuyến thượng thận.
Azilsartan liên kết chọn lọc với thụ thể AT1 như một chất đối kháng, ức chế tác dụng co mạch và tiết aldosteron của angiotensin II. Thuốc có ái lực với thụ thể AT1 lớn hơn 10.000 lần so với thụ thể AT2, thụ thể này chủ yếu liên quan đến cân bằng nội môi tim mạch.
Azilsartan dường như tách khỏi các thụ thể AT1 chậm hơn nhiều so với các ARB khác, điều này giải thích thời gian tác dụng dài hơn của nó khi so sánh với các ARB khác.
Khả năng ức chế tác dụng tăng huyết áp của truyền angiotensin II liên quan đến liều lượng. Ở liều duy nhất 32 mg, azilsartan ức chế tác dụng tăng huyết áp tối đa khoảng 90% ở nồng độ đỉnh trong huyết tương và 60% sau 24 giờ dùng thuốc. Ở những đối tượng khỏe mạnh dùng liều đơn và liều lặp lại, nồng độ angiotensin I và II trong huyết tương và hoạt tính renin trong huyết tương tăng lên, trong khi nồng độ aldosterone trong huyết tương giảm.
Giống như các ARB khác, azilsartan làm giảm sức cản ngoại biên phụ thuộc vào liều và giảm trương lực cơ trơn mạch máu. Vì azilsartan chẹn thụ thể angiotensin II, phản hồi điều hòa âm tính của angiotensin II đối với bài tiết renin bị ức chế. Tuy nhiên, kết quả là tăng hoạt tính renin huyết tương và nồng độ angiotensin II trong tuần hoàn không khắc phục được tác dụng hạ huyết áp của azilsartan.
Tác dụng hạ huyết áp của thuốc hạ huyết áp có thể giảm ở bệnh nhân gốc Phi. Tuy nhiên, không có khuyến cáo điều chỉnh liều azilsartan trên cơ sở giới tính, chủng tộc hoặc mức độ suy thận hoặc suy gan của bệnh nhân.
Ngoài ra, azilsartan có ảnh hưởng không đáng kể đến nồng độ kali hoặc natri huyết thanh và không ảnh hưởng đến quá trình sinh tổng hợp nồng độ angiotensin II và bradykinin. Nó cũng không liên kết với bất kỳ kênh ion nào có liên quan đến quá trình điều hòa tim mạch.
Ứng dụng trong y học
Azilsartan là thuốc hạ huyết áp được phát triển tương đối mới, lần đầu tiên được FDA chấp thuận vào tháng 2 năm 2011. Nhiều hướng dẫn khuyến cáo sử dụng ARB như liệu pháp đầu tay khi bắt đầu điều trị hạ huyết áp và chỉ ra rằng hiệu quả lâm sàng của ARB tương đương với angiotensin- thuốc ức chế men chuyển (ACE) cũng được sử dụng làm phương pháp điều trị đầu tay cho bệnh tăng huyết áp.
Azilsartan được bán trên thị trường dưới tên thương hiệu Edarbi. Nó được sử dụng để điều trị tăng huyết áp ở bệnh nhân trên 18 tuổi dưới dạng đơn trị liệu hoặc kết hợp với các thuốc hạ huyết áp khác. Nó cũng có sẵn trong một sản phẩm kết hợp với chlorthalidone.
Vì tăng huyết áp là một yếu tố nguy cơ chính đối với bệnh tim mạch, nên việc kiểm soát tăng huyết áp sớm có một số ý nghĩa đối với tỷ lệ sống sót và chất lượng cuộc sống của bệnh nhân trong tương lai.
Việc hạ huyết áp có liên quan đến việc giảm nguy cơ các biến cố tim mạch có thể gây tử vong hoặc không, chủ yếu là đột quỵ và nhồi máu cơ tim. Azilsartan do đó được suy đoán là làm giảm tỷ lệ tử vong và sự khởi phát của bệnh tim mạch. Mặc dù chưa xác định được ý nghĩa lâm sàng, nhưng azilsartan có thể có khả năng sử dụng ngoài hướng dẫn ở những bệnh nhân có tiền sử nhồi máu cơ tim hoặc suy tim.
Ngoài ra, azilsartan cũng được sử dụng để làm giảm sự tiến triển của albumin niệu từ trung bình đến nặng và ngăn ngừa rung tâm nhĩ tái phát khi sử dụng ngoài hướng dẫn ở bệnh nhân đái tháo đường và tăng huyết áp.
Dược động học
Hấp thu
Sinh khả dụng tuyệt đối ước tính của azilsartan sau khi dùng azilsartan medoxomil là khoảng 60%. Sau khi uống azilsartan medoxomil, nồng độ đỉnh trong huyết tương (Cmax) của azilsartan đạt được trong vòng 1,5 đến 3 giờ.
Nồng độ azilsartan ở trạng thái ổn định đạt được trong vòng năm ngày và không có sự tích tụ trong huyết tương xảy ra với liều lượng lặp đi lặp lại mỗi ngày một lần. Thực phẩm không ảnh hưởng đến khả dụng sinh học của azilsartan.
Phân bố
Thể tích phân bố azilsartan là khoảng 16 L. Ở chuột cống, một lượng tối thiểu thuốc được đánh dấu phóng xạ đã vượt qua hàng rào máu não. Hơn nữa, azilsartan qua được hàng rào nhau thai ở chuột mang thai và được phân phối cho bào thai.
Azilsartan liên kết cao với protein huyết tương của con người (>99%), chủ yếu là albumin huyết thanh. Liên kết protein là không đổi ở nồng độ azilsartan trong huyết tương vượt quá phạm vi đạt được với liều khuyến cáo.
Chuyển hóa
Azilsartan được chuyển hóa thành hai chất chuyển hóa chính không có hoạt tính. Chất chuyển hóa chính trong huyết tương được hình thành bởi O-dealkyl hóa, được gọi là chất chuyển hóa M-II, và chất chuyển hóa thứ yếu được hình thành bởi quá trình khử carboxyl, được gọi là chất chuyển hóa M-I.
Các enzyme CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1, và CYP3A4 đều có khả năng chuyển hóa azilsartan. Tuy nhiên, CYP2C9 cho thấy hoạt động cao nhất trong quá trình chuyển hóa azilsartan thành M-II và CYP2C8 trong quá trình chuyển hóa azilsartan thành M-I.
Thải trừ
Sau một liều uống azilsartan, khoảng 55% liều thuốc được thải trừ qua phân và khoảng 42% qua nước tiểu, với 15% liều bài tiết qua nước tiểu dưới dạng không đổi. Thời gian bán hủy của azilsartan là khoảng 11 giờ và độ thanh thải thận là khoảng 2,3 mL/phút.
Độc tính ở người
Không có liều độc tối đa nào được thiết lập cho azilsartan. Dữ liệu về con người liên quan đến quá liều azilsartan medoxomil còn hạn chế. Trong các thử nghiệm lâm sàng, các đối tượng khỏe mạnh dung nạp tốt liều một lần mỗi ngày lên đến 320 mg azilsartan medoxomil.
Tính an toàn
Sinh sản
Azilsartan không có tác dụng phụ đối với khả năng sinh sản của chuột cống đực hoặc cái ở liều uống lên đến 1.000 mg/kg/ngày.
Thời kỳ mang thai
Các thuốc tác động trực tiếp lên hệ thống renin-angiotensin (ví dụ: thuốc ức chế men chuyển, thuốc đối kháng thụ thể angiotensin II) làm giảm chức năng thận của thai nhi, tăng tỷ lệ mắc bệnh và tử vong ở thai nhi và trẻ sơ sinh khi sử dụng trong ba tháng giữa và cuối thai kỳ. Hơn nữa, thuốc ức chế men chuyển cũng có thể làm tăng nguy cơ dị tật bẩm sinh nghiêm trọng khi dùng trong ba tháng đầu của thai kỳ.
Vì vậy, azilsartan nên được ngừng sử dụng càng sớm càng tốt khi phát hiện có thai. Tuy nhiên, lợi ích tiềm năng từ việc sử dụng thuốc có thể lớn hơn nguy cơ tiềm ẩn. Chẳng hạn như thuốc có thể được sử dụng nếu cần trong tình huống đe dọa tính mạng hoặc bệnh nghiêm trọng mà các loại thuốc an toàn hơn không thể sử dụng hoặc không hiệu quả.
Thời kỳ cho con bú
Azilsartan được phân phối vào sữa ở chuột nhưng người ta không biết liệu thuốc có được phân phối vào sữa mẹ hay không. Do đó cần tránh sử dụng azilsartan hoặc ngừng cho con bú trong thời gian điều trị.
Trẻ em
Tính an toàn và hiệu quả của azilsartan chưa được xác định ở trẻ em dưới 18 tuổi.
Người cao tuổi
Tỷ lệ tăng nồng độ creatinine huyết thanh cao hơn được báo cáo ở những bệnh nhân từ 75 tuổi trở lên so với những bệnh nhân trẻ tuổi hơn. Tuy nhiên, không có sự khác biệt nào khác về tính an toàn và hiệu quả so với những người trẻ tuổi được báo cáo, nhưng cũng không thể loại trừ khả năng nhạy cảm tăng lên.
Suy thận
Bởi vì hệ thống renin-angiotensin-aldosterone (RAA) dường như góp phần đáng kể vào việc duy trì mức lọc cầu thận ở bệnh nhân suy tim sung huyết nặng, hẹp động mạch thận hoặc giảm thể tích tuần hoàn, chức năng thận có thể xấu đi rõ rệt (ví dụ: thiểu niệu, tăng nitơ máu tiến triển, hiếm gặp hơn là suy thận cấp và tử vong) ở những bệnh nhân này trong khi điều trị bằng thuốc ức chế men chuyển hoặc thuốc đối kháng thụ thể angiotensin II.
Mặc dù cho đến nay, các báo cáo được ghi nhận liên quan đến những bệnh nhân được điều trị bằng thuốc ức chế men chuyển và các thuốc đối kháng thụ thể angiotensin II khác, nhưng tác dụng phụ này cũng có thể xảy ra khi azilsartan được sử dụng theo cách tương tự.
Suy gan
Azilsartan có liên quan đến tỷ lệ tăng aminotransferase huyết thanh thấp, trong các thử nghiệm có kiểm soát, tỷ lệ này không cao hơn so với điều trị bằng giả dược. Những độ cao này là thoáng qua và hiếm khi cần điều chỉnh liều. Hơn nữa, không có trường hợp cụ thể nào về tổn thương gan cấp tính rõ ràng trên lâm sàng được báo cáo liên quan đến liệu pháp azilsartan.
Các ARB khác có liên quan đến các trường hợp nhiễm độc gan có triệu chứng hiếm gặp. Khởi phát tổn thương gan thường trong vòng 1 đến 8 tuần kể từ khi bắt đầu điều trị và dạng enzym huyết thanh điển hình là tế bào gan với hội chứng lâm sàng giống viêm gan cấp tính. Trong một số trường hợp, ứ mật đã phát triển có thể kéo dài và tái phát, nhưng liệu pháp ARB không liên quan đến hội chứng ống mật biến mất hoặc tổn thương gan mãn tính.
Các biểu hiện dị ứng miễn dịch (phát ban, sốt, tăng bạch cầu ái toan) không phổ biến, cũng như sự hình thành tự kháng thể.
Ung thư
Không có bằng chứng về khả năng gây ung thư khi azilsartan được dùng trong chế độ ăn cho chuột nhắt và chuột cống trong tối đa hai năm.
Đột biến
Azilsartan và chất chuyển hóa của nó không có khả năng gây độc gen trong thử nghiệm đột biến đảo ngược Ames với Salmonella typhimurium và Escherichia coli, thử nghiệm đột biến chuyển tiếp tế bào buồng trứng chuột Hamster Trung Quốc in vitro, thử nghiệm đột biến gen u lympho chuột in vitro, xét nghiệm tổng hợp DNA đột xuất ex vivo và xét nghiệm vi nhân tủy xương chuột và/hoặc chuột in vivo.
Tương tác với thuốc khác
Vì việc sử dụng các chất bổ sung kali và các chất thay thế muối chứa kali hoặc các thuốc lợi tiểu giữ kali (ví dụ amiloride, spironolactone, triamterene) với chất đối kháng thụ thể angiotensin II (ví dụ, azilsartan) có thể làm tăng khả năng tăng kali máu, nên một số bác sĩ lâm sàng đã gợi ý rằng nên tránh sử dụng đồng thời các chất này với azilsartan.
Điều trị đồng thời với thuốc chống viêm không steroid (NSAIDs), bao gồm thuốc ức chế chọn lọc cyclooxygenase-2 (COX-2) và thuốc đối kháng thụ thể angiotensin II có thể dẫn đến suy giảm chức năng thận, bao gồm cả suy thận cấp ở bệnh nhân cao tuổi, giảm thể tích tuần hoàn (bao gồm cả những người đang điều trị bằng thuốc lợi tiểu), hoặc chức năng thận bị tổn thương. Mặc dù những hiệu ứng này thường có thể đảo ngược nhưng chức năng thận nên được theo dõi định kỳ ở những bệnh nhân điều trị bằng azilsartan và NSAID. Ngoài ra, tác dụng hạ huyết áp của azilsartan có thể bị suy giảm ở những bệnh nhân dùng NSAID, bao gồm cả thuốc ức chế chọn lọc COX-2.
Sự gia tăng có hồi phục creatinine huyết thanh có thể xảy ra ở những bệnh nhân dùng azilsartan, và có thể lớn hơn ở những bệnh nhân sử dụng đồng thời với hydrochlorothiazide.
Lưu ý khi sử dụng Azilsartan
Vì hạ huyết áp có triệu chứng có thể xảy ra ở những bệnh nhân có hệ thống renin-angiotensin hoạt hóa (ví dụ, bệnh nhân bị giảm thể tích hoặc giảm muối thứ phát do dùng thuốc lợi tiểu liều cao), azilsartan nên được bắt đầu ở những bệnh nhân này sau khi tình trạng giảm thể tích hoặc giảm muối được điều chỉnh, hoặc liều ban đầu thấp hơn liều lượng thuốc nên sử dụng.
Nếu hạ huyết áp xảy ra ở bệnh nhân dùng azilsartan, nên đặt bệnh nhân ở tư thế nằm ngửa và nếu cần, nên truyền tĩnh mạch natri clorid 0,9%.
Hạ huyết áp thoáng qua không phải là chống chỉ định với các liều azilsartan bổ sung, và việc điều trị bằng thuốc có thể được khôi phục một cách thận trọng sau khi huyết áp đã được ổn định (ví dụ, khi tăng thể tích tuần hoàn).
Một vài nghiên cứu của Azilsartan trong Y học
Hiệu quả và độ an toàn của azilsartan 10 mg so với candesartan cilexetil 8mg ở bệnh nhân Nhật Bản bị tăng huyết áp
Nghiên cứu này đã điều tra xem liệu 10 mg azilsartan mỗi ngày, bằng một nửa liều lượng bình thường, có tốt hơn 8 mg candesartan cilexetil mỗi ngày để kiểm soát huyết áp ở bệnh nhân Nhật Bản bị tăng huyết áp hay không.

Trong thử nghiệm chéo, ngẫu nhiên, nhãn mở này, 309 người trưởng thành Nhật Bản bị tăng huyết áp được điều trị bằng candesartan cilexetil 8 mg được chia ngẫu nhiên thành hai nhánh và nhận azilsartan 10 mg hoặc candesartan cilexetil 8 mg theo cách chéo.
Kết quả chính về hiệu quả là huyết áp tâm thu và giới hạn không thua kém được đặt là 2,5 mm Hg. Những người tham gia là 67 ± 11 tuổi và 180 (58%) là nam giới. Mức huyết áp tâm thu và tâm trương ban đầu lần lượt là 127,1 ± 13,2 và 69,7 ± 11,2 mm Hg.
Trong thời gian nghiên cứu, sự khác biệt về huyết áp tâm thu giữa các phương pháp điều trị bằng azilsartan 10 mg và candesartan cilexetil 8 mg là -1,7 mm Hg, với khoảng tin cậy (CI) 95% hai phía nằm trong khoảng từ -3,2 đến -0,2 mm Hg.
Ranh giới trên của khoảng tin cậy 95% nằm dưới ngưỡng 2,5 mm Hg, xác nhận tính không thua kém của azilsartan 10 mg so với candesartan cilexetil 8 mg. Sự khác biệt cũng đạt mức ý nghĩa (P=0,037). Sự khác biệt tương ứng về huyết áp tâm trương là -1,4 (KTC 95%: -2,4 đến -0,4) mm Hg (P=0,006). Điều trị bằng azilsartan 10 mg tương tự như candesartan cilexetil 8 mg liên quan đến các tác dụng phụ hiếm gặp.
Tóm lại, azilsartan 10 mg không thua kém candesartan cilexetil 8 mg trong việc kiểm soát huyết áp tâm thu ở bệnh nhân tăng huyết áp Nhật Bản đã được điều trị bằng candesartan cilexetil 8 mg.
Tài liệu tham khảo
- Drugbank, Azilsartan, truy cập ngày 2 tháng 3 năm 2023.
- Takahara, M., Shiraiwa, T., Shindo, M., Arai, A., Kusuda, Y., Katakami, N., Kaneto, H., Matsuoka, T. A., & Shimomura, I. (2014). Efficacy and safety of 10-mg azilsartan compared with 8-mg candesartan cilexetil in Japanese patients with hypertension: a randomized crossover non-inferiority trial. Hypertension research : official journal of the Japanese Society of Hypertension, 37(9), 852–857.
- Pubchem, Azilsartan, truy cập ngày 2 tháng 3 năm 2023.
- Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội
