Bệnh hô hấp
Các kỹ thuật đặc biệt của hỗ trợ hô hấp trong thông khí hỗ trợ cho trẻ sơ sinh
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
nhathuocngocanh.com – Bài viết Các kỹ thuật đặc biệt của hỗ trợ hô hấp trong thông khí hỗ trợ cho trẻ sơ sinh của tác giả Nelson Claure và Eduardo Bancalari được biên dịch bởi Thạc sĩ – Bác sĩ Đặng Thanh Tuấn công tác tại Khoa Hồi sức ngoại – Bệnh viện Nhi đồng I.
Nội dung chính
- Ở trẻ sinh non, độ bão hòa oxy (oxygen saturation – SpO2) động mạch không được duy trì nhất quán trong phạm vi mục tiêu bằng cách điều chỉnh thủ công nồng độ oxy trong khi hít vào (FiO2) suốt quá trình chăm sóc làm sang định kỳ
- Kiểm soát tự động nồng độ oxy trong khi hít vào (fraction of inspired oxygen – FiO2) có thể cải thiện mục tiêu SpO, đồng thời giảm tiếp xúc với tăng oxy – máu, oxy bổ sung và các đợt giảm oxy máu nghiêm trọng. Tác động của việc ứng dụng rộng rãi công nghệ này trên lâm sàng đối với kết quả so sinh vẫn đang được xác định.
- Thông khí hỗ trợ theo tỷ lệ (proportional assist ventilation – PAV) có thể duy trì thông khi tương đương với áp lực thấp hơn so với các chế độ được kiếm soát áp lực thông thường. Cần có các nghiên cứu sâu hơn để xác định xem việc sử dụng phương pháp này lâu hơn có thể cải thiện kết quả hô hấp hay không.
- Hỗ trợ thông khi điều chỉnh theo tín hiệu thần kinh (neurally adjusted ventilatory assist – NAVA) có hiệu quả trong việc đồng bộ áp lực dương với hít vào tự phát của trẻ sơ sinh, đồng thời có thể duy trì thông khí với áp lực thấp hơn so với thông khi kiểm soát áp lực. Tác động của NAVA đối với kết quả hô hấp ngắn hạn và dài hạn ở trẻ sinh non vẫn cần được nghiên cứu.
- Các phương thức thông khí phút mục tiêu (targeted minute ventilation) tiến hành điều chỉnh tự động tần số máy thở để duy trì thông khi ổn định hơn. Các nghiên cứu khả thì đã chỉ ra rằng: Các phương thức thông khí phút mục tiêu có thể cung cấp sự trao đổi khí tương đương với hỗ trợ thông khi ít hơn so với các phương thức thông thưởng. Dữ liệu về kết quả sơ sinh hiện chưa có sẵn.
Giới thiệu
Việc chăm sóc trẻ sinh non bị suy hô hấp đã tiến bộ đáng kể trong những thập kỷ qua, song thực tế vẫn có một tỷ lệ không nhỏ trẻ sinh non sống sót với một số mức độ suy giảm chức năng hô hấp, thị giác và phát triển thần kinh. Ngày càng có nhiều bằng chứng cho thấy nhiều biến chứng trong số này có thể liên quan đến việc sử dụng thiết bị hỗ trợ hô hấp. Thực tế trên chỉ ra sự cần thiết phải cải thiện hơn nữa các chiến lược hỗ trợ hô hấp được sử dụng cho nhóm dân số này. Hiện đã có các kỹ thuật mới cung cấp hỗ trợ hô hấp và bổ sung oxy cho trẻ sinh non, nhưng việc ứng dụng những kỹ thuật này vẫn chưa phổ biến và không có nhiều thông tin về lợi ích hoặc hạn chế của chúng. Chương này mô tả một số phương thức trên, đồng thời thảo luận về cơ sở lý luận cũng như bằng chứng cho những ưu điểm và hạn chế khả dĩ. Các phương thức hỗ trợ hỗ hấp tiêu chuẩn được thảo luận ở các chương khác của cuốn sách này.
Kiểm soát tự động nồng độ oxy trong khí hít vào
Hầu hết trẻ sinh non đều cần oxy bổ sung để duy trì độ bão hòa oxy (SpO2) động mạch trong phạm vi mục tiêu quy định. Tuy nhiên, đã có tài liệu chứng minh rằng: Trong chăm sóc lâm sàng thông thường, việc điều chỉnh thủ công nồng độ oxy trong khí hít vào (FiO2) thường không giữ được SpO2 trong phạm vi cho phép. Cũng có báo cáo cho rằng trẻ sinh non dành gần một phần ba thời gian với mức SpO, trên phạm vi mục tiêu vì FiO2 quá cao. Hậu quả của tăng oxy máu là làm tăng nguy cơ tổn thương mắt, não và các cơ quan khác, trong khi tiếp xúc với FiO2 cao hơn mức cần thiết có thể dẫn đến tổn thương oxy hóa đối với phổi. Cùng một báo cáo cho thấy trẻ sinh non dành gần một phần tư thời gian với SpO2 dưới phạm vi mục tiêu. Tình trạng này được cho là xuất phát từ các đợt giảm oxy máu từng đợt xảy ra thường xuyên ở trẻ sinh non vì hô hấp của chúng không ổn định. Tần suất các đợt này tăng lên theo tuổi sau sinh, đặc biệt ở trẻ bị bệnh phổi mãn tính. Hầu hết các đợt giảm oxy máu là tự phát, nhưng một số có liên quan đến quy trình chăm sóc. Phản ứng kịp thời của nhân viên lâm sàng có thể làm giảm thời gian và mức độ nghiêm trọng của các đợt giảm oxy máu. Tuy nhiên, sự sẵn sàng của nhân viên trong việc thực hiện nhiệm vụ này thường hạn chế. Tác động từ sự sẵn sàng của nhân viên đối với việc duy trì SpO2 trong phạm vi mục tiêu đã được ghi nhận bởi sự giảm tỷ lệ thời gian với SpO2 trong phạm vi, do giảm tỷ lệ điều dưỡng so với trẻ sơ sinh. Điều này chủ yếu là do tăng thời gian tăng oxy máu. Ngoài ra, FiO2 tăng trong các đợt giảm oxy máu, nhưng việc giải quyết tình trạng giảm oxy máu không phải lúc nào cũng theo sát sau đó bằng cách đưa FiO2 trở lại mức ban đầu ngay lập tức, gây tăng oxy máu. Bởi vì các đợt giảm oxy máu một phần liên quan đến mức cơ bản của SpO2 nên mức SpO2 cao hơn thường được dung nạp để cố gắng ngăn chặn sự xuất hiện của chúng, nhưng phương pháp thực hành này có thể dẫn đến tăng phơi nhiễm với chứng tăng oxy máu.
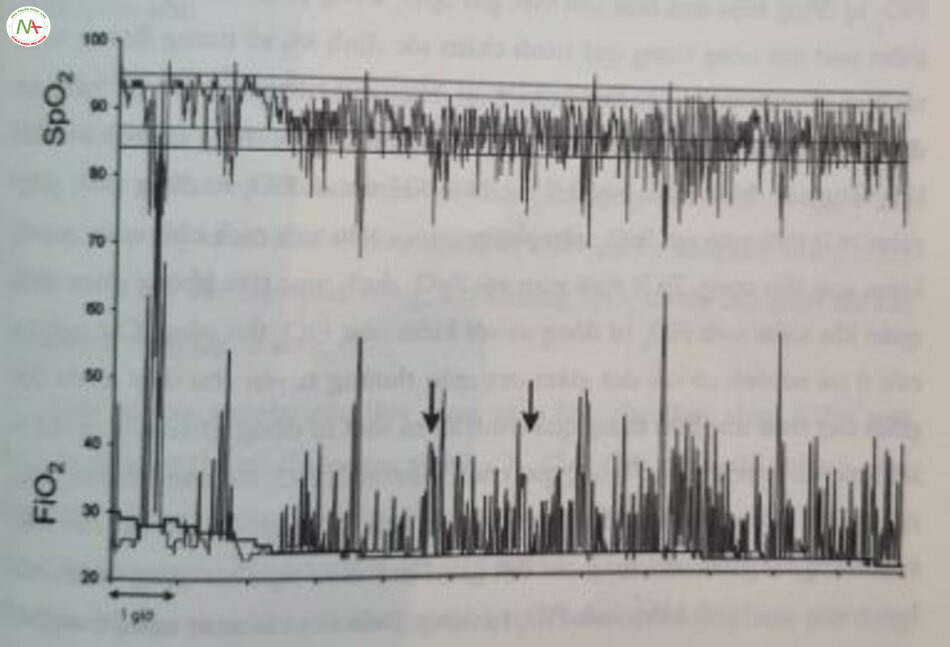
Những vấn đề trên giải thích tại sao việc duy trì ổn định SpO2 trong phạm vi mục tiêu quy định hiếm khi thành công ở trẻ sinh non được bổ sung oxy. Với nỗ lực giải quyết vấn đề này, các hệ thống khác nhau để kiểm soát FiO2 vòng lặp kín (closed-loop) tự động đã được phát triển, nhằm hỗ trợ người chăm sóc duy trì SpO2 trong phạm vi mục tiêu quy định, đồng thời giảm phơi nhiễm với tăng oxy máu và giảm oxy máu. Các hệ thống này liên tục điều chỉnh FiO2 nhằm mục đích giữ SpO2 trong phạm vi mục tiêu do bác sĩ lâm sàng đặt ra. Hình 23.1 minh họa các bản ghi đại diện của SpO2 và FiO2 từ một trẻ sinh non với các đợt giảm oxy máu thường xuyên trong quá trình kiểm soát FiO2 tự động, cho thấy rõ nhu cầu tối thiểu phải điều chỉnh FiO2 thủ công.
Các nghiên cứu lâm sàng ngắn hạn đã chỉ ra rằng: Hệ thống kiểm soát FiO2 tự động hiệu quả hơn cho việc giữ SpO2 trong phạm vi mục tiêu so với kiểm soát thủ công trong quá trình chăm sóc định kỳ, và tương đương hoặc tốt hơn so với y tá chuyên tâm hoàn toàn. Hiệu quả tương đối của hệ thống tự động so với điều chỉnh thủ công thông thường thu được trong các nghiên cứu lâm sàng này được trình bày ở Bảng 23.1. Kiểm soát FiO2 tự động cũng giúp giảm tỷ lệ thời gian với SpO2 trên phạm vi mục tiêu một cách nhất quán so với kiểm soát thủ công. Tỷ lệ thời gian với SpO2 dưới mục tiêu không giảm nhất quán khi kiểm soát FiO2 tự động so với kiểm soát FiO2 thủ công. Các nghiên cứu ở trẻ sơ sinh có các đợt giảm oxy máu thường xuyên cho thấy nhiều đợt giảm oxy máu nhẹ hơn trong quá trình kiểm soát tự động. Điều này có thể là kết quả của thực tế rằng: Trong quá trình kiểm soát FiO2 thủ công thường quy, trẻ sơ sinh được giữ ở mức SpO2 cơ bản cao hơn. Các nghiên cứu này cho thấy tình trạng sụt giảm số lượng các đợt giảm oxy máu nghiêm trọng và kéo dài hơn trong quá trình kiểm soát FiO2 tự động. Điều này rất quan trọng trong bối cảnh các báo cáo về tổn thương mắt và phát triển thần kinh nghiêm trọng có liên đến các đợt giảm oxy máu kéo dài. Những phát hiện trên cho thấy quan một thực tế là hệ thống kiểm soát FiO2 không ngăn được các đợt giảm oxy máu, nhưng những hệ thống này đáp ứng nhanh hơn, nhờ đó có thể làm giảm thời lượng và mức độ nghiêm trọng của chúng.
Số lần thay đổi thủ công của FiO2 là tối thiểu trong quá trình kiểm soát FIO2 tự động. Điều này cho thấy khả năng tiết giảm khối lượng công việc của nhân viên, cũng như khả năng chuyển nỗ lực của nhân viên sang các lĩnh vực chăm sóc y tế khác. Báo động SpO2 là một trong những hiện tượng phổ biến nhất ở khoa chăm sóc đặc biệt dành cho trẻ sơ sinh (NICU). Mặc dù chưa được kiểm tra, song các hệ thống kiểm soát FiO2 tự động có thể làm giảm sự mệt mỏi khi cảnh báo SpO2 trong quá trình sử dụng kéo dài. Mặt khác, việc giảm sự chú ý của nhân viên là hậu quả tiềm ẩn ngoài ý muốn của kiểm soát FiO2 tự động. Gia tăng tự động FiO2 có thể che giấu tình trạng suy giảm hô hấp mà nếu không sẽ biểu hiện bằng SpO2 thấp hơn liên tục. Do đó, các hệ thống kiểm soát FiO2 tự động nhất thiết phải thông báo cho bác sĩ khi có nhu cầu liên tục vé FiO2 cao hơn.
Sự khác biệt đáng kể có thể tồn tại giữa mục tiêu và phạm vi SpO2 thực tế trong quá trình chăm sóc thường quy. Cần thận trọng khi cài đặt phạm vi SpO2 được nhằm mục tiêu bởi các hệ thống tự động, vì có thể có ngụ ý lâm sàng quan trọng và trở nên rõ ràng khi SpO2 được giữ ổn định hơn trong phạm vi đó. Điều này đặc biệt quan trọng, bởi khoảng SpO2 tối ưu cho quần thể này chưa được thiết lập rõ ràng.
Tóm lại, các nghiên cứu lâm sàng ngắn hạn cho thấy rằng: Kiểm soát FiO2 tự động có thể cải thiện mục tiêu SpO2 đồng thời giảm tiếp xúc với tăng oxy máu, bổ sung oxy và các đợt giảm oxy máu nghiêm trọng. Việc ứng dụng rộng rãi công nghệ này trên lâm sàng có thể tác động đến kết quả phát triển thị giác, hô hấp và thần kinh lâu dài ở trẻ sinh non hay không hiện vẫn đang được xác định.
| Bảng 23.1 Duy trì phạm vi mục tiêu SpO2 trong quá trình kiểm soát FiO2 vòng lặp kín và thủ công | |||
|
% Thời gian trong phạm vi mục tiêu |
|||
| Phạm vi mục tiêu SpO2 | Kiểm soát FiO2 thủ công | Kiểm soát FiO2 vòng lặp kín | |
| Bhutani, 1992 | 94%-96% | 54 | 81 |
| Morozoff, 1993 | 90%-95% | 39 | 50 |
| Claure, 2001 | 88%-96% | 66 | 75 |
| Urschitz, 2004 | 87%-96% | 82 | 91 |
| Claure, 2009 | 88%-95% | 42 | 58 |
| Morozoff, 2009 | 90%-96% | 57 | 73 |
| Claure, 2011 | 87%-93% | 39 | /47 |
| Waitz, 2014 | 88%-96% | 69 | 76 |
| Hallenberger, 2014 | Bốn trung tâm (90%-95%, 80%-92%, 83%-93%, 85%-94%) | 61 | 72 |
| Zapata, 2014 | 85%-93% | 34 | 58 |
| Lal, 2015 | 90%-95% | 60 | 69 |
| Van Kaam, 2015 | 89%-93% | 54 | 62 |
| 91%-95% | 58 | 62 | |
ªBao gồm các giai đoạn có SpO> phạm vi mục tiêu, trong khi FiOy = 21%.
Kỹ thuật thông khí cung cấp hỗ trợ theo tỷ lệ với nỗ lực của bệnh nhân
Thông khí hỗ trợ theo tỷ lệ
Bệnh phổi căn nguyên có thể gây ảnh hưởng khác nhau đến các đặc tính cơ học của hệ hô hấp ở trẻ sơ sinh. Các bệnh lý hạn chế như hội chứng suy hô hấp (respiratory distress syndrome – RDS) làm giảm độ giãn nở của phổi, dẫn đến tăng tải trọng đàn hồi lên bơm hô hấp của trẻ sơ sinh. Tình trạng tắc nghẽn làm tăng sức cản của đường thở và áp đặt tải trọng. Các tải trọng hô hấp này dẫn đến tầng nỗ lực thở cần thiết để duy trì thông khí. Khi nỗ lực không đủ, bệnh nhân bị giảm thông khí và suy hô hấp.
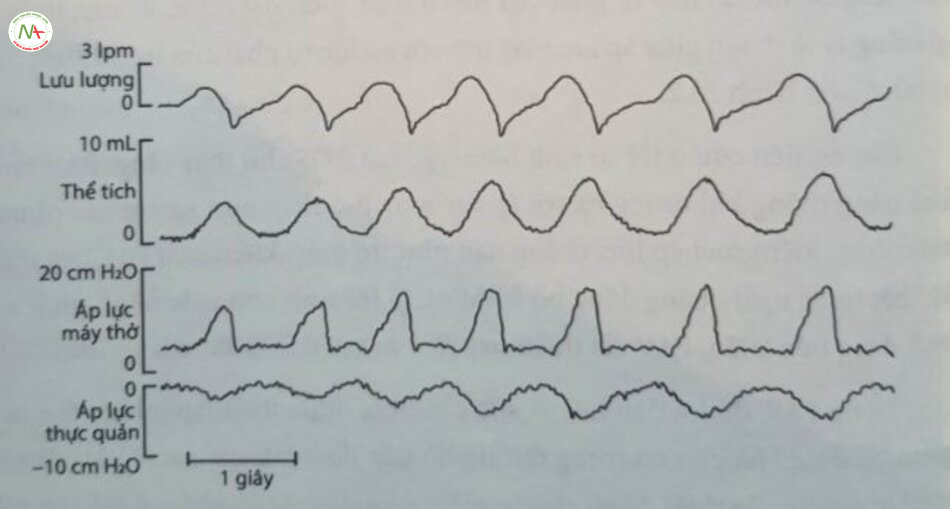
Thông khí hỗ trợ theo tỷ lệ (proportional assist ventilation – PAV) là phương thức mà tại đó, áp lực do máy thở tạo ra tặng tương ứng với thể tích, lưu lượng, hoặc cả hai, được tạo ra bởi nỗ lực hít vào của trẻ sơ sinh. Độ lợi tỷ lệ (proportional gain) mà áp lực dương tăng lên so với thể tích khí lưu thông đo được (VT) hoặc lưu lượng là độ lợi đàn hồi (tỷ lệ với thể tích, tính bằng đơn vị áp lực trên mililit thể tích đo), hoặc độ lợi sức cản (tỷ lệ lưu lượng, tính bằng đơn vị áp lực trên một đơn vị đo lưu lượng). Áp lực máy thở tăng đồng thời làm tăng nỗ lực hô hấp tự phát của trẻ sơ sinh, giúp đạt được Vị cần thiết. Sự gia tăng tỷ lệ thuận giữa áp lực máy thở với nỗ lực tự phát của trẻ sơ sinh được minh họa ở Hình 23.2.
Các nghiên cứu ở trẻ sơ sinh hồi phục sau RDS cho thấy rằng: PAV tạo ra khả năng thông khí tương tự với áp lực máy thở thấp hơn so với các phương thức được kiểm soát áp lực, chẳng hạn như trợ giúp kiểm soát (AC) và thông khí bắt buộc ngắt quãng đồng bộ (SIMV). Ở trẻ sinh non mắc bệnh phổi mãn tính đang tiến triển, PAV cải thiện oxy hóa so với AC kiểm soát áp lực.
Trong PAV, độ lợi đàn hồi và sức cản phải được thiết lập, nhằm tạo ra sự giảm tải đủ để bủ cho tải trọng đường hô hấp do bệnh gây ra. Độ lợi đàn hồi vượt quá mức cần thiết để bù cho sự giảm độ giãn nở của phổi có thể làm tăng áp lực quá mức. Độ lợi sức cản vượt quá mức cần thiết để vượt qua sức cản tăng lên của đường thở có thể gây ra dao động áp lực nhanh chóng. Để giảm thiếu nguy cơ tăng quá mức, bác sĩ lâm sàng phải cài đặt áp lực đỉnh và giới hạn VT phù hợp. Cần phải thừa nhận rằng, giả định cơ bản của PAV là trung khu hô hấp của bệnh nhân phù hợp, và thiết bị chỉ đơn thuần khắc phục tải cơ học do bệnh gây ra. Khi áp dụng cho trẻ sinh non với khả năng kiểm soát hô hấp chưa trưởng thành, khả năng sẽ xảy ra tình trạng giảm thông khí do ngưng thờ trung ương (central apnea), trừ phi cung cấp tần số dự phòng.
Cần hiểu rõ lý thuyết đằng sau việc giảm tải bằng PAV khi cài đặt độ lợi đàn hồi hoặc độ lợi sức cản. Khi độ giãn nở thay đổi, phải điều chỉnh độ lợi đàn hồi cho phù hợp để tránh VT quá mức; chấn thương thể tích cũng có thể xảy ra khi trẻ sơ sinh trở nên kích động và tạo ra VT quá lớn.
Tóm lại, dữ liệu được công bố chỉ ra rằng: PAV có hiệu quả ngắn hạn trong việc duy trì hệ thống thông khí tương đương với áp lực thấp hơn khi so với các chế độ kiểm soát áp lực thông thường. Cần có thêm các nghiên cứu chuyên sâu hơn, giúp xác định xem liệu ứng dụng lâu dài chiến lược này có thể có lợi cho việc giảm nhu cầu hỗ trợ thông khí và cải thiện kết cục hô hấp hay không. Sự phức tạp của phương thức này và tính khả dụng có hạn dường như đã hạn chế sự thâm nhập của nó vào thực hành lâm sàng. Theo văn bản này, chế độ hỗ trợ PAV chỉ dành riêng cho máy thở Stephanie (F. Stephan GmbH Medizintechnik, Gackenbach, Đức).
Hỗ trợ thông khí điều chỉnh theo tín hiệu thần kinh
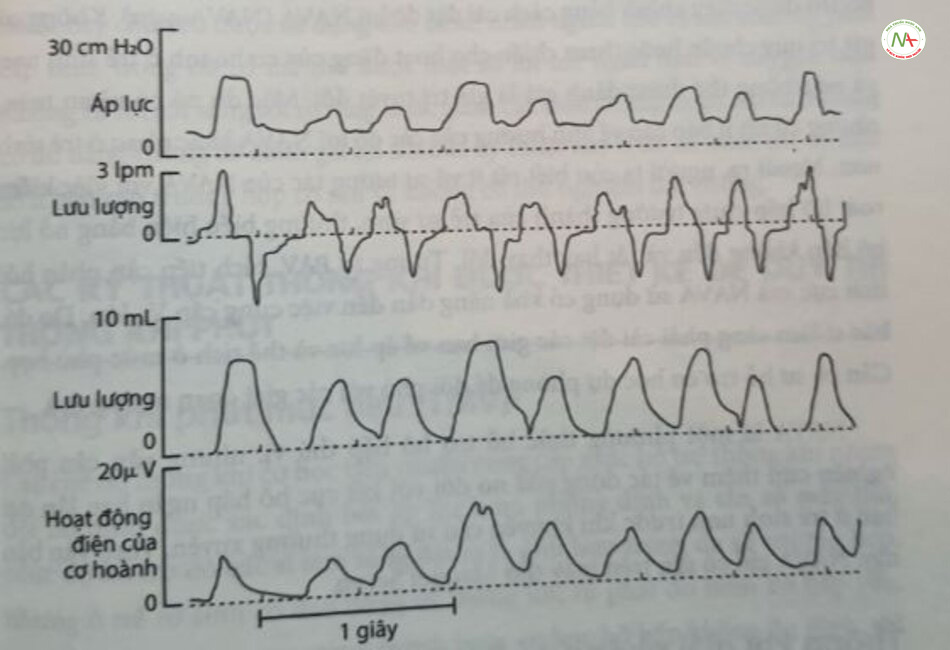
Hỗ trợ thông khí điều chỉnh theo tín hiệu thần kinh (neurally adjusted ventilatory assist – NAVA) là một phương thức mới mà tại đó, áp lực máy thở được điều chỉnh tương ứng với hoạt động điện của cơ hoành được đo bằng các điện cực thực quản gắn trên một ống cho ăn đã chỉnh sửa. Áp lực của máy thở trong NAVA tỷ lệ thuận với hoạt động của cơ hoành, trong đó hệ số tỷ lệ hoặc độ lợi do bác sĩ lâm sàng cài đặt (tính bằng đơn vị áp lực trên mỗi microvolt của hoạt động điện), được gọi là “mức NAVA” (“NAVA level”). Khi áp lực máy thở được tăng lên đồng thời và tỷ lệ thuận với sự gia tăng hoạt động điện của cơ hoành, NAVA có thể nâng cao khả năng tạo ra Vị lớn hơn của cơ hoành, hoặc duy trì VT tương tự với nỗ lực thở ít hơn. Sự gia tăng áp lực máy thở tương ứng với mức độ hoạt động của cơ hoành được minh họa ở Hình 23.3.
Các nghiên cứu ở trẻ sinh non nhận định: NAVA có hiệu quả trong việc đồng bộ áp lực dương với hít vào tự phát của trẻ sơ sinh. Các nghiên cứu này đã chứng minh rằng, NAVA duy trì sự thông khí và trao đổi khí tương tự hoặc tốt hơn, với áp lực đường thở thấp hơn so với phương thức thông khí kiểm soát áp lực. Tác động của NAVA đối với nỗ lực thở và áp lực máy thở liên quan đến các cài đặt cụ thể của áp lực hoặc thể tích mục tiêu được sử dụng theo phương thức thông thường. NAVA làm giảm hoạt động của cơ hoành so với phương thức thông khí kiểm soát áp lực, đồng thời cung cấp VT tương tự với áp lực đỉnh thấp hơn. Ngược lại, hoạt động của cơ hoành trong NAVA cao hơn so với thông khí mục tiêu thể tích (VTV), nhưng áp lực đường thở đỉnh và Vị nhỏ hơn. Trong một thử nghiệm ngẫu nhiên gần đây hơn bao gồm cả trẻ sinh non bị RDS, NAVA đã đạt được tỷ lệ cai máy thở tương đương với các chế độ kiểm soát áp lực.
Xử trí NAVA khác với các phương thức thông thường bởi vì trong NAVA, hỗ trợ được điều chỉnh bằng cách cài đặt độ lợi NAVA (NAVA gain). Không có giá trị quy chuẩn hoặc tham chiếu cho hoạt động của cơ hoành ở trẻ sinh non và nó không thể được đánh giá là giá trị tuyệt đối. Mặc dù nó có vẻ an toàn, nhưng có rất ít báo cáo về ảnh hưởng của các độ lợi NAVA khác nhau ở trẻ sinh non. Ngoài ra, người ta còn biết rất ít về sự tương tác của NAVA với việc kiểm soát hô hấp chưa trưởng thành của trẻ sơ sinh, thường biểu hiện bằng nỗ lực hô hấp không đều và rất hay thay đổi. Tương tự PAV, cách tiếp cận phản hồi tích cực mà NAVA sử dụng có khả năng dẫn đến việc cung cấp Vị lớn. Do đó, bác sĩ lâm sàng phải cài đặt các giới hạn về áp lực và thể tích ở mức phù hợp. Cần có sự hỗ trợ cơ học dự phòng để đối phó với các giai đoạn ngưng thở.
NAVA là một phương thức hỗ trợ hô hấp thú vị, nhưng vẫn cần phải nghiên cứu thêm về tác động của nó đối với kết cục hô hấp ngắn hạn lẫn dài hạn ở trẻ sinh non trước khi khuyến cáo sử dụng thường xuyên. Theo văn bản này, NAVA chỉ có sẵn trên máy thở Maquet Servo.
Thông khí giải phóng áp lực đường thở (APRV)
Thông khí giải phóng áp lực đường thở (airway pressure release ventilation – APRV) là phương thức được sử dụng chủ yếu ở người lớn bị suy hô hấp cấp tính, với vai trò là phương pháp thay thế giúp cải thiện quá trình oxygen hóa. APRV là phương thức mà tại đó, áp lực dương cao liên tục được áp dụng tại đường thở với giai đoạn giải phóng ngắt quãng. Trong APRV, áp lực dương mức cao hơn (Ph.) được dùng để duy trì thể tích phổi và huy động phế nang, còn giai đoạn giải phóng ngắn được kỳ vọng sẽ tạo ra thông khí. Tuy nhiên, phần lớn thông khí phút đến từ nỗ lực hô hấp tự phát của bệnh nhân trong quá trình sử dụng Phigh. Mô hình xen kẽ giữa áp lực thấp và cao này có thể được coi là quá trình hít vào cực đoan đối với thông khí tỷ lệ đảo ngược (inverse ratio ventilation) khi thở ra. Nó cũng có một số điểm tương đồng với các dạng khác nhau của áp lực đường thở dương hai mức áp lực (bilevel positive airway pressure – BiPAP), vì nó phụ thuộc vào hoạt động thở tự phát. APRV thường được sử dụng như một kỹ thuật cứu hộ (rescue), và khác với BiPAP, mức áp lực trên Phigh được duy trì trong phần lớn chu kỳ hô hấp (Th). Áp lực mà phổi được giải phóng được gọi là P… còn thời gian giải phóng được gọi là T… Kỳ Jow thuật này chủ yếu được sử dụng cho bệnh nhân người lớn bị tổn thương phối cấp tính, trong đó có thể thu được một số lợi ích ngắn hạn về oxygen hóa. Không có lợi ích sống sót rõ ràng hoặc giảm các biến chứng được chỉ ra. Không có đủ bằng chứng để đánh giá lợi ích của kỹ thuật này ở trẻ sơ sinh, chỉ có một số ít báo cáo trường hợp có sẵn và không có thử nghiệm đối chứng.
Các kỹ thuật thông khí được thiết kế để duy trì thông khí phút
Thông khí phút mục tiêu (TMV)
Các chế độ thông khí cơ học tiêu chuẩn cung cấp mức hỗ trợ thông khí tương đối ổn định được xác định bởi áp lực bơm phồng đỉnh và tần số máy thở. Mức độ hỗ trợ do bác sĩ lâm sàng đặt ra là phù hợp trong đa số trường hợp, nhưng ở trẻ sơ sinh có dao động vẽ thông khí tự phát do bơm hô hấp yếu, trung khu hô hấp chưa trưởng thành hoặc cơ học hô hấp không ổn định, thì hỗ trợ thông khí thường không đủ, ngược lại còn có thể vượt quá nhu cầu của trẻ. Lý do của thông khí phút mục tiêu (targeted minute ventilation – TMV) là tự động điều chỉnh tần số máy thở, nhằm duy trì sự thông khí và trao đổi khí ổn định hơn, cũng như giảm khả năng thông khí quá mức. Các phương thức của TMV dựa trên việc tự động điều chỉnh tần số bắt buộc, giúp duy trì thông khi phút ở mức tối thiểu hoặc trên mức tối thiểu. Khi nhịp thở tự phát đủ để duy trì thông khí phút trên mức này, thì tần số máy thở sẽ giảm, hoặc ngược lại. Các điều chỉnh liên tục đối với tần số máy thở trong quá trình TMV được thể hiện trong Hình 23.4.
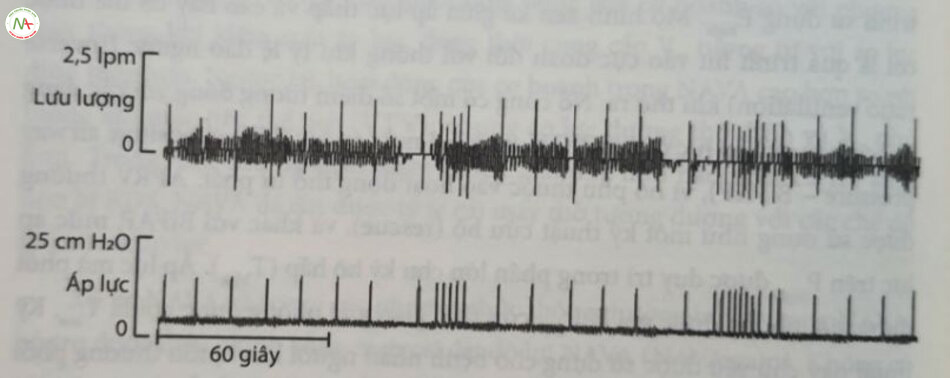
Ở trẻ sinh non hồi phục sau RDS, thông khí phút mục tiêu đạt được mức giảm 50% tần số thông khí bắt buộc ngắt quãng đồng bộ (SIMV) mà không ảnh hưởng đến trao đổi khí so với SIMV thông thường. Nghiên cứu này cho thấy rằng: Mặc dù trẻ sinh non có thể duy trì thông khí trong khoảng thời gian đáng kể, song trẻ thường có chu kỳ cẩn tần số máy thở cao hơn nhiều. Ở một nhóm nhỏ trẻ sơ sinh có các đợt giảm oxy máu tự phát thường xuyên, thông khí phút mục tiêu làm giảm các đợt giảm oxy máu so với SIMV. Kỹ thuật này phù hợp với những phát hiện của một nghiên cứu với mô hình động vật thi nghiệm về các đợt giảm oxy máu gây ra. Trong nghiên cứu này, kết hợp điều chỉnh tần số thở máy và áp lực bơm phồng đỉnh (PIP) để giữ thông khí phút và mục tiêu Vũ có hiệu quả hơn khi làm giảm các đợt giảm oxy máu so với tần số thở máy không đổi và PIP trong SIMV thông thường. Việc điều chỉnh tự động đồng thời tần số máy thở và PIP thậm chí còn hiệu quả hơn trong việc giảm mức độ nghiêm trọng của các đợt giảm oxy máu. Cần lưu ý rằng, kỹ thuật này có thể áp dụng riêng cho chế độ SIMV và chỉ được so sánh với SIMV. Không rõ liệu cách tiếp cận này có ưu việt hơn các phương thức thông khí đồng bộ khác, chẳng hạn như thông khí trợ giúp-kiểm soát và hỗ trợ áp lực như được thực hiện trên máy thở sơ sinh (chế độ trợ giúp mọi nhịp thở tự phát), hay SIMV với hỗ trợ áp lực hay không.
Thông khí phút bắt buộc (MMV)
Thông khí phút bắt buộc (mandatory minute ventilation – MMV) là một phương thức của TMV vốn dùng cho người trưởng thành và đã được điều chỉnh cho trẻ sơ sinh. Trong MMV, mục tiêu thông khí phút được duy trì bằng tích số của tần số máy thở không đổi và nhịp thở của thông khí nhắm mục tiêu thể tích (VTV). Khi thông khí phút vượt quá mức mục tiêu, nhịp thở của máy thở sẽ dừng lại. MMV thường được sử dụng kết hợp với hỗ trợ áp lực để trợ giúp mọi nhịp thở tự phát. Ở trẻ sinh non tháng muộn không bị bệnh phổi, MMV đạt được mức giảm tần số bắt buộc và áp lực đường thở trung bình so với SIMV mà không có thay đổi về trao đổi khí.
Thông khí dự phòng ngưng thở
Thông khí dự phòng ngưng thở (apnea backup ventilation) là phương thức có sẵn trong hầu hết máy thở sơ sinh. Nhịp thở tự phát thường được trợ giúp bởi hỗ trợ áp lực, nhưng trong trường hợp ngưng thở, máy thở bắt đầu tần số bơm phóng cơ học bắt buộc cài đặt trước. Mặc dù đã có sẵn trong hầu hết máy thở sơ sinh, nhưng lợi ích hoặc bất lợi của phương thức này vẫn chưa được đánh giá.
Thông khi dự phòng thích ứng
Thông khí dự phòng thích ứng (adaptive backup ventilation) là phương thức mà tại đó, một tần số bắt buộc được cung cấp trong thời gian ngưng thở hoặc trong các đợt giảm SpO, Ở trẻ sinh non đang hồi phục sau RDS, phương thức này làm giảm tần suất và mức độ nghiêm trọng của các đợt giảm oxy máu khi so với tần số bắt buộc dự phòng đối với ngưng thở đơn thuần.
Kết quả tổng hợp từ những nghiên cứu lâm sàng ngắn hạn đánh giá các phương thức khác nhau của TMV cho thấy rằng: Các phương thức này có thể phù hợp hơn với hỗ trợ cơ học, với các nhu cầu thở máy khác nhau của trẻ sinh non. Mặc dù những kết quả này đầy hứa hẹn, nhưng vẫn cần đánh giá lợi ích và hạn chế khả dĩ của các phương thức này trong các thử nghiệm lâm sàng dài hạn.
Thông khí hỗ trợ thích ứng (ASV)
Thông khí hỗ trợ thích ứng (adaptive support ventilation – ASV) là phương Đối với thức thông khi tự động được sử dụng ở bệnh nhân trẻ em và bệnh nhân người lớn. ASV cung cấp sự kết hợp của các điều chỉnh tần số hô hấp và V điều này, thuật toán ASV xác định tần số hô hấp dựa trên thể tích khoảng chết của bệnh nhân, thông khí phút mong muốn và hằng số thời gian hô hấp. VT được tính bằng cách lấy thông khí phút chia cho nhịp thở. Bác sĩ có thể điều chỉnh thông khí phút mục tiêu dựa vào tình trạng của bệnh nhân. Sau đó, ASV điều chỉnh áp lực đỉnh của máy thở để duy trì VT mục tiêu. Với tần số hô hấp đã cài đặt, VT và cơ học hô hấp được đánh giá lại trên từng nhịp thở. Trong các giai đoạn mà nhịp thở tự phát giảm, các nhịp bơm phồng bắt buộc được cung cấp để duy trì tần số mong muốn.
Bằng cách thích ứng tần số hô hấp phụ thuộc vào khoảng chết, cơ học hô hấp và trung khu hô hấp, ASV nhằm đến mục tiêu duy trì thông khí phút đầy đủ và tạo điều kiện thuận lợi cho việc cai máy thở. ASV đại diện cho một cách tiếp cận mới mẻ, tinh vi trong xử trí hỗ trợ thông khí ở bệnh nhân nhi lẫn người lớn. Tuy nhiên, tính đến thời điểm viết bài này, không có báo cáo nào để cập đến việc ứng dụng ASV ở trẻ sơ sinh.
Kết luận
Chương này đã thảo luận về nhiều kỹ thuật hỗ trợ hỗ hấp mới lạ, triển vọng và có thể giúp giải quyết một số hạn chế trong thở máy thông thường hoặc thở oxy. Mặc dù hầu hết các kỹ thuật mới này đều có sẵn hoặc có thể được ứng dụng trên lâm sàng trong tương lai gần, nhưng cần có thêm bằng chứng về tính an toàn và lợi ích của chúng ở trẻ sinh non trước khi ứng dụng rộng rãi hơn trên lâm sàng.