Bệnh hô hấp
Tăng thông khí trên bệnh nhân thở máy do chấn thương sọ não
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Biên dịch: BS. Đặng Thanh Tuấn – BV Nhi Đồng 1
Để tài file PDF của bài viết Tăng thông khí trên bệnh nhân thở máy do chấn thương sọ não xin vui lòng click vào link ở đây
Tăng thông khí là một liệu pháp thường được sử dụng để điều trị tăng áp lực nội sọ (ICHT, intracranial hypertension) ở bệnh nhân chấn thương sọ não (TBI, traumatic brain injury). Tăng thông khí thúc đẩy giảm CO2, gây co mạch trong các tiểu động mạch não và do đó làm giảm lưu lượng máu não và ở mức độ thấp hơn, thể tích máu não một cách hiệu quả, làm giảm áp lực nội sọ tạm thời. Tuy nhiên, tăng thông khí có thể gây ra các ảnh hưởng nghiêm trọng đến toàn thân và não, chẳng hạn như tổn thương phổi do máy thở hoặc thiếu máu cục bộ não. Do đó, việc sử dụng thường xuyên liệu pháp này không được khuyến khích. Ngược lại, trong những điều kiện cụ thể, chẳng hạn như ICHT kháng trị và sắp xảy ra thoát vị não, nó có thể là một liệu pháp cứu sống hiệu quả. Mục đích của tổng quan này là mô tả tác động của tăng thông khí lên các cơ quan ngoài não và huyết động hoặc chuyển hóa não, cũng như thảo luận về các tác dụng phụ và cách thực hiện để quản lý bệnh nhân TBI.
Giới thiệu
Tăng áp lực nội sọ (ICHT) là biến chứng nguy hiểm nhất và có khả năng tàn phá nặng nề nhất ở bệnh nhân chấn thương sọ não (TBI) (1). Vì hộp sọ là một ngăn cứng nên tổng thể tích của các chất nội sọ, tức là mô não, máu và dịch tủy sống, sẽ không đổi theo thời gian. Sự gia tăng thể tích của một trong những thành phần này ban đầu được bù đắp bởi sự dịch chuyển của các phần khác (tức là, sự chèn ép của hệ thống tĩnh mạch não có thể làm giảm thể tích máu não toàn cục; tái hấp thu dịch não tủy tăng và dịch chuyển dịch não tủy về phía bể chứa cơ bản và khoang cột sống có thể giảm thể tích CSF); khi các cơ chế này không còn có thể bù đắp cho những thay đổi về thể tích nữa, áp lực nội sọ (ICP) sẽ nhanh chóng tăng lên (2). Cả thời gian của ICHT và giá trị tối đa tuyệt đối của ICP đều có tác động đến kết quả của bệnh nhân (3); do đó, các liệu pháp nhằm mục đích kiểm soát ICP và giảm thiểu gánh nặng ICHT là nền tảng của quản lý TBI (4).
Mặc dù có các biện pháp can thiệp điều trị khác nhau, nhưng không có biện pháp nào cho thấy tác động đáng kể đến kết quả của bệnh nhân và một số tác dụng phụ tiềm ẩn có thể hạn chế việc sử dụng chúng. Việc điều chỉnh áp suất carbon dioxide trong động mạch (PaCO2) đã được sử dụng từ nhiều thập kỷ trong gây mê thần kinh và chăm sóc thần kinh, bởi vì giảm PaCO2 (tức là giảm CO2) thông qua tăng thông khí thể tích phút (tức là tăng thông khí) có thể góp phần nhanh chóng làm giảm thể tích của não phù lên và giúp kiểm soát ICP (5); những tác dụng này được thực hiện qua trung gian của co mạch não và giảm lưu lượng máu não (CBF) và thể tích máu não (CBV) (1, 2).
Mặc dù được sử dụng phổ biến, tăng thông khí không được hỗ trợ rộng rãi bởi bằng chứng chắc chắn, tác dụng của nó có thể thoáng qua và có thể không cải thiện xác suất phục hồi thần kinh (3). Hơn nữa, bằng cách giảm CBF, tăng thông khí có thể kích hoạt hoặc tăng cường thiếu máu cục bộ não (4, 5). Ngoài ra, tăng thông khí có một số tác động ngoài não có thể tác động tiêu cực đến kết quả của bệnh nhân (6). Do đó, nếu tăng thông khí thường xuyên được áp dụng ở bệnh nhân TBI (7), thì những rủi ro tiềm ẩn liên quan đến liệu pháp này đòi hỏi sự hiểu biết tối ưu về cách quản lý PaCO2 ở bệnh nhân TBI.
Mục đích của tổng quan này là mô tả tác động của tăng thông khí đối với sinh lý não và thảo luận về việc sử dụng nó trong việc quản lý bệnh nhân TBI. Chỉ các nghiên cứu tập trung vào tăng thông khí có kiểm soát (tức là điều chỉnh thông khí phút ở bệnh nhân TBI được điều trị bằng thở máy và các chế độ có kiểm soát) mới được đánh giá, còn tình trạng tăng thông khí trước khi nhập viện hoặc tăng thông khí tự phát sẽ không được thảo luận.
Tăng thông khí, giảm CO2 và các ảnh hưởng toàn thân
Tăng thông khí được đặc trưng bởi thông khí phế nang phút tăng cao, có thể là thứ phát sau tăng thể tích khí lưu thông và/hoặc tần số hô hấp, nếu khoảng chết không đổi. Tình trạng này thường được quan sát như một phản ứng sinh lý đối với tình trạng giảm oxy máu, viêm toàn thân, chấn thương ngực hoặc đau; tuy nhiên, trong thiết lập quản lý TBI, “tăng thông khí có kiểm soát” là sự điều chỉnh của thông khí phút để giảm CO2 (tức là PaCO2 <38 mmHg) để điều chỉnh huyết động não và độ giãn nở (8). Trong bối cảnh này, khoảng PaCO2 có thể chấp nhận được trong thực hành lâm sàng được coi là từ 35 đến 45 mmHg ở mực nước biển (8); khi tăng thông khí được áp dụng, nó có thể được xếp vào loại trung bình (PaCO2 31–35 mmHg), cưỡng bức (PaCO2 26–30 mmHg), hoặc tăng cường cưỡng bức (PaCO2 <26 mmHg), theo mức PaCO2 (9).
Có một số tác dụng ngoài não liên quan đến chiến lược điều trị này (Bảng 1); vì bệnh nhân TBI thường bị tổn thương phổi (7, 10, 11) do vi hít sặc, viêm phổi hoặc dập phổi (12), việc thúc đẩy tăng thông khí bằng cách tăng thể tích khí lưu thông có thể gây ra tổn thương phổi do máy thở (VILI) (13) và có khả năng trì hoãn chữa lành phổi hoặc kết quả xấu đi (14 – 16). Hơn nữa, tăng thông khí có thể làm tăng áp lực trong lồng ngực, gây rối loạn chức năng thất phải hoặc, ở những bệnh nhân giảm thể tích, gây suy giảm sự trở lại của tĩnh mạch và giảm cung lượng tim (17). Hơn nữa, giảm CO2 làm tổn hại đến lưu lượng máu mạch vành và có liên quan đến tăng nguy cơ thiếu máu cục bộ cơ tim (18) và phát triển loạn nhịp tim (19). Tăng thông khí kéo dài có liên quan đến nhiễm kiềm hô hấp (20); kiềm máu sẽ làm dịch chuyển đường cong phân ly oxy của hemoglobin sang trái, làm tăng ái lực của hemoglobin với oxy và ảnh hưởng đến việc cung cấp oxy ở mô (18). Giảm CO2 và nhiễm kiềm hô hấp cũng dẫn đến giãn mạch phổi (19) và co thắt phế quản (21), dẫn đến tình trạng không tương xứng thông khí và tưới máu (V/Q) và giảm oxy máu thứ phát ở bệnh nhân TBI có tổn thương phổi từ trước. Trong các nghiên cứu trên động vật, giảm CO2 cũng làm giảm sản xuất chất hoạt động bề mặt (22) và tăng tính thấm của hàng rào mao mạch phế nang (23), mặc dù điều này chưa được chứng minh rõ ràng ở người. Tăng thông khí cũng có thể làm tăng áp lực trong ổ bụng, thứ phát có thể làm tăng ICP (24); giảm CO2 làm giảm lưu lượng máu đến thận, các mô da và cơ, đồng thời làm tăng kết dính và kết tập tiểu cầu (12).
Bảng 1. Các tác dụng phụ tiềm ẩn liên quan đến tăng thông khí ở người
| Hệ thống | Não |
| Tổn thương phổi do thở máy Rối loạn chức năng thất phải Giảm cung lượng tim Thiếu máu cục bộ cơ tim Rối loạn nhịp tim Thiếu oxy mô Không tương xứng V/Q ở phổi Tăng áp lực trong ổ bụng Giảm lưu lượng máu thận Giảm lưu lượng máu da Giảm lưu lượng máu cơ bắp Tăng kết dính tiểu cầu Tăng kết tập tiểu cầu Hạ kali máu, hạ calci huyết và giảm phosphat máu |
Co mạch não CBF giảm CBV giảm Thiếu oxy não Tăng khả năng hưng phấn của tế bào thần kinh Giảm ngưỡng động kinh Tăng giải phóng các axit amin kích thích Tăng mức dopamine Thay đổi tổng hợp tế bào màng |
Ảnh hưởng của tăng thông khí và giảm CO2 trên sinh lý não và chuyển hóa
Cuối cùng, tăng thông khí thường liên quan đến rối loạn điện giải, chẳng hạn như hạ kali máu, hạ calci huyết và giảm phosphat máu (12). Tổng hợp lại, những phát hiện này cho thấy rằng tình trạng tăng thông khí có kiểm soát và giảm CO2 máu nên được áp dụng hết sức thận trọng cho tất cả các bệnh nhân bị bệnh nặng, vì có một số tác động tiêu cực đến các cơ quan đích.
Bộ não có nhu cầu năng lượng cao, chịu trách nhiệm về 20% tổng lượng oxy tiêu thụ của cơ thể (25). Vì não không có khả năng dự trữ năng lượng, nên việc điều chỉnh nhanh CBF là điều cần thiết để duy trì nguồn cung cấp đầy đủ oxy và chất dinh dưỡng cho mô não (26). Một số cơ chế, được gọi chung là “cơ chế tự điều chỉnh của não”, có hiệu quả để giữ cho CBF ở các giá trị cần thiết để đáp ứng nhu cầu năng lượng của não (26). Do đó, CBF là không đồng nhất và thay đổi tùy theo hoạt động trao đổi chất của từng vùng não (27); Các tiểu động mạch sức đề kháng co lại và giãn ra để điều chỉnh CBF để đáp ứng với các kích thích khác nhau, chẳng hạn như huyết áp, độ nhớt của máu, áp suất xuyên màng não, nhu cầu trao đổi chất, pH mô, và chất điện giải hoặc PaCO2 (28).
Đặc biệt, các tiểu động mạch đề kháng này phản ứng với sự thay đổi của PaCO2 từ 20 đến 60 mmHg bằng cách co lại (tức là giảm CO2) hoặc giãn ra (tức là tăng CO2) (2), một hiện tượng được gọi là “đáp ứng CO2 trong mạch máu não”. Đáp ứng này đối với các biến thể PaCO2 có lẽ là qua trung gian pH (18) (nghĩa là pH thấp hoặc nồng độ H+ cao sẽ thúc đẩy giãn mạch, trong khi pH cao và H+ thấp gây co mạch), và tỷ lệ thuận với tăng CO2 máu hơn là giảm CO2 (29). Khoảng 70% CBV nằm trong hệ thống tĩnh mạch và không bị ảnh hưởng bởi những thay đổi trong PaCO2; do đó, những thay đổi trong CBV sau tăng thông khí bị hạn chế ở thành phần động mạch và có liên quan đến giảm CBF (18). Đặc biệt, đối với mỗi mmHg giảm PaCO2, có sự giảm khoảng 3% trong CBF (2), mặc dù tác động của tình trạng giảm CO2 trên ICP ít rõ rệt hơn (5).
Tăng thông khí cũng có thể dẫn đến thiếu oxy não (Bảng 1). Cơ chế chính được đề xuất là giảm cung cấp oxy do giảm tưới máu toàn cục và/hoặc khu vực do giảm CBF (30, 31). Hơn nữa, do các tác động toàn thân nêu trên, giảm CO2 máu có thể dẫn đến VILI bổ sung, làm suy giảm trao đổi khí và giảm oxy máu, và có thể làm thay đổi đường cong phân ly oxy hemoglobin, làm giảm cung cấp oxy (18).
Cuối cùng, tình trạng kiềm máu và giảm CO2 máu làm tăng tính hưng phấn của tế bào thần kinh (32), giảm ngưỡng động kinh và/hoặc kéo dài các hoạt động co giật (33). Trong các nghiên cứu trên động vật, tình trạng giảm canxi dẫn đến tăng tiêu thụ ở não và làm cạn kiệt glucose cục bộ (34, 35). Giảm CO2 cũng có liên quan đến nhiễm độc thần kinh (12), bằng cách gây ra sự giải phóng axit amin kích thích gây độc tế bào (36), làm tăng mức dopamine trong hạch nền (37) và bằng cách thúc đẩy sự kết hợp không thích hợp của choline vào phospholipid của màng tế bào (38).
Tăng thông khí có kiểm soát ở bệnh nhân TBI
Tăng thông khí đã được báo cáo để kiểm soát hiệu quả ICHT ở bệnh nhân TBI (39, 40); trong Bảng 2, một bản tóm tắt của hầu hết các nghiên cứu có liên quan báo cáo dữ liệu về tình trạng giảm CO2 máu, ICP và kết cục ở nhóm bệnh nhân này đã được cung cấp.
Obrist và cộng sự cho thấy rằng tăng thông khí có thể làm giảm nhanh chóng ICP ở một nửa số bệnh nhân TBI, mặc dù điều này có liên quan đến việc giảm CBF ở hầu hết tất cả họ (4). Mối quan hệ giữa PaCO2 và ICP không phải là tuyến tính và những ảnh hưởng quan trọng nhất được quan sát thấy giữa các giá trị PaCO2 là 30 và 50 mmHg (52). Hơn nữa, tăng thông khí kéo dài (53) sẽ liên quan đến việc giảm dần tác dụng co mạch của nó, vì sự bình thường hóa quanh mạch của pH do đệm cục bộ. Do CBF giảm (tức là thiểu năng lượng máu) thường được quan sát thấy trong giai đoạn đầu sau khi mắc bệnh TBI (54), không nên bắt đầu giảm thông khí kéo dài ở những bệnh nhân này mà không theo dõi CBF. Lưu lượng máu não có thể được đo trực tiếp bằng cách sử dụng chụp cắt lớp vi tính Xenon (CT), chụp CT tưới máu (CTP) hoặc chụp cắt lớp phát xạ positron (PET), nhưng các kỹ thuật này liên quan đến việc tiêm chất đánh dấu phóng xạ hoặc phương tiện tương phản và yêu cầu vận chuyển của bệnh nhân, điều này không phải lúc nào cũng khả thi trong các trường hợp TBI nặng với ICHT (55). Đánh giá vận tốc CBF gián tiếp sử dụng siêu âm Doppler xuyên sọ (TCD) không tương ứng trực tiếp với các giá trị CBF tuyệt đối (56), mặc dù chỉ số mạch đập tăng (PI > 1,2), vận tốc tâm trương ở động mạch não giữa thấp (<20 cm/s) và ICP ước tính sử dụng các công thức đã được kiểm chứng có thể hữu ích để xác định bệnh nhân TBI có nguy cơ giảm tưới máu. Các nghiên cứu khác nhau đã chỉ ra sự giảm mức CBF trong quá trình giảm thông khí (5, 57 – 59); Ngoài ra, mức giảm CBF có liên quan nhất đã được quan sát thấy ở các khu vực quanh vết mổ, những nơi dễ bị tổn thương thứ cấp hơn (59).
Bảng 2. Danh sách các nghiên cứu lâm sàng liên quan nhất về vấn đề tăng thông khí có kiểm soát ở bệnh nhân chấn thương sọ não (TBI).
Nếu mức giảm CBF khá nhất quán, thì việc tăng thông khí có kiểm soát (tức là PaCO2 trung bình từ 37 đến 30 mmHg) có thể cải thiện các chỉ số của chức năng tự điều tiết não ở bệnh nhân TBI bị rối loạn phản ứng với áp suất lúc ban đầu, trong khi những người có phản ứng áp suất nguyên vẹn lúc ban đầu sẽ không có tác dụng của sự can thiệp như vậy (60). Một nghiên cứu thuần tập lớn khác cũng chỉ ra rằng giảm thông khí nhẹ có liên quan đến chỉ số phản ứng áp suất thấp hơn (tức là chức năng tự điều hòa tốt hơn), đặc biệt là vào ngày thứ 2 sau chấn thương (61). Một giả thuyết được đặt ra là tình trạng giảm CO2 và co mạch liên quan có thể thiết lập lại phản ứng nội mô trong các mạch máu não, vốn đã bị giãn ra trước đó để bù đắp lượng oxy cung cấp đến não bị giảm khi có ICHT.
Tuy nhiên, nếu quan sát thấy giảm CBF trong quá trình tăng thông khí, vẫn chưa rõ liệu hiện tượng này có liên quan đến các dấu hiệu tổn thương tế bào thiếu oxy và chuyển hóa kỵ khí hay không. Ở những bệnh nhân TBI nặng, Diringer et al. (62) quan sát thấy rằng tăng thông khí ngắn và trung bình làm giảm đáng kể CBF nhưng không làm giảm chuyển hóa não toàn cục và trích xuất oxy. Do đó, việc sử dụng theo dõi thần kinh, đặc biệt là quá trình oxy hóa não và/hoặc chuyển hóa, có thể cung cấp những phát hiện quan trọng về khả năng chịu đựng của não đối với tình trạng tăng thông khí có kiểm soát. Tăng thông khí cưỡng bức có liên quan đến giảm oxy trong não, được đo bằng phương pháp đo độ bão hòa oxy xoang cảnh (SjO2 nghĩa là ngưỡng thiếu oxy não là < 55%), mặc dù các kết quả này không nhất quán trong tất cả các nghiên cứu (63 – 65). Tuy nhiên, SjO2 phản ánh tình trạng oxy hóa toàn cục ở bán cầu và tình trạng thiếu oxy mô có thể xảy ra ngay cả trong các giá trị SjO2 bình thường (66). Áp lực oxy mô não (PbtO2) là một kỹ thuật khu vực, có tương quan tốt với CBF cục bộ và có thể theo dõi trực tiếp các khu vực có nguy cơ thiếu máu cục bộ thứ phát cao hơn (67). Tác động của tăng thông khí đối với PbtO2 là khác nhau, với một số nghiên cứu báo cáo sự giảm đáng kể oxy hóa não (68 – 71) trong khi những người khác không có thay đổi lớn (72, 73) và một số báo cáo sự gia tăng PbtO2, đặc biệt là do ICP giảm nhiều với tình trạng giãn mạch não trước đó (tức là tăng sung huyết) (45, 74). Các nghiên cứu gần đây báo cáo giá trị PbtO2 không thay đổi ở bệnh nhân TBI nặng người lớn trải qua tăng thông khí trung bình và với giá trị PbtO2 trung bình tại thời điểm ban đầu nằm trong giá trị bình thường (tức là > 30 mmHg) (39, 40).
Chức năng chuyển hóa của não có thể được đánh giá tại giường bệnh bằng kỹ thuật vi thẩm tách (microdialysis), hoặc thực hiện các nghiên cứu quang phổ chụp PET và cộng hưởng từ (MRI). Trong một nghiên cứu, tăng thông khí sớm (tức là 24–36 giờ sau khi bị thương) có liên quan đến sự gia tăng đáng kể tỷ lệ lactate mô và lactate/pyruvate, cho thấy chuyển hóa kỵ khí và thiếu oxy mô (46); những tác động chuyển hóa này ít rõ rệt hơn ở giai đoạn muộn (tức là 3–4 ngày sau TBI). Tuy nhiên, hai nghiên cứu gần đây cho thấy không có tác dụng tăng thông khí vừa phải trên các chất chuyển hóa ở não ở bệnh nhân TBI người lớn (39, 40). Sử dụng quét PET, một nghiên cứu (n= 9) cho thấy rằng tăng thông khí vừa phải và cường độ cao dẫn đến giảm CBF và tăng quá trình trích xuất oxy, nhưng chuyển hóa oxy liên tục (tức là không bị suy giảm năng lượng) (44). Trong hai nghiên cứu lớn hơn (43, 75), tăng thông khí (tức là, PaCO2 <30 mmHg) làm tăng thể tích vùng não giảm tưới máu trong não bị tổn thương, điều này, trong trường hợp không tăng cường trích xuất oxy, sẽ dẫn đến tình trạng thiếu oxy ở mô.
Với tất cả những tác dụng phụ tiềm ẩn này, tác dụng của tăng thông khí có kiểm soát đối với kết quả của bệnh nhân TBI là gì? Trong một nghiên cứu hồi cứu lớn (n = 251), Gordon et al. (76) báo cáo tỷ lệ tử vong thấp hơn ở bệnh nhân TBI trải qua quá trình tăng thông khí (tức là PaCO2 từ 25 đến 30 mmHg trong 6 đến 41 ngày); tuy nhiên, những di chứng thần kinh nghiêm trọng hơn đã được quan sát thấy ở những người sống sót trong nhóm tăng thông khí khi so sánh với nhóm còn lại. Chỉ có một thử nghiệm lâm sàng ngẫu nhiên tiền cứu đã nghiên cứu tác động của tăng thông khí trong bối cảnh này; Muizelaar và cộng sự (41) so sánh kết quả thần kinh 3 và 6 tháng của những bệnh nhân được giữ ở mức PaCO2 trung bình 25 mmHg đối với những người giữ ở mức trung bình 35 mmHg trong 5 ngày: tăng thông khí cưỡng bức có liên quan đến tỷ lệ bệnh nhân có kết cục kém cao hơn. Điều thú vị là trong số những bệnh nhân được điều trị bằng tăng thông khí có kiểm soát và tromethamine (THAM, tức là một chất đệm ngăn cản sự thay đổi pH trong dịch não ngoại bào và co mạch quá mức), có một tỷ lệ cao hơn những bệnh nhân có kết cục thần kinh thuận lợi lâu dài khi so sánh với khác.
Thảo luận: Một cách tiếp cận thực tế
Mục tiêu PaCO2 ban đầu ở bệnh nhân TBI có giá trị ICP bình thường đang thở máy phải nằm trong giá trị bình thường (tức là 38–42 mmHg— Hình 1); mặc dù các hướng dẫn của Tổ chức Chấn thương Não không thể xác định được ngưỡng tối ưu cho các giá trị PaCO2 trong giai đoạn đầu của quản lý TBI [(66), sự đồng thuận quốc tế khuyến nghị cho các giá trị “sinh lý” này vì tình trạng thiếu ôxy máu thường xuyên xảy ra trong 24-48 giờ đầu tiên sau khi bị thương và có thể trở nên trầm trọng hơn do tình trạng giảm CO2 máu (49, 50). Dự phòng (tức là trong trường hợp không có ICHT) và tăng thông khí kéo dài không được khuyến cáo và không nên sử dụng, (61) vì nó sẽ không mang lại lợi ích và có thể dẫn đến tình trạng thiếu oxy mô và rối loạn chuyển hóa não. Để phát hiện thiếu máu não ở những bệnh nhân này, chụp CTP ban đầu có thể hữu ích để xác định giá trị CBF rất thấp, dẫn đến thiếu máu cục bộ thứ phát trong trường hợp PaCO2 giảm xuống dưới giá trị sinh lý. Trong trường hợp không có CTP, siêu âm não, sử dụng kết hợp PI, ICP ước tính và vận tốc CBF tâm trương, có thể xác định bệnh nhân có nguy cơ giảm tưới máu não. Trong giai đoạn này, cần chú ý theo dõi chặt chẽ các phân tích khí, yêu cầu lấy mẫu lặp lại và theo dõi CO2 (etCO2) cuối triều, vì tăng thông khí trong trường hợp không có ICP tăng cao thường thấy ở bệnh nhân TBI người lớn (61). Điều quan trọng là etCO2 có thể có một số hạn chế trong trường hợp đồng thời có chấn thương ngực nặng và huyết động không ổn định (tức là cung lượng tim thấp) (77). Việc nhắm mục tiêu các giá trị PaCO2 hoặc pH bình thường có phải là cách tiếp cận thích hợp nhất hay không vẫn chưa được biết ở những bệnh nhân này. Tuy nhiên, do pH quanh mạch não có thể bị ảnh hưởng bởi các yếu tố khác ngoài PaCO2 và pH toàn thân (tức là chuyển hóa tại chỗ, K+, tình trạng thiếu oxy não biệt lập) và do đó ít được dự đoán chính xác hơn, sử dụng mức PaCO2 và định lượng các thay đổi về huyết động và sinh lý não đến PaCO2 các thay đổi tại giường bệnh khả thi hơn đối với các thầy thuốc. Nếu ICP vẫn nằm trong giá trị chấp nhận được sau 48 giờ kể từ khi bị tổn thương (tức là < 15 mmHg), các giá trị PaCO2 thấp hơn (tức là 33– 36 mmHg) có thể dẫn đến cải thiện quá trình tự điều hòa não (66), tuy nhiên, rất khó để khuyến nghị phương pháp này thường quy ở tất cả bệnh nhân TBI nặng.
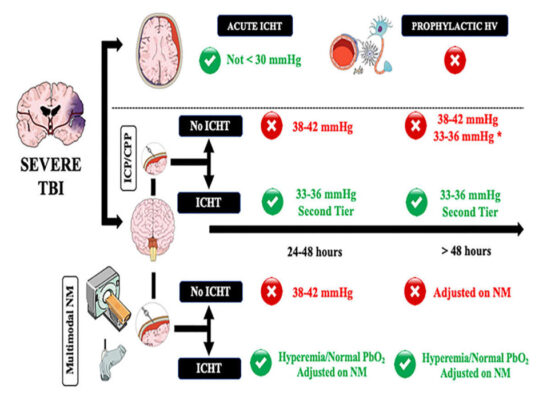
Hình 1: Một cách tiếp cận thực tế về cách quản lý tình trạng tăng thông khí có kiểm soát và tình trạng giảm CO2 máu ở bệnh nhân chấn thương sọ não (TBI). Tăng huyết áp nội sọ cấp tính (ICHT) = tăng ICP đe dọa tính mạng, đặc biệt khi có các dấu hiệu thoát vị (tức là giãn đồng tử, ngừng thở, tăng huyết áp, nhịp tim chậm). ICHT, áp lực nội sọ gần đến ngưỡng tới hạn để điều trị mà không có dấu hiệu thoát vị; HV, tăng thông khí có kiểm soát và giảm CO2. Vòng tròn màu xanh lá cây và màu đỏ đề cập đến khả năng sử dụng (màu xanh lá cây) hoặc chống chỉ định (màu đỏ) đối với việc sử dụng HV. NM, giám sát thần kinh. * Trường hợp chấn thương sọ não lan tỏa nhưng tiềm ẩn nguy cơ thiếu oxy mô cao. ** Điều chỉnh trên giám sát thần kinh
Bệnh nhân TBI có nguy cơ suy giảm khả năng tự điều hòa não cao nhất là những người bị tổn thương não lan tỏa (51); do đó, nếu đánh giá TCD cho thấy vận tốc CBF bình thường ở những bệnh nhân này, các giá trị PaCO2 thấp hơn (nghĩa là 33–36 mmHg) có thể được dung nạp, mặc dù theo dõi thần kinh toàn diện hơn sẽ là giải pháp hiệu quả duy nhất để phát hiện khả năng xảy ra tình trạng thiếu oxy mô. Vì tăng thông khí kết hợp với giảm CO2 là phương pháp hiện có nhanh nhất để giảm ICP, nên tăng thông khí vừa phải và ngắn nên được sử dụng để điều trị tăng ICP đe dọa tính mạng, đặc biệt khi có dấu hiệu thoát vị (tức là giãn đồng tử, ngừng thở, tăng huyết áp, nhịp tim chậm) (61) và có thể được sử dụng như một cầu nối đối với các can thiệp bổ sung (tức là, chụp CT-scan lặp lại; liệu pháp thẩm thấu; phẫu thuật). Trong bối cảnh này, tăng thông khí phải trong thời gian ngắn và, nếu có thể, không bao giờ được giảm xuống dưới trị số PaCO2 là 30 mmHg vì: (a) các tác dụng quan trọng nhất của PaCO2 trên ICP được quan sát thấy từ 30 đến 50 mmHg và (b) hầu hết các tác dụng phụ liên quan đến não được báo cáo đối với tăng thông khí cưỡng bức. Nếu có thể, nên giảm thiểu việc sử dụng tăng thông khí cho những bệnh nhân này trong 24 giờ đầu tiên sau khi bị chấn thương, khi CBF thường giảm nhiều nhất (61), trừ khi có thể đo được CBF.
Ở những bệnh nhân có giá trị ICP duy trì gần với ngưỡng tới hạn cho điều trị (tức là 20–22 mmHg), các hướng dẫn quốc tế khuyến cáo chỉ sử dụng tăng thông khí có kiểm soát như liệu pháp “bậc 2”, sau khi thất bại trong việc tăng cường an thần và truyền dịch thẩm thấu (78); thực sự, tăng thông khí có kiểm soát tạo ra tác dụng tương tự trên ICP nhưng rối loạn chuyển hóa của chuyển hóa não nhiều hơn mannitol ở bệnh nhân TBI (61). Ở những bệnh nhân này, nên đặt PaCO2 khoảng 33–36 mmHg và tránh các giá trị < 30 mmHg (49). Trong trường hợp không có các giám sát thần kinh khác ngoài ICP và áp lực tưới máu não (CPP), chụp CTP và TCD rất hữu ích để gợi ý các giá trị CBF bình thường hoặc cao (tức là tăng sung huyết), những giá trị này sẽ đáp ứng một cách hợp lý với tăng thông khí. Tuy nhiên, trong trường hợp giảm CO2 máu, các bác sĩ có thể quyết định tránh giảm CO2 máu và chuyển sang liệu pháp “bậc 3”, chẳng hạn như barbiturat, hạ thân nhiệt hoặc phẫu thuật mở hộp sọ, để điều trị ICHT vì giảm CO2 máu sẽ dẫn đến giảm tưới máu não bổ sung.
Theo chúng tôi, theo dõi thần kinh xâm lấn cũng nên được xem xét ở bệnh nhân TBI nặng và ICHT để tối ưu hóa việc quản lý tổng thể và đặc biệt, để đánh giá tác động của giá trị PaCO2 thấp đối với quá trình oxy hóa não và chuyển hóa. Do đó, các giá trị PaCO2 và tăng thông khí có thể được điều chỉnh theo khả năng dung nạp của não và các mục tiêu điều trị được cá nhân hóa theo nhu cầu của bệnh nhân. Trong trường hợp cần trị số PaCO2 thấp và đồng thời chấn thương phổi, các can thiệp khác nhằm mục đích giảm sản xuất CO2, chẳng hạn như tăng cường an thần hoặc hạ thân nhiệt, có thể được xem xét để gây giảm CO2 và tránh căng thẳng phổi và VILI. Tuy nhiên, chiến lược này cần được đánh giá thêm trong các nghiên cứu lâm sàng.
Nếu giá trị PaCO2 được kiểm soát là bắt buộc ở bệnh nhân TBI nặng vì ảnh hưởng đáng kể đến huyết động học của não và sự độ giãn nở, liều cao của thuốc an thần, thường kết hợp với các thuốc ngăn chặn thần kinh cơ (NMBA), được yêu cầu để điều chỉnh các thông số thở để đạt được các mục tiêu PaCO2 mong muốn. Do đó, trong trường hợp không có các liệu pháp điều trị tích cực cho ICHT, vẫn chưa biết khi nào thì có thể an toàn để ngừng thuốc an thần và cuối cùng có thể chịu được tình trạng tăng thông khí tự phát ở những bệnh nhân này. Nếu điều này xảy ra sau vài ngày (tức là> 7–10 ngày) kể từ khi bị chấn thương, nguy cơ bị kém tuối máu có thể sẽ được hạn chế. Ngoài ra, tăng thông khí tự phát sau chấn thương não cấp tính thường được kích hoạt bởi nhiễm toàn cục bộ (nghĩa là, pH thấp xung quanh trung tâm hô hấp nằm trong thân não), dẫn đến giãn mạch và có thể bù đắp do co mạch do tăng thông khí. Trong những trường hợp này, việc theo dõi không xâm lấn (tức là TCD) và xâm lấn (tức là PbtO2) một lần nữa sẽ hữu ích để cá nhân hóa các quyết định điều trị.
Kết luận, tăng thông khí có kiểm soát có hiệu quả trong việc giảm ICP nhưng nó cũng làm giảm CBF và có thể có các tác dụng phụ nghiêm trọng về não và toàn thân. Do đó, các giá trị PaCO2 bình thường nên được duy trì trong giai đoạn đầu sau khi thực hiện TBI nếu ICP vẫn nằm trong các giá trị chấp nhận được. Tăng thông khí có kiểm soát (tức là không bao giờ PaCO2 dưới 30 mmHg) nên được sử dụng như một can thiệp cứu sống tạm thời trong trường hợp tăng áp nội sọ nặng; Mức độ PaCO2 cũng nên được điều chỉnh và cá nhân hóa ở từng bệnh nhân bằng cách sử dụng CTP và siêu âm não, theo dõi thần kinh đa phương thức nâng cao, bất cứ khi nào có thể.