Chưa có sản phẩm trong giỏ hàng.
Tucatinib

Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
6-N-(4,4-dimethyl-5H-1,3-oxazol-2-yl)-4-N-[3-methyl-4-([1,2,4]triazolo[1,5-a]pyridin-7-yloxy)phenyl]quinazoline-4,6-diamine
Nhóm thuốc
Tucatinib thuộc nhóm nào? Thuốc chống ung thư
Mã ATC
L – Chất chống ung thư và điều hòa miễn dịch
L01 – Thuốc chống ung thư
L01E – Chất ức chế protein kinase
L01EH – Thuốc ức chế tyrosine kinase thụ thể yếu tố tăng trưởng biểu bì 2 (her2) ở người
L01EH03 – Tucatinib
Mã UNII
234248D0HH
Mã CAS
937263-43-9
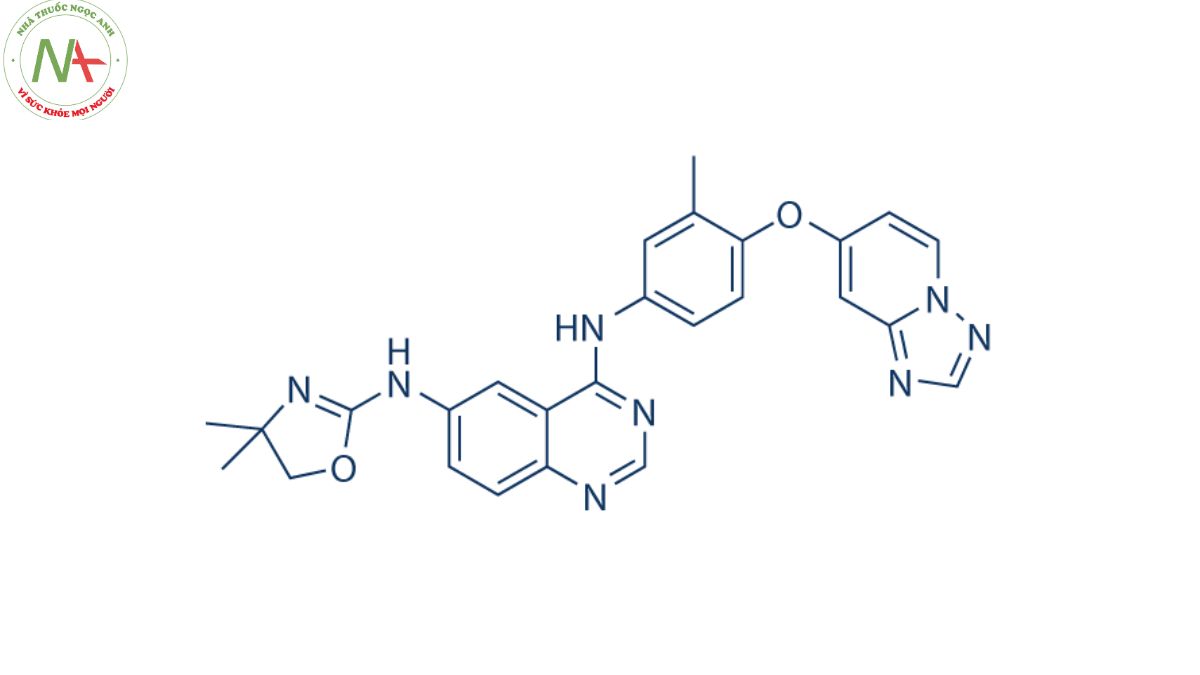
Cấu trúc phân tử
Công thức phân tử
C26H24N8O2
Phân tử lượng
480.5 g/mol
Cấu trúc phân tử
Các tính chất phân tử
Số liên kết hydro cho: 2
Số liên kết hydro nhận: 8
Số liên kết có thể xoay: 6
Diện tích bề mặt tôpô: 111Ų
Số lượng nguyên tử nặng: 36
Các tính chất đặc trưng
Điểm nóng chảy: 230°C
Tỷ trọng riêng: 1.4±0.1 g/cm3
Độ tan trong nước: 0.004 mg/mL
Hằng số phân ly pKa: 4.57
Chu kì bán hủy: 5,38 giờ
Khả năng liên kết với Protein huyết tương: 97%
Dạng bào chế
Viên nén: Tucatinib 50 mg, Tucatinib 150 mg

Độ ổn định và điều kiện bảo quản
Bảo quản thuốc ở nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp và nhiệt độ cao.
Đóng chặt nắp hộp thuốc sau khi sử dụng và không để thuốc tiếp xúc với không khí.
Không sử dụng thuốc quá hạn sử dụng hoặc có dấu hiệu biến đổi màu sắc, hình dạng hoặc mùi.
Nguồn gốc
Tucatinib là thuốc gì? Tucatinib, một loại thuốc ức chế kinase, hiện đang được áp dụng kết hợp với trastuzumab và capecitabine trong quá trình chăm sóc bệnh nhân mắc ung thư vú dương tính với HER-2 không thể phẫu thuật hoặc đã di căn. Được phát triển bởi Seattle Genetics và nhận được sự chấp thuận của FDA vào ngày 17 tháng 4 năm 2020, Tucatinib đại diện cho một tiến bộ quan trọng trong lĩnh vực điều trị ung thư vú. Đối với những bệnh nhân không phản ứng đầy đủ với các phác đồ hóa trị trước đây, phương pháp điều trị này mang lại hy vọng mới và đầy hứa hẹn.
Dược lý và cơ chế hoạt động
Tucatinib có tác dụng gì? Bằng cách ức chế enzyme tyrosine kinase, tucatinib không chỉ có tác dụng chống khối u mà còn giảm kích thước khối u trong quá trình điều trị ung thư vú dương tính với HER-2. Trong các thử nghiệm lâm sàng, sự kết hợp của tucatinib và trastuzumab đã thể hiện một hiệu suất tăng cường cả in vitro và in vivo so với việc sử dụng từng loại thuốc một cách độc lập.
Đột biến ở gen HER-2 thường được quan sát thấy trong nhiều loại ung thư biểu mô vú, và tucatinib đặc biệt ức chế enzyme tyrosine kinase của gen này. Sự đột biến của tyrosine kinase trong gen HER-2 thường dẫn đến tăng cường tín hiệu và sự tăng sinh tế bào, từ đó góp phần vào sự phát triển của bệnh ác tính.
Nghiên cứu in vitro đã chỉ ra rằng tucatinib không chỉ ức chế quá trình phosphoryl hóa của HER-2 mà còn của HER-3, tạo ra những thay đổi quan trọng trong tín hiệu MAPK và AKT cũng như sự tăng sinh tế bào. Hiệu quả chống khối u của tucatinib được chứng minh đặc biệt ở các tế bào biểu hiện HER-2. Trong môi trường in vivo, tucatinib tiếp tục thể hiện khả năng ức chế hiệu quả đối với sự phát triển của các khối u biểu hiện HER-2, có thể thông qua cơ chế tương tự.
Ứng dụng trong y học
Tucatinib chỉ định là để kết hợp với trastuzumab và capecitabine trong quá trình điều trị ung thư vú HER2 dương tính ở người lớn, đặc biệt là khi bệnh đã tiến triển không thể cắt bỏ hoặc đã di căn. Phạm vi của điều này mở rộng đến những bệnh nhân mắc bệnh ung thư vú HER2 dương tính với di căn não và những người đã trải qua một hoặc nhiều phác đồ điều trị dựa trên thuốc kháng HER2 trước đó, trong ngữ cảnh của tình trạng di căn.
Ngoài ra, tucatinib cũng được chỉ định để kết hợp với trastuzumab trong việc điều trị ung thư đại trực tràng di căn ở bệnh nhân trưởng thành hoặc không thể cắt bỏ, đặc biệt là trong trường hợp ung thư HER2 dương tính với RAS đã tiến triển sau khi đã được điều trị bằng hóa trị liệu dựa trên fluoropyrimidine-, oxaliplatin- và irinotecan. Lưu ý rằng chỉ dẫn này đã được phê duyệt theo quy trình phê duyệt nhanh, đồng nghĩa với việc nó đang chờ xác nhận và mô tả lợi ích lâm sàng chính xác thông qua các thử nghiệm xác nhận.
Dược động học
Hấp thu
Thời điểm đạt đỉnh hấp thụ (Tmax) của tucatinib biến động từ 1 đến 4 giờ. Kết quả từ một nghiên cứu dược động học cho thấy giá trị Cmax là 1120 ng/mL sau khi sử dụng liều 350 mg, hai lần mỗi ngày, với khoảng thời gian Tmax dao động từ 1 đến 3 giờ. Diện tích dưới đường cong (AUC) được báo cáo là khoảng 7120 giờ×ng/mL.
Phân bố
Thể tích phân bố của tucatinib là khoảng 1670 L, và thuốc này có khả năng xâm nhập vào não qua hàng rào máu não. Đặc biệt, tucatinib liên kết với protein huyết tương khoảng 97%.
Chuyển hóa
Quá trình chuyển hóa của tucatinib chủ yếu diễn ra thông qua enzyme CYP2C8, với sự đóng góp nhỏ từ CYP3A.
Thải trừ
Trong một nghiên cứu về tucatinib sử dụng đánh dấu bằng phóng xạ, khoảng 86% tổng liều được đào thải qua phân, trong khi 4,1% được phát hiện trong nước tiểu. Khoảng 16% liều tucatinib trong phân được xác định là dạng không biến đổi của thuốc. Độ thanh thải toàn bộ là 148 L/h. Theo một nghiên cứu dược động học, thời gian bán hủy của tucatinib là khoảng 5,38 giờ. Thông tin kê đơn nêu rõ thời gian bán hủy trung bình hình học là khoảng 8,21 giờ.
Độc tính ở người
Tucatinib tác dụng phụ thường gặp có thể bao gồm các triệu chứng như bệnh tiêu chảy, phát ban, mẩn đỏ, đau, sưng hoặc phồng rộp ở lòng bàn tay hoặc lòng bàn chân, buồn nôn, và sự mệt mỏi. Ngoài ra, có thể xuất hiện các biểu hiện khác như tăng xét nghiệm chức năng gan, nôn mửa, nhiệt miệng, giảm sự thèm ăn, đau ở vùng bụng, đau đầu, số lượng hồng cầu thấp (thiếu máu), và phát ban.
Rất tiếc là thông tin về LD50 và quá liều Tucatinib không có sẵn trong tài liệu. Trong trường hợp dùng quá liều, các tác dụng phụ có thể gia tăng, bao gồm tiêu chảy, buồn nôn, đau bụng, mệt mỏi, nôn mửa, tổn thương gan, chán ăn, thiếu máu, đau đầu và phát ban.
Tính an toàn
Trong các thử nghiệm lâm sàng trước khi cấp phép, việc sử dụng tucatinib kết hợp với trastuzumab và capecitabine ở bệnh nhân ung thư vú HER2 dương tính di căn và không thể cắt bỏ đã gây ra các biến đổi bất thường trong xét nghiệm gan, thường chỉ xuất hiện tạm thời và có mức độ nhẹ. Điều đáng chú ý là có sự tăng ALT ở tỷ lệ 46% người sử dụng tucatinib so với 27% người được điều trị chỉ bằng trastuzumab và capecitabine đơn thuần. Mức tăng ALT vượt qua ngưỡng bình thường (ULN) lên trên 5 lần chỉ xuất hiện ở 8% bệnh nhân được điều trị bằng tucatinib, trong khi chỉ dưới 1% trong nhóm chứng kiểm soát chỉ sử dụng trastuzumab và capecitabine.
Trong một nghiên cứu kiểm soát với 612 bệnh nhân ung thư vú, 9 trường hợp sử dụng tucatinib đã gặp tăng ALT và bilirubin máu. Tuy nhiên, sau đánh giá chi tiết, không có bằng chứng nào đặt ra nghi vấn về tổn thương gan nặng liên quan đến tucatinib; mọi bệnh nhân đều có các nguyên nhân khác có thể gây tổn thương gan và vàng da. Trong toàn bộ các nghiên cứu tiền cấp phép, không có trường hợp suy gan hoặc nhiễm độc gan nào có liên quan với việc sử dụng tucatinib dẫn đến tử vong.
Hướng dẫn sử dụng của tucatinib đề xuất theo dõi các xét nghiệm gan định kỳ trước và 3 tuần một lần trong suốt quá trình điều trị và theo chỉ định lâm sàng.
Đối với phụ nữ mang thai, dựa trên nghiên cứu động vật và cơ chế tác động của tucatinib, có khả năng gây hại cho thai nhi. Tuy nhiên, do chưa có dữ liệu cụ thể về sử dụng tucatinib ở phụ nữ mang thai, nguy cơ cụ thể đối với thai nhi không rõ ràng. Phụ nữ mang thai và có kế hoạch mang thai nên thảo luận với bác sĩ về nguy cơ tiềm ẩn liên quan đến thai nhi, bao gồm cả nguy cơ về dị tật nghiêm trọng và sẩy thai.
Về việc sử dụng tucatinib trong thời kỳ cho con bú, không có thông tin lâm sàng cụ thể. Nhà sản xuất khuyến cáo tạm dừng cho con bú trong khi điều trị bằng tucatinib và trong 1 tuần sau liều cuối cùng. Tuy nhiên, khi sử dụng tucatinib kết hợp với trastuzumab và capecitabine, việc tạm dừng cho con bú được khuyến nghị trong 7 tháng sau khi sử dụng trastuzumab.
Tương tác với thuốc khác
Khi sử dụng Tucatinib, tránh kết hợp với chất cảm ứng CYP3A mạnh hoặc CYP2C8 vừa phải để ngăn chặn giảm hoạt động của thuốc.
Không sử dụng đồng thời với Tucatinib nếu có sự hiện diện của chất ức chế CYP2C8 mạnh hoặc trung bình để tránh tăng nguy cơ ngộ độc.
Tránh kết hợp với chất nền CYP3A khi sử dụng Tucatinib để ngăn chặn tăng độc tính liên quan đến chất nền CYP3A. Nếu không tránh khỏi, hãy giảm liều lượng chất nền CYP3A.
Lưu ý khi sử dụng Tucatinib
Không tự ý thay đổi liều dùng Tucatinib đã được bác sĩ chỉ định.
Người bệnh được khuyến cáo không nên sử dụng viên thuốc nếu nó bị vỡ, nứt hoặc không còn nguyên vẹn.
Trước khi bắt đầu sử dụng, đọc kỹ tờ hướng dẫn sử dụng thuốc Tucatinib để hiểu rõ hơn về cách sử dụng và các hạn chế liên quan.
Một vài nghiên cứu của Tucatinib trong Y học
Hiệu quả của tucatinib đối với bệnh ung thư vú di căn dương tính với HER2 sau liệu pháp nhắm mục tiêu HER2: phân tích tổng hợp mạng lưới
Mục tiêu: Đánh giá tài liệu có hệ thống và phân tích tổng hợp mạng lưới các thử nghiệm ngẫu nhiên có đối chứng ở những bệnh nhân được điều trị ung thư vú di căn/không thể cắt bỏ HER2+ sau ≥1 liệu pháp điều trị bằng HER2 được tiến hành để so sánh tỷ lệ sống sót không tiến triển (PFS) và tỷ lệ sống sót chung (OS).
Phương pháp: Tỷ lệ rủi ro (HR) và sự khác biệt tương đối so với đa thức phân đoạn (FP) đối với PFS và OS được đánh giá bằng phân tích tổng hợp mạng Bayesian.
Kết quả: Đối với PFS, bề mặt dưới biểu đồ xếp hạng tích lũy (SUCRA) xếp hạng tucatinib cộng với trastuzumab với capecitabine là cao nhất trong cả phân tích HR và FP, tiếp theo là đơn trị liệu T-DM1 và neratinib cộng với capecitabine. Đối với OS, SUCRA xếp hạng tucatinib cộng trastuzumab với capecitabine là cao nhất trong cả phân tích HR và FP, tiếp theo là pertuzumab cộng trastuzumab với đơn trị liệu capecitabine và T-DM1, với điểm số tương tự.
Kết luận: Tucatinib cộng với trastuzumab với capecitabine và đơn trị liệu T-DM1, luôn cho thấy PFS và OS được cải thiện so với lapatinib/trastuzumab cộng với capecitabine và các phương pháp điều trị không nhắm mục tiêu.
Tài liệu tham khảo
- Drugbank, Tucatinib, truy cập ngày 18 tháng 11 năm 2023.
- DeBusk K, Abeysinghe S, Vickers A, Nangia A, Bell J, Ike C, Forero-Torres A, Blahna MT. Efficacy of tucatinib for HER2-positive metastatic breast cancer after HER2-targeted therapy: a network meta-analysis. Future Oncol. 2021 Nov;17(33):4635-4647. doi: 10.2217/fon-2021-0742. Epub 2021 Aug 31. PMID: 34463120.
- Pubchem, Tucatinib, truy cập ngày 18 tháng 11 năm 2023.
- Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội.
Liệu pháp nhắm trúng đích
0 đ
Xuất xứ: Bangladesh