Chưa có sản phẩm trong giỏ hàng.
Trastuzumab
Danh pháp
Tên chung quốc tế
Nhóm thuốc
Thuốc chống ung thư
Mã ATC
L – Chất kháng nhựa và điều chỉnh miễn dịch
L01 – Chất kháng nhựa
L01F – Kháng thể đơn đơn và tổng hợp thuốc kháng thể
L01FD – Thuốc ức chế HER2 (Thụ thể yếu tố tăng trưởng biểu bì 2 ở người)
L01FD01 – Trastuzumab
Phân loại nguy cơ cho phụ nữ có thai
X
Mã UNII
180288-69-1
Mã CAS
180288-69-1
Cấu trúc phân tử
Công thức phân tử
C6470H10012N1726O2013S42
Phân tử lượng
145531.5 Da
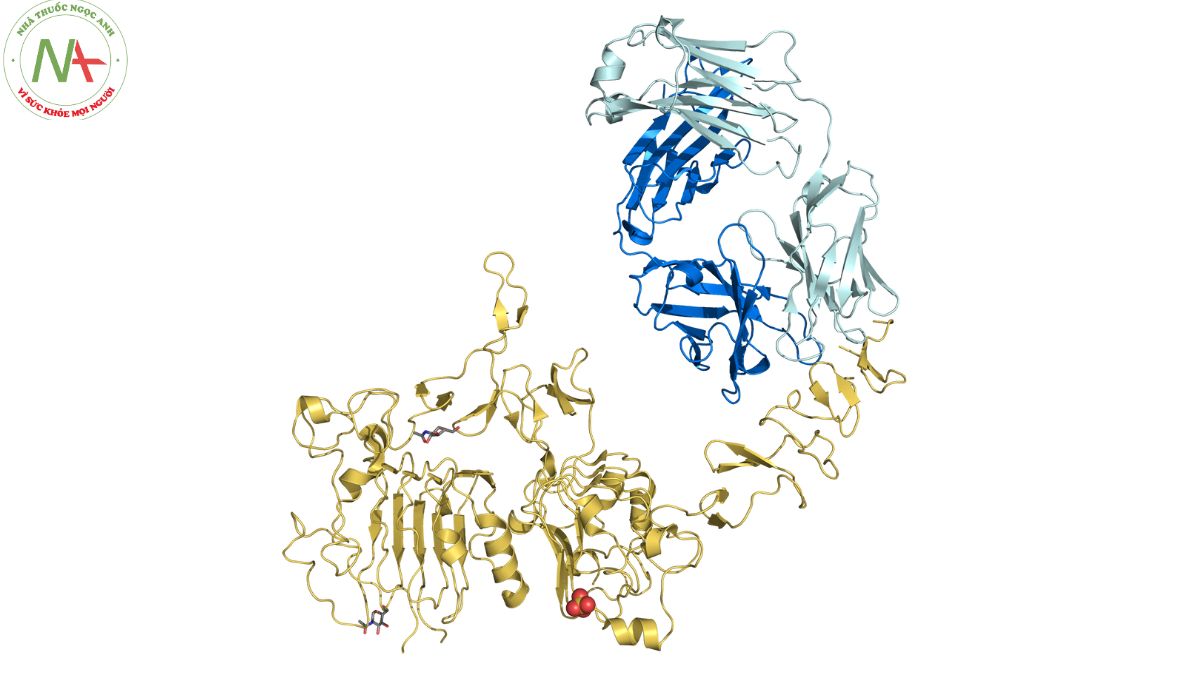
Cấu trúc phân tử
Dạng bào chế
Bột dùng để pha dịch truyền: 150 mg trong lọ 15 ml; 440 mg trong lọ 20 ml.

Độ ổn định và điều kiện bảo quản
Trastuzumab là một loại thuốc có tính ổn định cao và yêu cầu điều kiện bảo quản cụ thể để đảm bảo hiệu quả và an toàn sử dụng. Dưới đây là một số hướng dẫn về độ ổn định và điều kiện bảo quản của trastuzumab:
Bảo quản nhiệt độ: Trastuzumab dạng bột có thể được bảo quản an toàn trong tủ lạnh, ở nhiệt độ từ 2 đến 8 °C trong vòng 4 năm. Điều này đảm bảo rằng thuốc không bị phân hủy và duy trì tính chất hiệu quả.
Hòa tan ổn định: Khi hòa tan trastuzumab, hãy làm điều này ở nhiệt độ từ 2 đến 8 °C và sử dụng nó trong vòng 48 giờ. Điều này giúp duy trì tính chất của dung dịch và tránh việc mất hiệu quả của thuốc.
Pha loãng vô trùng: Nếu cần pha loãng trastuzumab, hãy thực hiện quy trình này trong điều kiện vô trùng và sử dụng dung dịch đã pha loãng trong vòng 24 giờ ở nhiệt độ dưới 30 °C. Điều này đảm bảo sự ổn định của dung dịch pha loãng.
Hạn chế sử dụng dung dịch glucose: Trastuzumab không nên được pha vào dung dịch glucose, vì điều này có thể gây tủa protein và làm mất tính chất của thuốc.
Không pha lẫn với các loại thuốc khác: Trastuzumab không nên được pha lẫn với bất kỳ loại thuốc nào trong dung dịch truyền. Điều này giúp tránh xảy ra tương kỵ hoặc phản ứng không mong muốn.
Tương thích với túi và ống dây truyền: Trastuzumab không tương kỵ với các túi và ống dây truyền được làm từ polyvinyl clorid, polyetylen và polypropylen. Do đó, có thể sử dụng các túi và dây truyền này để đựng dung dịch truyền trastuzumab một cách an toàn.
Nguồn gốc
Trastuzumab là thuốc gì? Trong hành trình đột phá y khoa, thuốc trastuzumab đã trải qua một quá trình phát triển đầy thách thức và hợp tác. Ban đầu, nó là kết quả của những phát hiện tiên phong bởi Tiến sĩ Axel Ullrich và Tiến sĩ H. Michael Shepard từ Genentech, Inc., cùng với những đóng góp không thể phủ nhận từ các phòng thí nghiệm của Robert Weinberg và Mark Greene. Những nghiên cứu này đã mở đường cho các liệu pháp nhắm mục tiêu vào gen gây ung thư HER2. Tiến sĩ Dennis Slamon và đội ngũ của ông sau đó đã phát triển trastuzumab, một bước tiến lớn trong điều trị ung thư.
Cuộc hành trình của trastuzumab từ phòng thí nghiệm đến bệnh nhân không chỉ là một câu chuyện khoa học, mà còn là nguồn cảm hứng cho bộ phim truyền hình ‘Living Proof’, phát sóng vào năm 2008. Sự hợp tác giữa Genentech và UCLA đã dẫn đến các thử nghiệm lâm sàng quan trọng, bắt đầu từ năm 1992 với 15 phụ nữ và mở rộng lên đến hơn 900 người tham gia vào năm 1996. Đáp ứng áp lực từ cộng đồng, Genentech đã hợp tác với FDA để triển khai một chương trình xổ số độc đáo, mở cánh cửa cho nhiều bệnh nhân tiếp cận thuốc ngoài khuôn khổ thử nghiệm.
Cuối cùng, vào tháng 9 năm 1998, FDA đã nhanh chóng chấp thuận Herceptin, một bước ngoặt quan trọng trong điều trị ung thư. Tuy nhiên, Biocon Ltd và Mylan, sau khi nhận được sự chấp thuận vào năm 2014 để sản xuất phiên bản tương tự của thuốc, đã đối mặt với sự phản đối pháp lý từ Roche. Mặc dù cuộc chiến pháp lý kéo dài đến năm 2016, cả Biocon và Mylan cuối cùng cũng đã giới thiệu các sản phẩm của mình, mở ra một kỷ nguyên mới trong việc sản xuất thuốc sinh học.
Dược lý và cơ chế hoạt động
Trastuzumab cơ chế: Trastuzumab là một thành tựu y khoa đột phá, một kháng thể đơn dòng tái tổ hợp với khả năng đặc biệt liên kết với thụ thể HER2, đóng vai trò quan trọng trong việc điều chỉnh quá trình biệt hóa và tăng sinh của tế bào. Đặc điểm nổi bật của trastuzumab là khả năng tác động mục tiêu đến những tế bào ung thư có biểu hiện HER2 quá mức, trong khi gây ít tổn thương đến tế bào lành tính.
Trastuzumab không chỉ là một phương pháp điều trị hiệu quả trong cuộc chiến chống ung thư vú, mà còn là một ví dụ điển hình về cách thức mà y khoa hiện đại tấn công vào những tế bào ung thư đặc thù. HER2, vốn là một tiền gen ung thư, chịu trách nhiệm cho sự tăng trưởng và phát triển không kiểm soát của tế bào ung thư. Khi HER2 được kích hoạt quá mức, nó thúc đẩy quá trình hình thành và tiến triển của ung thư vú, bất kể tình trạng hạch.
Trước khi bắt đầu liệu pháp trastuzumab, việc xác định mức độ biểu hiện của HER2/neu là bước không thể thiếu. Các phòng thí nghiệm chuyên biệt sử dụng phương pháp hóa miễn dịch mô và lai huỳnh quang tại chỗ để đánh giá mức độ biểu hiện protein HER2/neu và khuếch đại của gen ung thư liên quan. Mặc dù trị liệu bằng trastuzumab là một quá trình tốn kém, nhưng nó mở ra hy vọng mới trong việc điều trị cho những bệnh nhân ung thư vú HER2 dương tính.
Ứng dụng trong y học
Trastuzumab chỉ định? Trastuzumab, một kháng thể đơn dòng có tác động mạnh mẽ, đã trở thành lựa chọn hàng đầu trong điều trị bổ trợ cho bệnh ung thư vú với sự biểu hiện quá mức của HER2. Trong thực hành lâm sàng, trastuzumab được tích hợp thành công vào nhiều phác đồ điều trị. Điển hình, nó được sử dụng kết hợp với các hóa chất liệu pháp như doxorubicin, cyclophosphamide và paclitaxel hoặc docetaxel; hoặc trong sự kết hợp với docetaxel và carboplatin. Ngoài ra, trastuzumab cũng được sử dụng độc lập sau các liệu pháp đa phương thức dựa trên anthracycline.
Đối với trường hợp ung thư vú di căn biểu hiện quá mức HER2, trastuzumab lại đóng vai trò như một lựa chọn điều trị ưu tiên khi kết hợp với paclitaxel. Đặc biệt, nó cũng được áp dụng như một liệu pháp đơn lẻ cho những bệnh nhân đã trải qua nhiều chế độ hóa trị liệu trong bối cảnh di căn.
Bên cạnh đó, trastuzumab còn mở rộng ảnh hưởng của mình trong việc điều trị ung thư biểu mô tuyến dạ dày hoặc khu vực nối giữa dạ dày và thực quản, khi được kết hợp cùng cisplatin và capecitabine hoặc 5-fluorouracil, đặc biệt đối với những trường hợp chưa từng được điều trị trước cho bệnh di căn.
Ngoài ra, trastuzumab còn có hình thức tiêm dưới da, khi kết hợp với hyaluronidase hoặc cả hyaluronidase và pertuzumab, như một giải pháp hiệu quả cho người lớn mắc bệnh ung thư vú HER2 dương tính. Điều này không chỉ cung cấp một phương pháp điều trị mới mà còn tạo điều kiện thuận lợi cho việc quản lý bệnh.
Dược động học
Hấp thu
Trastuzumab, khi vào cơ thể, trải qua một loạt quá trình tương tác phức tạp. Trong giai đoạn ổn định từ tuần 16 đến tuần 32, nồng độ trastuzumab trong huyết tương đạt đỉnh khoảng 123 mcg/mL và đáy ở mức 79 mcg/mL. Đặc biệt, ở liều cao nhất được nghiên cứu, 500 mg mỗi tuần, nồng độ đỉnh trung bình đạt 377 mcg/mL.
Phân bố
Không có thông tin
Chuyển hóa
Sau khi liên kết với HER2, trastuzumab được phân giải trong tế bào thành các peptide và axit amin nhỏ hơn.
Thải trừ
Quá trình thải trừ trastuzumab diễn ra thông qua các tế bào biểu mô theo một cơ chế phi tuyến tính, phụ thuộc vào liều lượng. Thú vị là, sự bài tiết qua thận của trastuzumab rất thấp. Thời gian bán hủy cuối cùng của nó vào khoảng 28 ngày, nhưng có thể rút ngắn đáng kể ở liều thấp hơn – chẳng hạn, ở liều 10mg và 500mg, thời gian bán hủy trung bình lần lượt là khoảng 1,7 và 12 ngày.
Độ thanh thải của trastuzumab ở trạng thái ổn định được dự đoán từ 0,173 đến 0,337 L/ngày, phụ thuộc vào chế độ dùng thuốc. Đối với trastuzumab tiêm dưới da, được điều chế với hyaluronidase để cải thiện khả năng hấp thu, tốc độ thanh thải là 0,11 L/ngày.
Phương pháp sản xuất
Trastuzumab, một ví dụ điển hình của sự tiến bộ trong công nghệ y sinh, được tạo ra thông qua quá trình tinh vi của DNA tái tổ hợp. Trong quá trình sản xuất, tế bào động vật có vú – cụ thể là tế bào buồng trứng của Hamster Trung Quốc – đóng vai trò thiết yếu. Điều đặc biệt là, dù trong quá trình nuôi cấy sử dụng kháng sinh gentamicin, nhưng qua các bước lọc và tinh chế kỹ lưỡng, gentamicin không còn tồn tại trong sản phẩm cuối cùng.
Độc tính ở người
Trastuzumab tác dụng phụ? Trastuzumab không tránh khỏi việc gây ra các tác dụng phụ (ADR), đặc biệt khi sử dụng kết hợp với các loại thuốc khác. Các ADR này có thể phân loại dựa trên tần suất xuất hiện:
- Rất thường gặp (trên 10 trường hợp trong mỗi 100 người dùng): Phản ứng do truyền thuốc, rối loạn tim mạch như giảm phân số tống máu, các vấn đề về da như nổi mẩn, và các vấn đề tiêu hóa như đau bụng, ỉa chảy, chán ăn, buồn nôn và nôn. Ngoài ra, còn có các vấn đề huyết học, miễn dịch, cơ – xương, thần kinh, hô hấp, và hội chứng giống cúm.
- Thường gặp (trên 1 trường hợp nhưng dưới 10 trường hợp trong mỗi 100 người dùng): Các vấn đề về tim mạch như phù ngoại vi và tăng huyết áp, trầm cảm, vấn đề về da như trứng cá, ngứa, và các vấn đề hô hấp như viêm xoang và viêm mũi họng.
- Ít gặp (trên 1 trường hợp nhưng dưới 10 trường hợp trong mỗi 1,000 người dùng): Các vấn đề về thận như hội chứng thận hư và suy thận, suy hô hấp cấp, phản vệ, và suy tim cấp.
Trong quá trình nghiên cứu và ứng dụng lâm sàng, trastuzumab vẫn chưa ghi nhận trường hợp quá liều hoặc ngộ độc cấp tính đáng kể. Điều này được chứng minh ngay cả trong các thí nghiệm lâm sàng với liều lượng lên đến 500 mg/m2. Đáng chú ý là, đến nay, chưa có bất kỳ thuốc giải độc đặc hiệu nào dành riêng cho trastuzumab.
Tính an toàn
Trastuzumab chống chỉ định? Trastuzumab, một phần không thể thiếu trong điều trị một số loại ung thư, không phù hợp cho tất cả mọi người. Những trường hợp không nên sử dụng trastuzumab bao gồm những người đang trải qua khó khăn với hô hấp, kể cả khi nghỉ ngơi, hoặc những người cần sử dụng oxy liên tục. Ngoài ra, nếu có vấn đề về tim như đau thắt ngực cần điều trị, loạn nhịp tim, rối loạn nặng trong hệ thống dẫn truyền tim, các vấn đề về van tim có triệu chứng lâm sàng, tim to trên phim X-quang, phì đại thất trái trên siêu âm, huyết áp cao, tràn dịch màng ngoài tim, nhồi máu cơ tim, suy tim ứ máu hoặc bệnh cơ tim, thì trastuzumab cũng không phải là lựa chọn thích hợp.
Trong thời kỳ mang thai, trastuzumab cần được cân nhắc kỹ lưỡng do khả năng gây thiểu ối và ảnh hưởng tới sự phát triển của hệ tim mạch và thần kinh trung ương của thai nhi, đặc biệt xét đến mức độ cao của HER2 receptor trong nhiều mô của thai, bao gồm cả mô tim và thần kinh. Sử dụng trastuzumab trong giai đoạn này chỉ được khuyến nghị khi lợi ích mang lại lớn hơn rủi ro tiềm ẩn.
Đối với thời kỳ cho con bú, vẫn chưa rõ liệu trastuzumab có được bài tiết qua sữa mẹ hay không. Tuy nhiên, vì kháng thể IgG có mặt trong sữa mẹ và trastuzumab có thể gây ra các tác dụng phụ (ADR) ở trẻ bú mẹ, nên người mẹ cần ngừng cho con bú trong suốt thời gian điều trị và 6 tháng sau khi dùng liều cuối cùng của trastuzumab.
Tương tác với thuốc khác
Vẫn còn nhiều điều chưa được khám phá về cách thức tương tác giữa trastuzumab và các loại thuốc khác. Một điểm đáng lưu ý là sự kết hợp của trastuzumab với các thuốc chống ung thư nhóm anthracyclin đã được chứng minh làm tăng nguy cơ độc tính lên tim. Do đó, việc sử dụng đồng thời hai loại thuốc này trong điều trị ung thư vú không được khuyến nghị.
Ngoài ra, trong quá trình nghiên cứu lâm sàng, đã phát hiện ra rằng khi trastuzumab được sử dụng phối hợp với paclitaxel, nồng độ trung bình của trastuzumab trong cơ thể tăng lên khoảng 1,5 lần. Điều này cần được cân nhắc kỹ lưỡng trong việc quyết định liều lượng và theo dõi bệnh nhân.
Thêm vào đó, trastuzumab cũng làm tăng hiệu quả của warfarin, một loại thuốc chống đông. Điều này yêu cầu một sự chú ý đặc biệt để tránh các rủi ro tiềm ẩn, đặc biệt là với bệnh nhân đang dùng warfarin cho các vấn đề về huyết học.
Lưu ý khi sử dụng Trastuzumab
Khi áp dụng trastuzumab trong điều trị, một số khía cạnh quan trọng cần được chú trọng. Đầu tiên và quan trọng nhất, việc kiểm tra HER2 phải được tiến hành tại phòng thí nghiệm chuyên khoa, đảm bảo tuân thủ các tiêu chuẩn kỹ thuật nghiêm ngặt.
Đối với bệnh nhân đã trải qua hóa trị liệu với anthracycline (như doxorubicin hoặc epirubicin), cần phải hết sức thận trọng. Đặc biệt là đối với những người có vấn đề về tim, việc kiểm tra kỹ lưỡng trước khi sử dụng trastuzumab là cần thiết: từ việc thu thập tiền sử bệnh, thực hiện khám lâm sàng, điện tâm đồ, siêu âm tim, chụp hình phóng xạ, cho đến cộng hưởng từ. Việc đánh giá lợi ích so với rủi ro trước khi sử dụng trastuzumab là bước không thể bỏ qua. Nó chỉ nên được sử dụng cho những người có phân số tống máu của thất trái trong phạm vi bình thường (ít nhất là ≥ 50%) và có sự giảm ít hơn 15 điểm từ mức cơ sở sau khi hoàn thành hóa trị liệu bổ sung với doxorubicin và cyclophosphamide.
Cần lưu ý rằng người cao tuổi có thể gặp nguy cơ cao hơn về tác dụng phụ so với người trẻ. Đối với bệnh nhân gặp phản ứng do truyền thuốc, họ không nên lái xe hoặc vận hành máy móc cho đến khi triệu chứng hết hoàn toàn, để tránh nguy cơ gây ra tai nạn.
Một vài nghiên cứu của Trastuzumab trong Y học
Trastuzumab điều trị ung thư vú dương tính với HER2 giai đoạn đầu: phân tích tổng hợp trên 13.864 phụ nữ trong bảy thử nghiệm ngẫu nhiên
Bối cảnh: Trastuzumab nhắm vào miền ngoại bào của protein HER2. Việc bổ sung trastuzumab vào hóa trị liệu cho bệnh nhân ung thư vú dương tính với HER2 giai đoạn đầu giúp giảm nguy cơ tái phát và tử vong nhưng có liên quan đến nhiễm độc tim. Chúng tôi đã nghiên cứu những lợi ích và rủi ro lâu dài của trastuzumab bổ trợ đối với việc tái phát ung thư vú và tỷ lệ tử vong do nguyên nhân cụ thể.
Phương pháp: Chúng tôi đã thực hiện phân tích tổng hợp cộng tác dữ liệu của từng bệnh nhân từ các thử nghiệm ngẫu nhiên đánh giá hóa trị liệu cộng với trastuzumab so với chỉ hóa trị liệu tương tự. Các thử nghiệm ngẫu nhiên thu nhận những phụ nữ mắc ung thư vú có thể phẫu thuật được, có hạch âm tính hoặc hạch dương tính, có thể phẫu thuật được.
Chúng tôi đã thu thập dữ liệu ở cấp độ bệnh nhân riêng lẻ về các đặc điểm cơ bản, ngày và vị trí tái phát ung thư vú ở xa lần đầu tiên và bất kỳ đợt tái phát cục bộ nào trước đó hoặc ung thư nguyên phát thứ hai cũng như ngày và nguyên nhân tử vong cơ bản. Kết quả chính là tái phát ung thư vú, tử vong do ung thư vú, tử vong không tái phát và tử vong do mọi nguyên nhân.
Các phân tích thứ hạng log theo ý định điều trị tiêu chuẩn, được phân tầng theo độ tuổi, tình trạng hạch, trạng thái thụ thể estrogen (ER) và thử nghiệm mang lại tỷ lệ biến cố đầu tiên (RR).
Kết quả: Bảy thử nghiệm ngẫu nhiên đáp ứng các tiêu chí thu nhận và bao gồm 13.864 bệnh nhân được ghi danh từ tháng 2 năm 2000 đến tháng 12 năm 2005. Thời gian điều trị trung bình theo lịch trình là 14·4 tháng và thời gian theo dõi trung bình là 10·7 năm (IQR 9·5 đến 11·9).
Nguy cơ tái phát ung thư vú (RR 0·66, 95% CI 0·62 đến 0·71; p<0·0001) và tử vong do ung thư vú (0·67, 0·61 đến 0·73; p<0 ·0001) thấp hơn khi dùng trastuzumab cộng với hóa trị so với chỉ dùng hóa trị.
Nguy cơ tái phát tuyệt đối sau 10 năm đã giảm 9·0% (KTC 95% 7·4 đến 10·7; p<0·0001) và tỷ lệ tử vong do ung thư vú trong 10 năm đã giảm 6·4% (4·9 đến 7·8; p<0·0001), với mức giảm 6·5% (5·0 đến 8·0; p<0·0001) về tỷ lệ tử vong do mọi nguyên nhân và không tăng tỷ lệ tử vong mà không tái phát (0·4 %, -0·3 đến 1·1; p=0·35).
Mức giảm tỷ lệ tái phát lớn nhất ở các năm 0-1 sau khi ngẫu nhiên hóa (0·53, 99% CI 0·46 đến 0·61), với các lợi ích kéo dài qua các năm 2-4 (0·73, 0·62 đến 0· 85) và 5-9 (0·80, 0·64 đến 1·01), và rất ít theo dõi sau năm thứ 10.
Tỷ lệ giảm tái phát theo tỷ lệ là tương tự nhau bất kể đặc điểm của bệnh nhân và khối u được ghi lại, bao gồm cả tình trạng ER. Khối u có nguy cơ càng cao thì mức giảm tuyệt đối tái phát sau 5 năm càng lớn (ví dụ: 5·7% [95% CI 3·1 đến 8·3], 6·8% [4·7 đến 9·0], và 10·7% [7·7 đến 13·6] ở bệnh N0, N1-3 và N4+).
Giải thích: Việc bổ sung trastuzumab vào hóa trị liệu cho bệnh ung thư vú dương tính với HER2 giai đoạn đầu làm giảm tỷ lệ tái phát và tỷ lệ tử vong do ung thư vú xuống 1/3, với mức giảm tỷ lệ đáng kể bất kể đặc điểm khối u và bệnh nhân được ghi nhận.
Tài liệu tham khảo
- Drugbank, Trastuzumab, truy cập ngày 24 tháng 11 năm 2023.
- Early Breast Cancer Trialists’ Collaborative group (EBCTCG). Trastuzumab for early-stage, HER2-positive breast cancer: a meta-analysis of 13 864 women in seven randomised trials. Lancet Oncol. 2021 Aug;22(8):1139-1150. doi: 10.1016/S1470-2045(21)00288-6. PMID: 34339645; PMCID: PMC8324484.
- Pubchem, Trastuzumab, truy cập ngày 24 tháng 11 năm 2023.
- Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội.
Liệu pháp nhắm trúng đích
0 đ
Xuất xứ: Thụy Sĩ
Liệu pháp nhắm trúng đích
0 đ
Xuất xứ: Đức