Bệnh hô hấp
Liệu Pháp Oxy Dòng Cao Qua Ống Thông Mũi Trong Bệnh Nhân COPD Với Suy Hô Hấp Tăng CO2 Máu
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
nhathuocngocanh. Liệu Pháp Oxy Dòng Cao Qua Ống Thông Mũi Trong Bệnh Nhân COPD
Để tải file PDF, hãy click Tại Đây.
Bản Lược Dịch Của Bác Sĩ Trần Minh Thành
Bác Sĩ Hà Thị Phương Thảo
Bệnh Viện Đa Khoa Tỉnh Khánh Hòa
Tóm Tắt
Liệu pháp oxy dòng cao qua ống thông mũi (NHF) gần đây đã được chú ý như một hệ thống hỗ trợ hô hấp mới và đang ngày càng được sử dụng trong thực hành lâm sàng hàng ngày. Các nghiên cứu gần đây cho thấy rằng nó cũng có thể hiệu quả ở những bệnh nhân tăng CO2 máu và đề xuất NHF như một giải pháp thay thế khả thi cho những bệnh nhân không dung nạp thông khí không xâm lấn. Tổng quan tài liệu thảo luận về cơ chế hoạt động làm cho NHF có khả năng phù hợp với bệnh nhân bệnh phổi tắc nghẽn mạn tính (COPD) và đánh giá bằng chứng hiện tại về việc sử dụng NHF để điều trị bệnh nhân COPD ổn định tăng CO2 máu cũng như đợt cấp COPD tăng CO2 máu. Một thuật toán cũng được đề xuất cho ứng dụng lâm sàng của NHF ở bệnh nhân COPD đợt cấp tăng CO2 máu, dựa trên các tài liệu hiện tại.
Giới Thiệu
Thông khí không xâm lấn (NIV) được công nhận rộng rãi là liệu pháp chính cho những bệnh nhân đợt cấp bệnh phổi tắc nghẽn mãn tính (COPD) tăng CO2 máu cấp [1,2]. Gần đây, NIV cũng được đề xuất theo hướng dẫn của Hiệp hội Hô hấp Châu Âu cho bệnh nhân COPD ổn định mãn tính tăng CO2 máu, nhằm mục tiêu giảm hoặc thậm chí bình thường hóa mức PaCO2 [2,3]. Tuy nhiên, bất kể chỉ định áp dụng NIV, khả năng dung nạp thường kém do nhiều tác dụng phụ, chẳng hạn như hội chứng sợ hãi, kích ứng mắt và loét áp lực [4]. Cho đến nay, không có phương pháp điều trị thay thế nào được thiết lập cho những bệnh nhân không thể dung nạp NIV chuẩn.
Liệu pháp oxy dòng cao qua ống thông mũi (NHF) gần đây đã được chú ý như một hệ thống hỗ trợ hô hấp mới và ngày càng được sử dụng nhiều hơn trong thực hành lâm sàng hàng ngày [5,6]. Việc cung cấp hỗn hợp khí oxy đã được làm ẩm và làm ấm ở tốc độ dòng cao (lên đến 60 L/min) được thực hiện thông qua một ống thông mũi. Mặc dù lợi ích của nó đã được chứng minh chủ yếu trong việc điều trị bệnh nhân suy hô hấp cấp giảm oxy máu [5–8], những nghiên cứu gần đây cho thấy rằng NHF cũng có thể có hiệu quả ở những bệnh nhân tăng CO2 máu và đề xuất NHF như một giải pháp thay thế khả thi cho những bệnh nhân không thể dung nạp NIV chuẩn. [9].
Bài tổng quan thảo luận về cơ chế hoạt động làm cho NHF có khả năng thích hợp cho những bệnh nhân COPD không thể dung nạp NIV. Ngoài ra, chúng tôi đánh giá bằng chứng hiện tại của NHF để điều trị bệnh nhân COPD ổn định có tăng CO2 máu mạn tính cũng như bệnh nhân đợt cấp COPD và suy hô hấp loại II. Hơn nữa, chúng tôi đề xuất một thuật toán cho ứng dụng lâm sàng của NHF ở bệnh nhân đợt cấp COPD tăng CO2 máu cấp, dựa trên các tài liệu hiện tại.
Cơ Chế Hoạt Động
NHF cung cấp tốc độ dòng lên đến 60 L/min có thể phù hợp hoặc thậm chí vượt quá nhu cầu dòng chảy vào đường hô hấp của bệnh nhân thông qua các ống thông mũi được thiết kế để tránh tạo ra áp lực trực tiếp vào bề mặt niêm mạc. Tốc độ dòng chảy cao này được dung nạp tốt vì khí cung cấp được làm ấm và làm ẩm liên tục giúp ngăn ngừa tình trạng mất độ ẩm đường thở [10]. Bộ trộn khí cung cấp nồng độ oxy hít vào (FiO2) nằm trong khoảng từ 0,21 đến 1,0 thông qua bộ dây được làm ấm một nhánh để tránh mất nhiệt và ngưng tụ [6]. Một ưu điểm rõ ràng của ứng dụng liệu pháp ống thông mũi so với mặt nạ hô hấp là tạo điều kiện thuận lợi cho các hoạt động hàng ngày, khả năng giao tiếp và ăn uống dễ dàng và mức độ tuân thủ cao hơn.
Một số lợi ích sinh lý làm cho NHF có khả năng thích hợp cho bệnh nhân COPD tăng CO2 [11]. Liệu pháp NHF tạo ra một ít áp lực dương cuối kỳ thở ra (PEEP) do sự đề kháng quá trình thở ra của bệnh nhân đối với dòng khí đi vào [12,13], điều đó dường như đối trọng với PEEP nội tại [14] và huy động vùng phổi xẹp [ 15–17]. Hơn nữa, tốc độ cao của khí đi vào làm tăng áp lực đường thở trên cao hơn áp suất khí quyển trong quá trình hít vào làm giảm rõ rệt sức cản hít vào liên quan đến vùng hầu họng [18].
Ngoài ra, liệu pháp NHF làm giảm thông khí khoảng chết thông qua hiệu ứng rửa CO2 từ đường thở trên, dẫn đến giảm mức PaCO2 [19,20]. Sự giảm PaCO2 không phụ thuộc vào áp lực mà phụ thuộc vào dòng, điều này cực kỳ quan trọng vì nó tách NHF khỏi NIV [21].
Hơn nữa, NHF tăng cường thanh thải niêm mạc phổi bằng cách làm ấm khí được cung cấp ở mức nhiệt độ lõi (37°C) và làm ẩm hệ hô hấp đến mức bão hòa, đặc biệt là ở tốc độ dòng cao [10, 22]. Việc hít thở không khí ấm và ẩm sẽ ức chế phản ứng co thắt phế quản, ngăn chặn bất kỳ sự gia tăng sức cản đường thở có thể gây ra bởi không khí lạnh và khô [23]. Hơn nữa, vì NHF cung cấp đầy đủ khí cho đường thở, chi phí chuyển hóa cần thiết để làm ấm và làm ẩm khí hít sẽ giảm xuống [24].
Một lý do khác khiến NHF có khả năng phù hợp với bệnh nhân COPD là thực tế NHF cung cấp các giá trị FiO2 ổn định hơn so với các giá trị của hệ thống cung cấp oxy chuẩn, vì tốc độ dòng cao có thể phù hợp hoặc thậm chí vượt quá nhu cầu lưu lượng hít vào của bệnh nhân, do đó làm giảm sự cuốn của không khí trong phòng và pha loãng oxy được cung cấp [25,26].
Kết quả là NHF làm giảm công thở ở bệnh nhân COPD dẫn đến giảm tần số hô hấp đồng thời cải thiện thông khí [7], giảm chỉ số thở nông nhanh (RSBI) [13] và cải thiện đồng bộ ngực – bụng [27].
Liệu Pháp Oxy Dòng Cao Trong COPD Ổn Định Có Tăng CO2 Máu
Xử trí bệnh nhân COPD ổn định ở giai đoạn nặng là đa yếu tố. Các điều trị dược lý, LTOT để điều trị giảm oxy máu mãn tính khi nghỉ ngơi và NIV cho bệnh nhân bị tăng CO2 máu nặng đồng thời được sử dụng để kiểm soát các triệu chứng cũng như giảm đợt cấp, cải thiện chất lượng cuộc sống (QoL) và tỷ lệ sống [2]. NHF dường như đóng một vai trò quan trọng trong mỗi lĩnh vực được đề cập ở trên để quản lý COPD (Bảng 1).
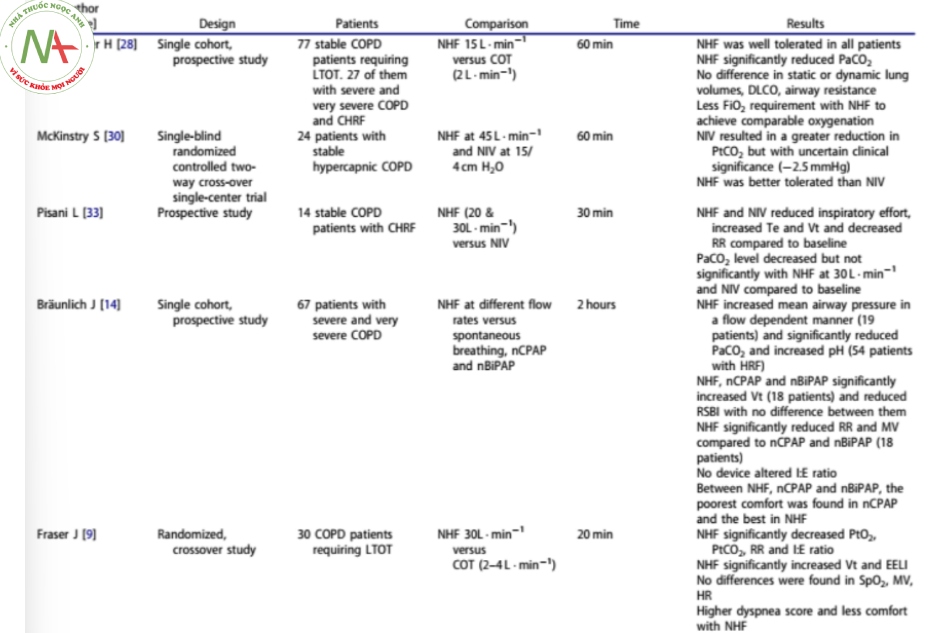

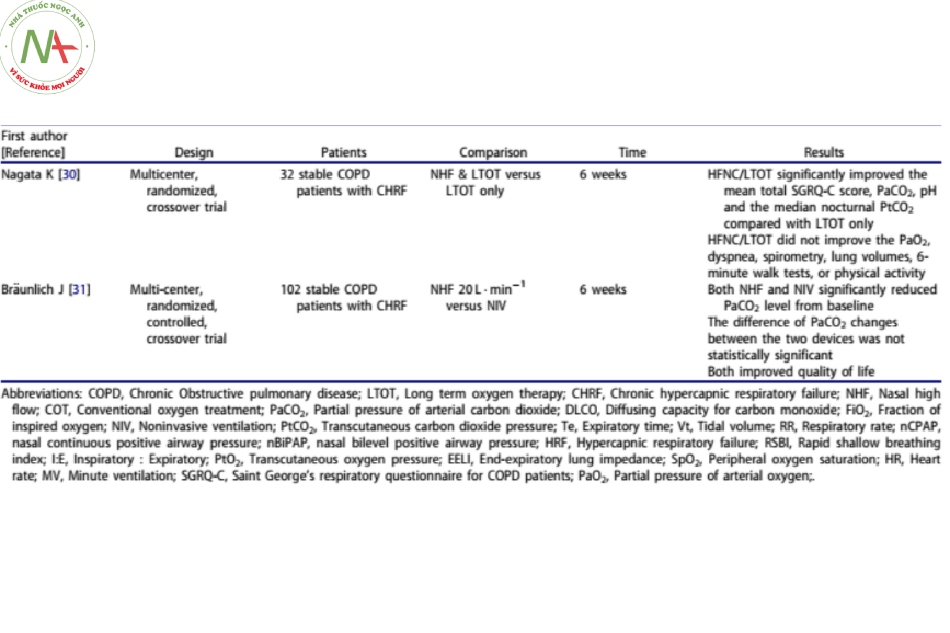
NHF làm giảm đáng kể mức PaCO2 phụ thuộc lưu lượng trong các nghiên cứu ngắn hạn và dài hạn (≥ 6 tuần) so với điều trị oxy thông thường (COT) [28-31]. NHF cũng làm giảm tải cơ hô hấp và công thở quá mức, tương tự như NIV, dẫn đến thông khí hiệu quả hơn và thay đổi đường cong áp suất – thể tích [6, 12, 32, 33]. Sự gia tăng đáng kể đồng thời về thể tích khí lưu thông và EELV kèm theo giảm tần số thở và giảm mức PaCO2 đã được mô tả [6,7,13,27,33] ngụ ý rằng bệnh nhân có thể quay trở lại để thở hiệu quả hơn [6]. Hơn nữa, NHF dường như được hầu hết bệnh nhân dung nạp tốt [28,34] và cảm giác thoải mái tốt hơn đáng kể so với nCPAP và BiPAP mũi [14].
NHF dường như cũng có tác dụng có lợi đối với khả năng gắng sức của bệnh nhân COPD. Trong một nghiên cứu của Chatila và cộng sự, bệnh nhân COPD gắng sức lâu hơn trên máy đo chu kỳ với ít khó thở hơn, kiểu thở tốt hơn và huyết áp thấp hơn được cho là do giảm tải và cải thiện cơ học phổi, so với COT [35]. Ngoài ra, oxy hóa cao hơn do FiO2 phù hợp hơn với NHF. Những kết quả này đã được Cirio et al hỗ trợ thêm. [36], họ đã báo cáo sự cải thiện đáng kể về thời gian chịu đựng ở bệnh nhân COPD nặng khi gắng sức cường độ cao liên tục dưới liệu pháp NHF. Hiệu quả có liên quan đến việc cải thiện độ bão hòa oxy, ít khó thở hơn và ít mỏi chân hơn [36].
NHF dường như không làm giảm tần suất đợt cấp một cách đáng kể, mặc dù nó làm giảm số ngày đợt cấp và tăng thời gian đến đợt cấp đầu tiên [37]. Chức năng phổi được đo bằng FEV1 và FVC được cải thiện và giảm tình trạng bẫy khí ở phổi. Cả hai tác dụng này được cho là do chức năng đường thở nhỏ tốt hơn thông qua việc thanh thải chất nhầy tốt hơn [37].
Tác dụng có lợi của NHF đối với cơ hô hấp, trao đổi khí, khả năng gắng sức và các đợt cấp trong giai đoạn nặng của COPD đi kèm với sự cải thiện các biện pháp QoL, như được chỉ ra trong các nghiên cứu dài hạn, với những lợi ích được quan sát thấy trong cả bốn thành phần của SGRQ [30,31,37].
Oxy Dòng Cao Qua Ống Thông Mũi Trong Đợt Cấp COPD
Một trong những tiến bộ kỹ thuật quan trọng nhất trong hỗ trợ hô hấp là sự ra đời của NIV trong xử trí suy hô hấp cấp type II ở bệnh nhân COPD [38]. NIV đã được chứng minh là cải thiện tình trạng nhiễm toan hô hấp cấp, giảm tần số hô hấp, giảm công thở, mức độ khó thở, tỷ lệ đặt nội khí quản và thời gian nằm viện [2]. Quan trọng nhất, tỷ lệ tử vong đã được chứng minh là giảm 50% [1,38]. Tuy nhiên, NIV không được dung nạp ở gần 20% bệnh nhân dẫn đến đặt nội khí quản và thở máy xâm nhập vì không có giải pháp thay thế được thiết lập [39].
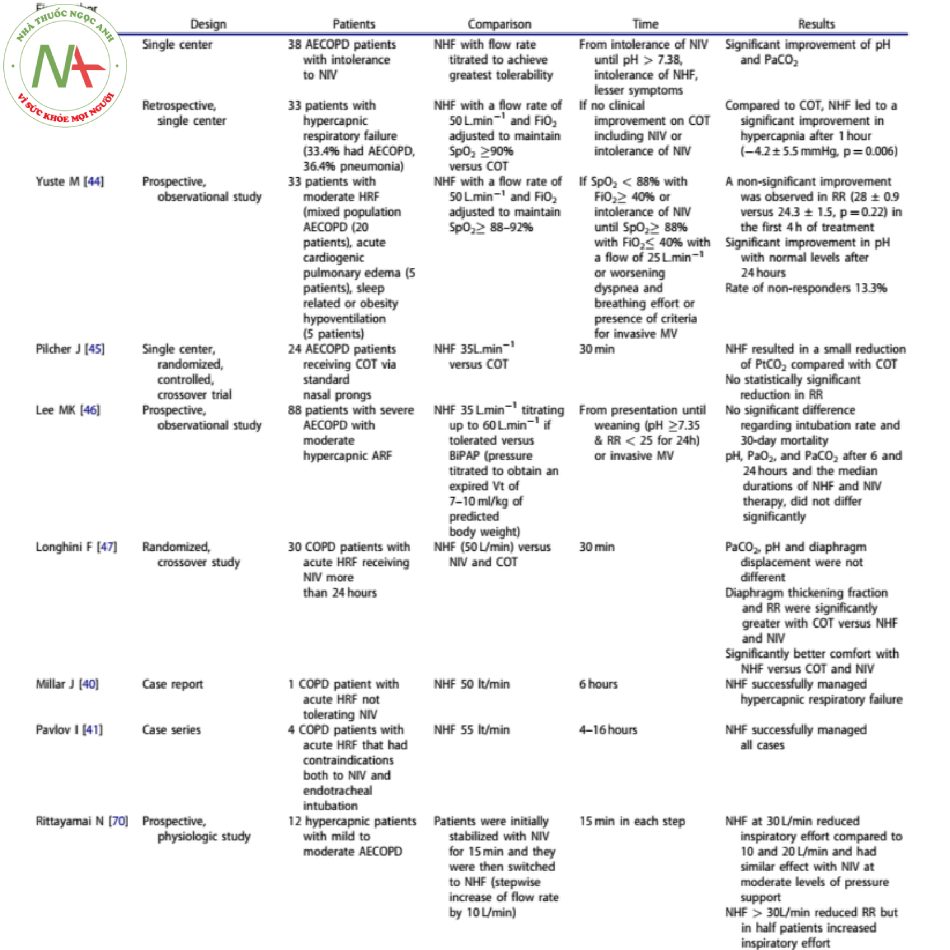
Năm 2014, Millar et al. [40], đã công bố một trường hợp NHF điều trị thành công suy hô hấp cấp do tăng CO2 máu ở một bệnh nhân COPD không thể dung nạp NIV. Hai năm sau, Pavlov et al. [41], báo cáo rằng 4 bệnh nhân chống chỉ định điều trị NIV bị suy hô hấp nặng đã được cứu sống thành công bằng NHF với tốc độ dòng cao (55 L/ min) và FiO2 được điều chỉnh để duy trì đo nồng độ oxy ngoại vi ≥ 90%. Hai trong số bốn bệnh nhân đạt được đáp ứng hoàn toàn về lâm sàng và xét nghiệm trong vòng chưa đầy 4 giờ [42]. Những kết quả này đã được xác nhận thêm bởi một nghiên cứu lớn hơn. Ba mươi tám bệnh nhân tăng CO2 máu toan máu trung bình đến nặng (pH <7,38 và PaCO2> 45 mmHg) đợt cấp COPD (AECOPD), những bệnh nhân này không dung nạp NIV cho thấy sự cải thiện đáng kể về pH và PaCO2 khi NHF được sử dụng cùng với tốc độ dòng được chuẩn độ để đạt được khả năng dung nạp lớn nhất [42].
Trong một nghiên cứu dân số hỗn hợp gồm những bệnh nhân bị suy hô hấp cấp loại II (chủ yếu là viêm phổi và AECOPD) và thất bại hoặc không dung nạp COT, bao gồm NIV, sự cải thiện đáng kể PaCO2 sau 1 giờ điều trị NHF (50 L /min) đã được báo cáo. [43]. Những phát hiện tương tự cũng được báo cáo trong một nghiên cứu khác trên một quần thể hỗn hợp gồm 30 bệnh nhân bị suy hô hấp cấp tính tăng CO2 máu được điều trị bằng NHF. Tần số hô hấp được cải thiện trong 4 giờ đầu điều trị (mặc dù không có ý nghĩa thống kê) và pH được bình thường hóa trong vòng 24 giờ (7,28 so với 7,37, p = 0,02). Chỉ có 4 bệnh nhân (13,3%) không đáp ứng. Một NIV được yêu cầu và phần còn lại đã được đặt nội khí quản [44]. Một hạn chế của các nghiên cứu trên là không thể tổng quát kết quả từ các quần thể hỗn hợp ở bệnh nhân AECOPD. Tuy nhiên, NHF dường như có hiệu quả trong việc cải thiện các thông số lâm sàng và trao đổi khí ở những bệnh nhân suy hô hấp tăng CO2 mức độ trung bình, với tỷ lệ chấp nhận được ở những bệnh nhân không đáp ứng, những bệnh nhân cần hỗ trợ thông khí thêm.
Như đã nêu, NHF có khả năng làm giảm PaCO2 ở bệnh nhân COPD bằng cách cải thiện cơ học phổi và giảm công thở [45]. Một yếu tố quan trọng khác có thể dẫn đến giảm mức PaCO2 một cách độc lập là FiO2 được phân phối qua NHF ổn định hơn. Tuy nhiên, trong một nghiên cứu cắt ngang trên bệnh nhân COPD có đợt cấp tập trung vào việc bổ sung oxy chuẩn độ đến độ bão hòa oxy mao mạch ngoại biên baseline của bệnh nhân (SpO2), NHF (35 L / phút) so với ngạnh mũi chuẩn (thử nghiệm 30 phút) dẫn đến giảm đáng kể PtCO2 mặc dù mức độ phù hợp lâm sàng còn nghi ngờ vì sự khác biệt chỉ là 1,4 mmHg [46]. Không có bất kỳ sự khác biệt nào về FiO2 sau 30 phút, điều này cho thấy rằng sự khác biệt về PtCO2 giữa các phương pháp điều trị là do tác động sinh lý của NHF, chứ không phải do sự thay đổi cung cấp oxy. Một hạn chế của nghiên cứu là chỉ có 58% số người tham gia tăng CO2 và sự khác biệt lớn hơn về PtCO2 có thể dẫn đến nếu tất cả bệnh nhân đều bị tăng CO2. Ngoài ra, tốc độ dòng chảy cao hơn và sử dụng NHF trong thời gian dài hơn cũng có thể có ảnh hưởng lớn hơn đến PtCO2 [46].
Trong nỗ lực so sánh NHF với NIV, đây là tiêu chuẩn vàng cho bệnh nhân AECOPD tăng CO2 máu, Lee et al. [47], đã thực hiện một nghiên cứu tiền cứu ở những bệnh nhân bị AECOPD nặng và suy hô hấp tăng CO2 trung bình. Nhóm NHF cho kết quả cuối cùng tương tự so với nhóm NIV bao gồm tỷ lệ đặt nội khí quản (lần lượt là 25% và 27,3%) và tỷ lệ tử vong trong 30 ngày (lần lượt là 15,9% và 18,2%). Các điểm cắt khác, chẳng hạn như độ pH, PaO2 và PaCO2 cũng như thời gian điều trị trung bình không khác biệt có ý nghĩa thống kê giữa các nhóm.
Đánh giá siêu âm chức năng cơ hoành được thực hiện trong một nghiên cứu cắt ngang bao gồm 30 bệnh nhân COPD có suy hô hấp cấp tăng CO2 máu được điều trị NIV trong hơn 24 giờ [48]. Các bệnh nhân đã trải qua năm thử nghiệm 30 phút, thử nghiệm đầu tiên, thứ ba và thứ năm sử dụng NIV, và thử nghiệm thứ hai và thứ tư sử dụng liệu pháp oxy tiêu chuẩn hoặc NHF (50 L / phút). Liệu pháp oxy tiêu chuẩn dẫn đến sự gia tăng đáng kể độ dày cơ hoành trong khi điều trị NHF, độ dày cơ hoành vẫn không thay đổi, nghĩa là ít công thở hơn. Tuy nhiên, một nghiên cứu khác trên 12 bệnh nhân COPD gợi ý rằng việc đặt NHF trên 30 L / phút có thể dẫn đến tăng nỗ lực hít vào trong một nửa trường hợp, mặc dù nó làm giảm tần số hô hấp [49].
Một vai trò khác của NHF được Longhini và cộng sự nhấn mạnh là trong thời gian NIV gián đoạn, để bệnh nhân nghỉ ngơi, ăn uống và giao tiếp mà không bị giảm cơ học phổi [48]. Thật vậy, ngay cả ở những bệnh nhân COPD sau đặt nội khí quản, việc áp dụng NHF với tốc độ dòng cao nhất mà bệnh nhân dung nạp được, đã làm giảm đáng kể điều hòa thần kinh và công thở so với COT [50]. NHF cũng đã được báo cáo là có thể giữ cho
PaCO2 không bị biến động và làm giảm công thở bằng cách mở rộng tương tự như NIV, làm cho NHF trở nên lý tưởng trong thời gian NIV gián đoạn [51].
Ứng Dụng Thực Tế
Tóm tắt các tài liệu hiện có đã giúp chúng tôi đề xuất thuật toán sử dụng NHF sau đây cho bệnh nhân AECOPD và suy hô hấp tăng CO2 khi có NHF và được chọn làm thiết bị hỗ trợ thở ban đầu hoặc trong trường hợp không dung nạp NIV (Hình 1).
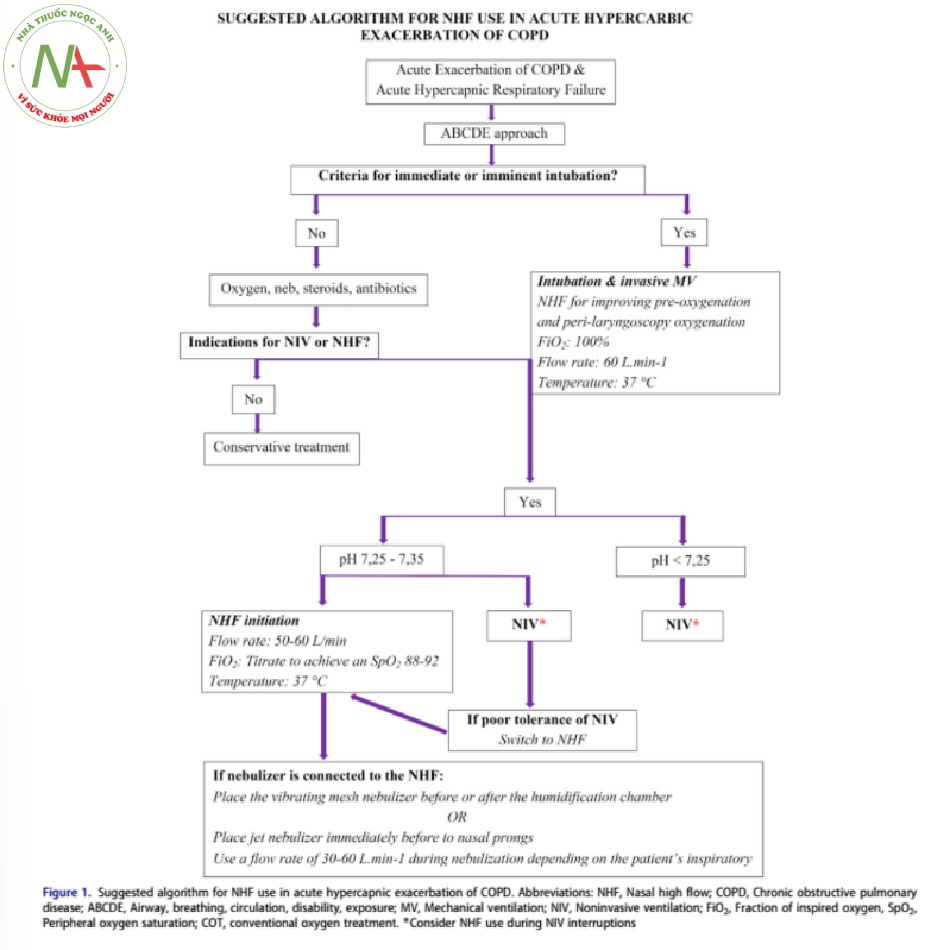
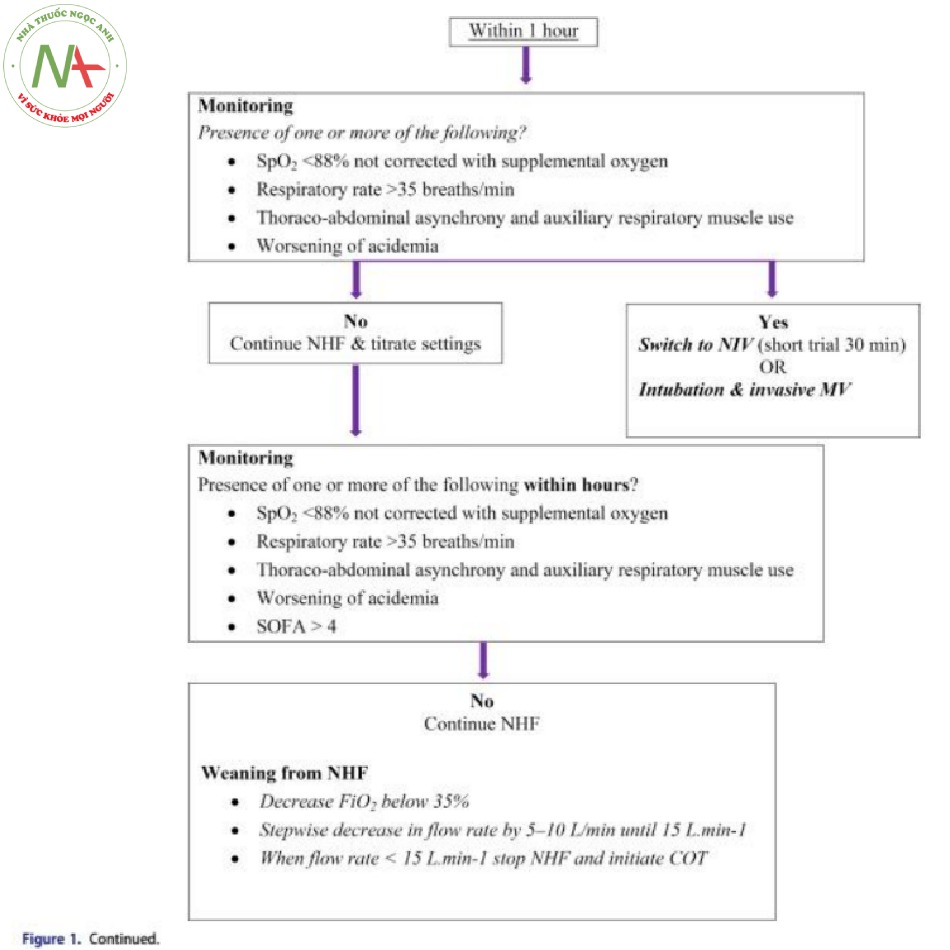
Đối với bệnh nhân nhập viện AECOPD và suy hô hấp type II, cần phải kiểm tra xem có chỉ định đặt nội khí quản tức thời hoặc sắp xảy ra và thở máy xâm nhập hay không, chẳng hạn như ngừng thở hoặc ngừng tim, huyết động không ổn định, rối loạn nhịp thất hoặc nhịp tim < 50 lần/phút với lơ mơ và giảm ý thức hoặc kích động không kiểm soát được bằng thuốc an thần [2]. Nếu có, và có thời gian để thiết lập NHF, NHF có thể được sử dụng để tạo tiền oxy và oxy hóa trong ngưng thở trong quá trình soi đèn đặt NKQ bằng cách sử dụng cài đặt thiết bị tối đa (tốc độ dòng chảy 60 L/min, FiO2: 100%) [34]. Cung cấp oxy lưu lượng cao trong khi đặt nội khí quản sẽ mở rộng cửa sổ ngưng thở bằng cách duy trì độ bão hòa oxy trong các giá trị an toàn hơn (> 90%) trong thời gian dài hơn với
tốc độ tăng CO2 chậm hơn [65]. Nó đã được chứng minh rằng NHF giảm thiểu các tác dụng phụ liên quan đến đặt nội khí quản như tốc độ và mức độ giảm độ bão hòa oxy, rối loạn nhịp tim và ngừng tim [66].
Đối với những bệnh nhân không cần đặt nội khí quản ngay lập tức hoặc sắp xảy ra và thở máy xâm nhập, nên điều trị ban đầu bằng oxy bổ sung nhằm mục đích SpO2 88– 92%, thuốc giãn phế quản, steroid (uống hoặc tiêm tĩnh mạch) và kháng sinh khi có dấu hiệu nhiễm khuẩn [2]. Trong vòng một giờ sau khi xử trí ban đầu, khó thở nặng với các dấu hiệu lâm sàng của mệt cơ hô hấp và tăng nhịp thở (sử dụng các cơ hô hấp phụ, chuyển động nghịch thường của bụng, co rút các khoang liên sườn) hoặc suy giảm trao đổi khí (pH ≤ 7,35 với PaCO2 ≥ 45 mmHg) cần hỗ trợ hô hấp với NIV hoặc NHF nên được đánh giá.
Khuyến cáo đối với bệnh nhân có pH < 7,25, NIV nên là lựa chọn điều trị đầu tay vì không có dữ liệu về hiệu quả của NHF trong AECOPD nặng. Đối với bệnh nhân suy hô hấp tăng CO2 máu và giá trị pH từ 7,25 đến 7,35, NHF có thể được sử dụng như một lựa chọn đầu tay hoặc như một liệu pháp thay thế nếu bệnh nhân không thể dung nạp NIV [45]. Dựa trên các nghiên cứu sinh lý [17,27,67–69], NHF được chứng minh là có tác dụng có lợi với tốc độ dòng chảy tối đa, do đó, người ta đề nghị rằng liệu pháp nên bắt đầu điều chỉnh thông số này trước (tốc độ dòng chảy ở 50–60 L/min), và sau đó nếu vẫn cần oxy bổ sung thì chuẩn độ FiO2 để duy trì oxy mục tiêu (SpO2: 88–92%) [20,21,24]. Điều quan trọng cần nhớ là các giá trị FiO2 thấp hơn thường được yêu cầu với NHF do sự phân phối hỗn hợp khí nhất quán hơn so với COT. Nhiệt độ nên được đặt ở 37°C. Các tiêu chí khác, chẳng hạn như không thể dung nạp NIV, giảm oxy máu đe dọa tính mạng ở những bệnh nhân không thể dung nạp NIV và không có khả năng loại bỏ dịch tiết không cho thấy chỉ định tuyệt đối đặt nội khí quản ngay lập tức và thở máy xâm nhập [2], vì những bệnh nhân này có thể được thử NHF liệu pháp. Hơn nữa, cần lưu ý rằng NHF có thể được sử dụng như một liệu pháp bổ sung trong thời gian nghỉ ngơi của NIV [48,70]. Sử dụng NHF thay vì COT đã được chứng minh là thoải mái hơn và thậm chí ngăn ngừa sự gia tăng tần số hô hấp, mức độ PaCO2 và khó thở khi sử dụng COT [51,71].
Trong quá trình điều trị NHF, thuốc giãn phế quản có thể được sử dụng thông qua máy phun khí dung dạng lưới rung được đặt trước hoặc sau buồng tạo ẩm [57,63] hoặc máy phun khí dung được đặt gần với ngạnh mũi nếu không có đầu nối thích hợp cho buồng tạo ẩm [62]. Nên sử dụng tốc độ dòng chảy từ 30 – 40 L /min trong quá trình cung cấp khí dung. Lưu lượng cao hơn là cần thiết cho bệnh nhân khó thở và lưu lượng thở vào cao hơn [57,59]. Nếu sử dụng máy phun sương phản lực, khí điều khiển máy phun khí dung cần được đặt thành 5 – 6 L /min [62].
Trong vòng một giờ kể từ khi bắt đầu NHF, cần kiểm tra sự xuất hiện hoặc tồn tại của các thông số có ý nghĩa tiên lượng thất bại, chẳng hạn như SpO2 < 88% không được điều chỉnh với bổ sung oxy, nhịp thở > 35 lần/phút, mất đồng bộ ngực-bụng và sử dụng cơ hô hấp phụ và tình trạng tăng CO2 đồng thời trở nên trầm trọng hơn cho thấy mệt cơ hô hấp thêm [72]. Sự hiện diện của một hoặc nhiều thông số này xác định những bệnh nhân không đáp ứng với NHF. Có thể cân nhắc đặt nội khí quản trực tiếp hoặc thử nghiệm NIV trong thời gian ngắn (30 phút) trước khi đặt nội khí quản cho bệnh nhân. Nếu không có thông số nào, có thể tiếp tục NHF và điều chỉnh cài đặt ban đầu dựa trên nhịp hô hấp của bệnh nhân (< 25–30 nhịp thở / phút), SpO2 (> 88–90%) và sự thoải mái và khả năng dung nạp của bệnh nhân. Nếu SpO2 mục tiêu, tần số hô hấp và công thở không đạt được, trong khi tốc độ dòng chảy < 60 L /min, thì nên tăng tốc độ dòng chảy thêm 5–10 L /min, vì tốc độ dòng chảy cao hơn giảm tải cho cơ hô hấp ở mức độ lớn hơn và cải thiện cơ học phổi bằng cách tăng thêm áp lực đường thở ở thì hít vào và thở ra.
Cần theo dõi chặt chẽ bệnh nhân đang điều trị bằng NHF để tránh các biến chứng không mong muốn về hô hấp và tim. Các thông số cần theo dõi thường xuyên và có ý nghĩa tiên lượng là những thông số được liệt kê trước đó. Ngoài các thông số hô hấp, sự hiện diện của rối loạn chức năng cơ quan khác được biểu hiện bằng điểm đánh giá suy cơ quan tuần tự > 4, rối loạn huyết động, cũng có liên quan đáng kể với thất bại NHF, cho thấy một nhóm bệnh nhân nặng hơn [73,74]. Khi các thông số lâm sàng và khí máu của bệnh nhân được cải thiện, nếu được cung cấp oxy bổ sung, trước tiên phải giảm oxy đến giá trị FiO2 <35%, tiếp theo là giảm tốc độ dòng chảy từng bước từ 5–10 L /min cho đến 15 L /min. Khoảng thời gian của những lần giảm này có thể dài hơn hoặc ngắn hơn dựa trên các thông số lâm sàng và khí máu của bệnh nhân. Khi bệnh nhân ổn định trong 1-2 giờ với lưu lượng <15 L/ min, nên ngừng NHF và có thể bắt đầu sử dụng mặt nạ Venturi hoặc thở oxy qua gọng mũi.
Kết Luận
NHF là một phương pháp hỗ trợ thông khí thân thiện với người sử dụng có thể hoạt động như một hình thức hỗ trợ hô hấp trung gian giữa hệ thống cung cấp oxy truyền thống và NIV. Nó cũng có thể được sử dụng thay thế cho NIV ở những bệnh nhân kém dung nạp và tuân thủ, hoặc kết hợp với NIV để giảm các tác dụng phụ liên quan đến mask thở. Mặc dù NHF dường như có thể làm giảm mức độ tăng CO2 máu, các nghiên cứu can thiệp lớn hơn là cần thiết để kiểm tra việc sử dụng NHF cho suy hô hấp cấp và mãn tính do tăng CO2 máu ở bệnh nhân COPD. Tuy nhiên cần phải xác định cách chọn lựa bệnh nhân tốt nhất và thực hiện các điều chỉnh (dòng khí, mức độ nhiệt và độ ẩm) để tối ưu hóa sự thoải mái. Hiện tại, ba thử nghiệm lâm sàng lớn (NCT03466385, NCT03214458, NCT03370666) đang được tiến hành nhằm làm rõ vai trò của NHF trong đợt cấp của COPD. Cho đến khi sự an toàn của NHF có thể được thiết lập trong các môi trường khác nhau, chúng tôi khuyến nghị rằng việc sử dụng NHF được giới hạn ở các khoa nơi bệnh nhân có thể được theo dõi chặt chẽ như khoa hô hấp hoặc chăm sóc đặc biệt của bệnh viện.
Câu hỏi lâm sàng
Nam 64 tuổi tới khoa cấp cứu vì khó thở tăng dần. 3 ngày trước anh ta có chảy nước mũi và ho mà anh ta nghĩ là liên quan tới cháu của anh ta. Anh ta có tiền sử hút thuốc lá 40 năm, khó thở khi gắng sức. Bệnh nhân cũng nói có phù mắt cá chân hai bên. Thăm khám thấy thừa cân nhẹ, rối loạn hô hấp nhẹ. Nghe phổi thấy ran rít hai bên và thì thở ra kéo dài. Số lượng bạch cầu: 14.500, Hemoglobin 16 g/dL.
Khí máu động mạch: pH 7.34, PaO2 68 mmHg, PaCo2 65 mmHg. Đâu là lí giải hợp lý nhất cho việc không có dấu hiệu toan hóa ở bệnh nhân này?
- Sự trao đổi Clo ở màng tế bào hồng cầu (Erythrocyte chloride shift).
- Tăng khoảng chết thông khí.
- Tăng thông khí/ phút.
- Sự co mạch phổi.
- Sự bù trừ của ống thận.
Đáp án đúng là E: Bệnh nhân này có khả năng mắc COPD (tiền sử hút thuốc lá lâu, triệu chứng hô hấp tăng dần có ran rít và thì thở ra kéo dài, phù gợi ý khả năng mắc tâm phế mạn) biểu hiện với khó thở tăng dần và dấu hiệu tăng Co2 máu (hypercapnia) – PaCo2 65 mmHg. Bệnh nhân có giảm thông khí mạn do COPD, hội chứng giảm thông khí bởi béo phì, hoặc nguyên nhân thần kinh cơ thường gây tăng PaCo2 từ từ dẫn tới nhiễm toan hô hấp mãn (chronic respiratory acidosis) để bù trừ thì thận tăng tái hấp thu Hco3 tạo nhiễm kiềm chuyển hóa thứ phát. Với tình trạng đợt cấp của COPD thì PaCo2 có thể tăng nhiều như ở bệnh nhân này.
Thông thường, giá trị pH mong đợi ở bệnh nhân có tăng PaCo2 cấp từ 40mmHg (thông thường) lên 65mmHg thì pH đạt khoảng 7.2 (pH giảm 0.08 cho mỗi 10mmHg tăng PaCo2). pH của bệnh nhân là 7.34 gợi ý rằng để có sự bù trừ cho tình trạng tăng PaCo2 mãn lớn này thì thận cần có thời gian. Ngược lại với sự bù trừ của hô hấp thì sự bù trừ của chuyển hóa bởi thận diễn ra trong khoảng 48h và chỉ trong tình trạng mạn tính. Sự bù trừ chuyển hóa không làm bình thường hóa hoặc điều chỉnh quá mức pH (mất thăng bằng kiềm toan nguyên phát không hoàn toàn được bình thường hóa bởi đáp ứng bù trừ).
Đáp án A: HCo3- đi ra và Cl đi vào hồng cầu là cách di chuyển của Co2 đi khắp cơ thể. Nó là đáp ứng ban đầu với nhiễm toan hô hấp nhưng có ảnh hưởng nhỏ vs pH so với bù trừ tại thận.
Đáp án B: Tăng khoảng chết thông khí là nguyên nhân chính gây tăng PaCo2 ở COPD và làm tệ hơn sự nhiễm toan hô hấp.
Đáp án C: Thông khí phổi/phút là tích của thể tích thông khí và tần số hô hấp. Cơ thể tăng thông khí phút làm giảm PaCo2 và bù trừ cho nhiễm toan chuyển hóa. Do mắc COPD nên bệnh nhân này không có khả năng tăng thông khí/phút.
Đáp án D: Sự co mạch phổi dẫn tới giảm oxi phế nang. Nó có thể bình thường hóa các shunt và sự bất tương hợp trao đổi khí-tưới máu tại phổi nhưng không bù trừ khi nhiễm kiềm hô hấp.
Tổng kết: Cơ thể bù trừ đối với tăng PaCo2 mạn bằng cách tăng tái hấp thu Hco3 tại thận và tạo ra nhiễm toan chuyển hóa thứ phát.

