Tác giả: Nguyễn Anh Dũng, Phạm Thị Tuyết Dung
Bài viết HỒI SỨC HUYẾT ĐỘNG Ở BỆNH NHÂN COVID-19 được trích từ chương 10 trong phần 3 “Hồi sức ở bệnh nhân nặng và nguy kịch” sách Chẩn đoán và điều trị COVID-19, Nhà xuất bản Đại học Quốc gia Hà Nội.
1. ĐẠI CƯƠNG
Hồi sức huyết động có một vai trò quan trọng trong quá trình điều trị bệnh nhân COVID-19 đặc biệt trên các bệnh nhân có biến chứng hội chứng suy hô hấp cấp tiến triển (ARDS). Một nghiên cứu trên 138 bệnh nhân nhập viện tại Vũ Hán Trung Quốc các tác giả nhận thấy những bệnh nhân nhập đơn vị hồi sức (ICU) có tỷ lệ sốc cao hơn một cách có ý nghĩa so với các bệnh nhân không nhập ICU. Hiện nay có nhiều phương pháp theo dõi huyết động bao gồm các biện pháp không xâm lấn như đo áp lực tĩnh mạch trung tâm (CVP), đánh giá đường kính tĩnh mạch chủ dưới và biện pháp xâm lấn như đo PiCCO, đặt catheter Swan-Ganz. Lựa chọn liệu pháp thăm dò huyết động nào và xử trí sao cho cho phù hợp sẽ phụ thuộc vào điều kiện trang thiết bị của mỗi đơn vị ICU.
Nguyên lý cơ bản để tối ưu hoá huyết động là tập trung cải thiện cung cấp oxy cho các mô bằng cách khôi phục trở lại thể tích tuần hoàn thoả đáng, tái hồi lại tưới máu bằng cách tối ưu hoá cung lượng tim và áp lực động mạch hệ thống, đảm bảo khả năng vận chuyển oxy đầy đủ bằng cách cải thiện tối ưu nồng độ hemoglobin và độ bão hoà oxy của hemoglobin.
2. CƠ CHẾ RỐI LOẠN HUYẾT ĐỘNG TRONG COVID 19
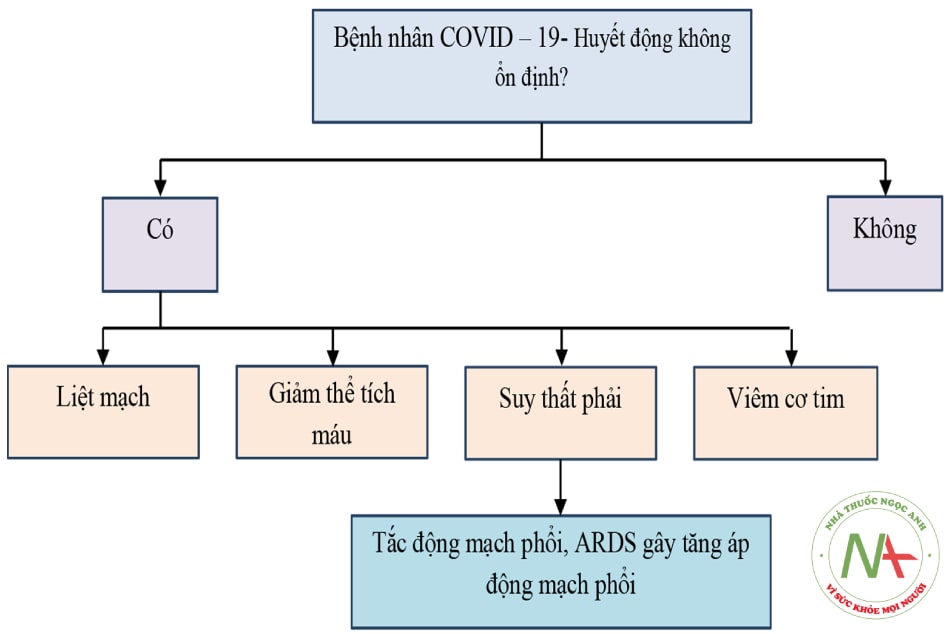
Bệnh nhân COVID-19 có tình trạng huyết động không ổn định là do các nguyên nhân sau:
- Viêm cơ tim do
- Tổn thương cơ tim do
- Giảm thể tích do sốt.
- Tình trạng thiếu oxy, tụt huyết áp kéo dài gây ra tổn thương tế bào cơ
- Liệt mạch, suy thất phải.
- Rối loạn nhịp tim do rối loạn điện giải như kali, Mg mà không được theo dõi kịp thời.
- Sốc nhiễm khuẩn.
- Tắc động mạch phổi lớn.
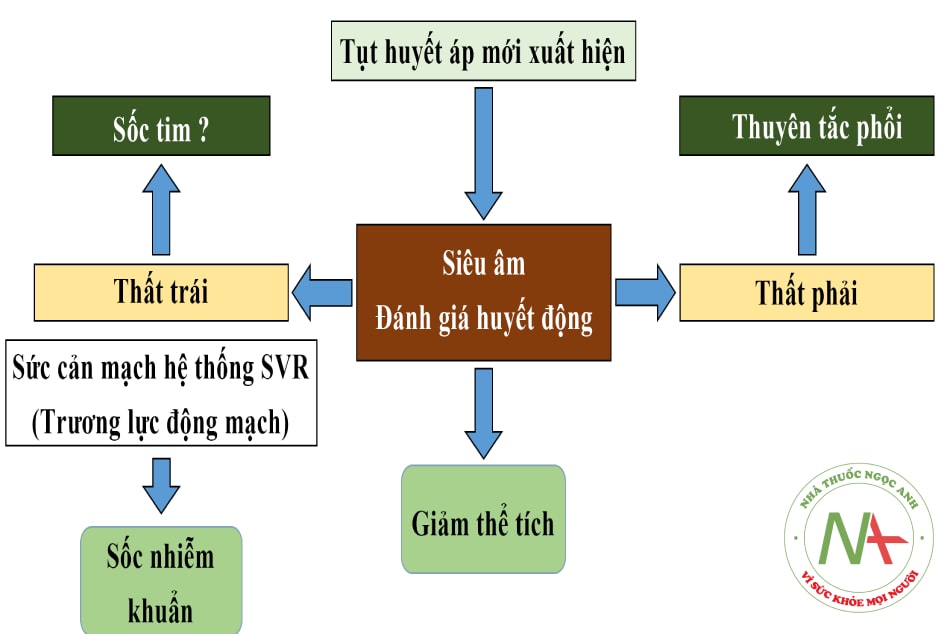
- Hình 10.1. Cơ chế rối loạn huyết động ở bệnh nhân COVID-19
3. CÁC BIỆN PHÁP THĂM DÒ HUYẾT ĐỘNG
3.1. Doppler qua thực quản
- Đo cung lượng tim bằng Doppler qua thực quản dựa trên nguyên tắc đo tốc độ dòng máu qua động mạch chủ xuống. Kỹ thuật này đòi hỏi phải đặt một đầu thu phát sóng âm vào thực quản và xoay đầu dò để thu được tín hiệu tốt nhất. Tốc độ dòng máu sẽ được đo dựa trên các thay đổi tần số của sóng âm phản hồi. Thể tích tống máu (SV) ước tính từ lấy đạo hàm của tích phân tốc độ thời gian nhân với diện tích mặt cắt ngang của động mạch chủ. Sau khi tính được thể tích tống máu (SV), cung lượng tim (CO) được xác định bằng công thức:
Cung lượng tim (CO) = Tần số tim x Thể tích tống máu (SV)
Ngoài thông số thể tích tống máu (SV) và cung lượng tim (CO). Doppler qua thực quản có thể cung cấp được thông số về tiền gánh được gọi dưới tên thời gian dòng chảy được hiệu chỉnh (FTc). FTc là thời gian dòng chảy thì tâm thu được hiệu chỉnh theo tần số tim. Giá trị bình thường biến đổi trong khoảng 330-360 ms. Tốc độ đỉnh hoặc tối đa là chiều cao của dạng sóng và có thể được sử dụng như một thông số để đánh giá tình trạng co bóp của cơ tim. Giới hạn bình thường đối với tốc độ dòng đỉnh giảm dần theo tuổi của bệnh nhân.
Theo dõi cả FTc và vận tốc dòng đỉnh giúp hồi sức tối ưu cho bệnh nhân trong nhiều tình huống lâm sàng phức tạp. Ví dụ: trong sốc giảm thể tích, theo dõi trên monitor sẽ thấy phần đáy dạng sóng biểu diễn hẹp với tình trạng giảm FTc tương ứng (< 330 ms) và tốc độ dòng đỉnh tương đối bình thường. Truyền dịch sẽ làm tăng phần đáy của dạng sóng biểu diễn hoặc kéo dài FTc. Nếu tình trạng bệnh lý nền gây ức chế co bóp cơ tim, dạng sóng ban đầu sẽ cho thấy có tốc độ dòng đỉnh thấp và FTc bình thường. Điều trị bằng thuốc tăng co bóp có tim sẽ cải thiện tốc độ đỉnh hoặc làm tăng khả năng co bóp cơ tim trong các tình huống này.
Thiết bị này dễ diễn giải và dễ cài đặt, Đầu dò được đặt qua đường miệng và luồn xuống 35-40 cm tới khoảng vùng giữa ngực. Có thể lưu Doppler thực quản tại chỗ trong vòng 2 tuần, song điều quan trọng là phải kiểm tra vị trí đầu dò để đảm bảo có được tín hiệu tối ưu. Thiết bị này cũng rất an toàn khi sử dụng cho hầu hết các đối tượng, kể cả các bệnh nhân bị rối loạn đông máu.
Một hạn chế đối với kỹ thuật này là sử dụng ở bệnh nhân được an thần và thở máy. Thể tích tống máu (SV) được ước tính từ tỷ lệ dòng chảy đi vào động mạch chủ xuống. Một điều được thừa nhận là có tỷ lệ dòng chảy hằng định 70/30 giữa động mạch chủ xuống (70%) và động mạch cánh tay đầu và hệ mạch vành (30%). Diện tích thiết diện cắt ngang của động mạch chủ được ước tính dựa vào một biểu đồ toán học sử dụng các đặc điểm của bệnh nhân (tuổi, giới, trọng lượng cơ thể). Vì vâỵ, nếu có bệnh lý của động mạch chủ, giá trị tuyệt đối tính được từ các dữ liệu nói trên có thể sẽ không chính xác. Khi có bất kỳ một trong các yếu tố kể trên đều rất khó thu được tín hiệu ổn định và khi có tình trạng gù vẹo cột sống hoặc vữa xơ động mạch nặng có thể gây biến đổi góc cố định của đầu dò Doppler.
Theo dõi cung lượng tim bằng Doppler qua thực quản rất hữu ích khi sử dụng thiết bị để tiến hành đo đạc liên tục nhằm phát hiện chiều hướng thay đổi và đáp ứng với điều trị.
3.2. Phương pháp hoà loãng nhiệt qua phổi
Trái ngược với kỹ thuật hoà loãng nhiệt của đặt catheter động mạch phổi, kỹ thuật hoà loãng nhiệt qua phổi thực hiện việc đo cung lượng tim bằng cách phát hiện liều bolus nước lạnh ở hệ thống động mạch ngoại vi. Nước lạnh được tiêm qua catheter tĩnh mạch trung tâm và sẽ được một catheter với đầu có bộ phận cảm nhiệt đặt vào động mạch quay nách hoặc động mạch đùi để nhận cảm.
Tính toán cung lượng tim bằng phương trình Stewart-Hamilton tương tự như trong phương pháp hoà loãng nhiệt của đặt catheter động mạch phổi. Lợi ích của kỹ thuật hoà loãng nhiệt qua phổi là kỹ thuật này có khả năng cung cấp kết quả cung lượng tim cũng như các chỉ dấu khác đánh giá tiền gánh (ví dụ: thể tích cuối tâm trương tổng thể hay của bốn buồng tim), thể tích máu trong lồng ngực và lượng nước trong phổi ngoài lòng mạch, song lại không cần phải đặt catheter động mạch phổi.
Có thể sử dụng các đo đạc bằng phương pháp hoà loãng nhiệt không chỉ để đo dòng chảy mà còn để đo thể tích mà dòng chảy qua thể tích này được đo đạc (tức là từ điểm tiêm tới điểm phát hiện được thể tích nước lạnh qua).
- Thể tích nhiệt trong lồng ngực = Cung lượng tim (CO) x Thời gian di chuyển trung bình của chất chỉ thị nhiệt.
- Thể tích nhiệt của phổi = Cung lượng tim (CO) x Thời gian dốc xuống của chất chỉ thị nhiệt.
- Thể tích cuối tâm trương của bốn buồng tim = ITTV – PTV và cung cấp một chỉ dấu đánh giá tiền gánh với mức độ tin cậy vừa phải.
- ITBV = 1,25 x GEDV – 28,4 ml
- Lượng nước trong phổi ngoài lòng mạch = ITTV – ITBV và có thể được sử dụng để giúp hướng dẫn truyền dịch hoặc để phân biệt giữa phù phổi do tăng áp lực thuỷ tĩnh với tình trạng tổn thương phổi cấp. Lợi ích lâm sàng của thông số đánh giá lượng nước trong phổi ngoài lòng mạch (EVLW) còn chưa thật rõ ràng. Tăng EVLW có thể được sử dụng như một chỉ dẫn cho tình trạng phù phổi sớm. Người ta cũng thấy là tỷ lệ tử vong sẽ cao hơn khi giá trị của EVLW tăng cao hơn 15 mL/kg.
3.3. Phân tích dạng sóng mạch
Phương pháp phân tích dạng sóng mạch sử dụng dạng sóng áp lực động mạch để dự đoán dòng máu trong lòng mạch và để tính toán thể tích tống máu (SV). Các hệ thống hiện có trên thị trường như: PiCOO, Pulse CO và Flo Trac/Vigileo… Phương pháp hoà loãng nhiệt được sử dụng trong thiết bị PiCCO. Lithium là chất chỉ thị đối với Pulse CO, trái lại thiết bị Flo Trac/ Vigileo không cần sử dụng bất kì kỹ thuật hoà loãng cao.
Phân tích dạng sóng mạch đòi hỏi phải đặt đường truyền động mạch, đối với thiết bị PiCCO hoặc PulseCO cần đặt thêm catheter tĩnh mạch trung tâm để hiệu chuẩn. Phân tích dạng sóng mạch giúp theo dõi liên tục cung lượng tim trái ngược với kỹ thuật đặt catheter động mạch phổi chỉ cung cấp các kết quả không liên tục.
Đo cung lượng tim bằng cách phân tích hình dạng sóng dễ bị sai số. Những thiết bị này bị hạn chế bởi sự thay đổi động trong sức cản của mạch và điều này sẽ cần chuẩn độ lại khi sử dụng. Thường có khuyến cáo là phải tiến hành chuẩn độ lại thiết bị PiCCO và LiDCO sau mỗi 8 giờ sử dụng. Thiết bị Flo Trac/Vigileo không cần phải chuẩn độ song các thông số đo được có thể sẽ không còn tin cậy ở bệnh nhân giảm sức cản hệ thống như sepsis. Hiệu suất của các thiết bị này cũng bị ảnh hưởng khi có tình trạng hở van động mạch động chủ, phình động mạch chủ ngực và khi dạng sóng bị bẹt. Bên cạnh đó, các thiết bị có thể cung cấp các thông tin cực kỳ hữu ích như các thay đổi áp lực động mạch và thay đổi thể tích tống máu ở bệnh nhân được thông khí nhân tạo điều khiển hoàn toàn (không có bất kỳ một nỗ lực thở tự nhiên nào), với nhịp xoang bình thường và khi thở máy được cài đặt thể tích lưu thông thoả đáng.
3.4. Đáp ứng truyền dịch
- Đáp ứng truyền dịch: Là khả năng của tim làm tăng đáng kể thể tích nhát bóp (SV) hoặc cung lượng tim (CO) khi truyền thêm dịch.
- Tuy nhiên không phải tất cả các bệnh nhân khi có rối loạn huyết động đều đáp ứng với liệu pháp truyền dịch, theo nghiên cứu của Fréderic và Teboul trên tạp chí CHEST 2002 cho thấy chỉ có 52% bệnh nhân đáp ứng với truyền dịch. Các tác giả nhận thấy những bệnh nhân không đáp ứng có nguy cơ dẫn tới phù phổi và DO2 giảm.
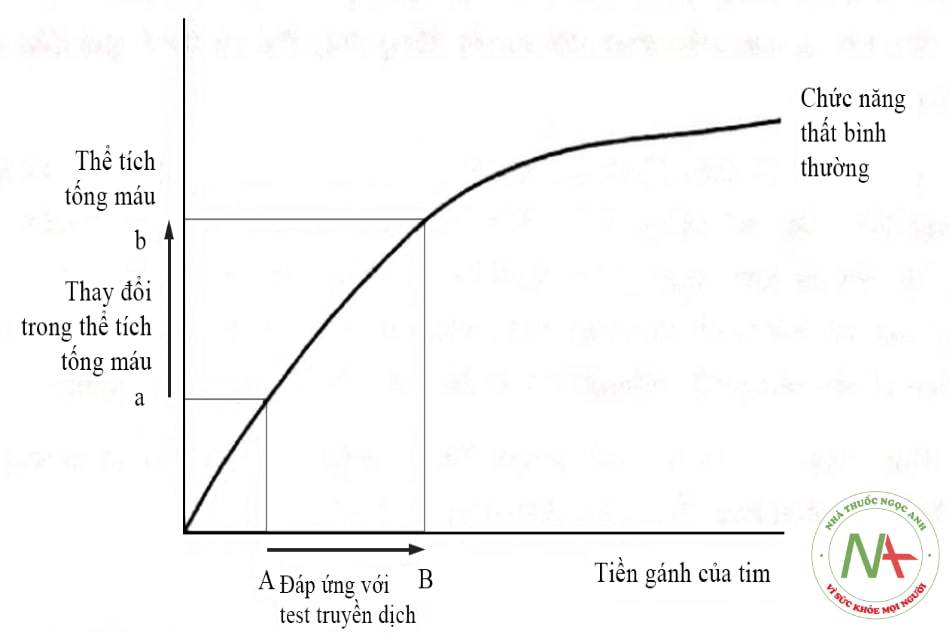
- Các chỉ dấu tĩnh để đánh giá đáp ứng truyền dịch: Hình 2 và hình 10.3 giúp cắt nghĩa khái niệm đáp ứng với truyền dịch bằng cách mô tả lại đường biểu diễn Frank Starling đối với một quả tim bình thường. Các thầy thuốc lâm sàng thường sử dụng các thông số huyết động tĩnh mà chủ yếu là áp lực trong lòng mạch, để dự kiến đối tượng bệnh nhân nào sẽ có được lợi ích khi tiến hành test truyền dịch.
- Hình 10.2. Đáp ứng với truyền dịch: Tăng thể tích tống máu khi đáp ứng với test truyền dịch ở bệnh nhân có chức năng 2 thất bình thường và ở phần dốc (tiền gánh thấp) của đường cong Frank Starling.
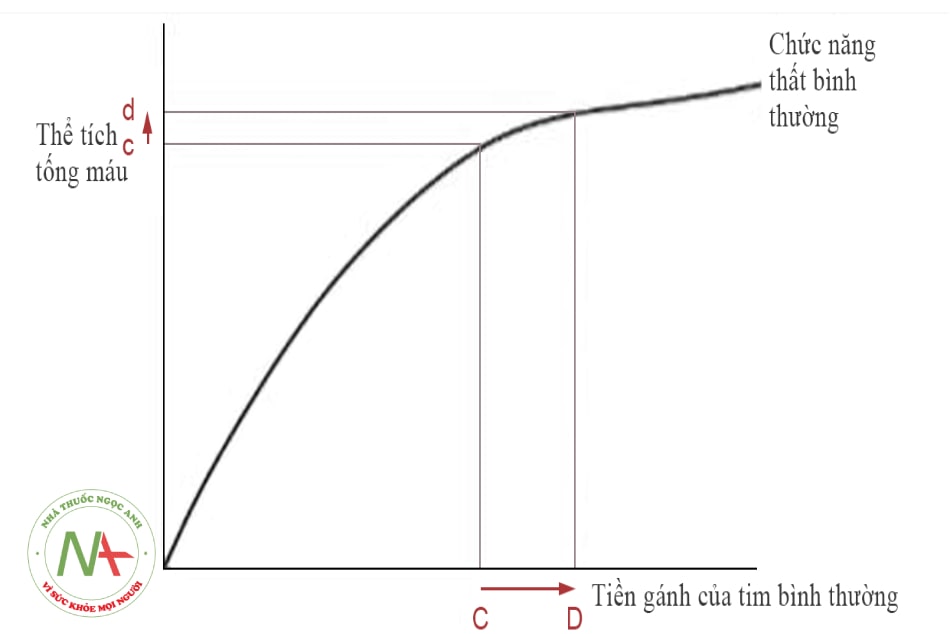
- Hình 10.3. Không đáp ứng với truyền dịch: Thể tích tống máu tăng không đáng kể mặc dù tiến hành bồi phụ thể tích ở bệnh nhân có chức năng 2 thất bình thường trên phần nằm ngang (tiền gánh cao) của đường cong Frank Starling.
- Dự đoán đáp ứng truyền dịch có vai trò quan trọng trong hồi sức bệnh nhân nặng có rối loạn huyết động nói chung và bệnh nhân COVID-19 nói riêng. Các thông số giúp đánh giá đáp ứng truyền dịch gồm có thông số tĩnh và thông số động.
- Thông số tĩnh đánh giá đáp ứng truyền dịch:
- CVP (Áp lực tĩnh mạch trung tâm).
- IVC (Đường kính tĩnh mạch chủ dưới).
- PAOP (Áp lực mao mạch phổi bít).
- GEDV (Thể tích cuối tâm trương toàn bộ).
- Thông số động đánh giá đáp ứng truyền dịch:
- PPV (Biến thiên áp lực mạch).
- SPV (Biến thiên huyết áp tối đa).
- SVV (Biến thiên thể tích nhát bóp).
- Thông số tĩnh đánh giá đáp ứng truyền dịch:
3.5. Áp lực tĩnh mạch trung tâm (CVP)
Áp lực tĩnh mạch trung tâm được sử dụng rộng rãi tại các khoa hồi sức để đưa ra các quyết định lâm sàng cho tình trạng thể tích, do bệnh nhân thường được đặt đường truyền tĩnh mạch trung tâm. Tuy nhiên, không có mối liên quan giữa áp lực tĩnh mạch trung tâm và thể tích máu lưu hành.
Áp lực tĩnh mạch trung tâm là áp lực trong lòng mạch ở các tĩnh mạch lớn trong lồng ngực, được đo theo các mức tương ứng với áp suất khí quyển. Áp lực này cung cấp một giá trị ước tính cho áp lực nhĩ phải do lý tưởng là nó phải được đo ở vùng nối giữa tĩnh mạch chủ trên và nhĩ phải.
Có nhiều yếu tố có ảnh hưởng tới áp lực tĩnh mạch trung tâm như thể tích máu, trương lực mạch và chức năng và độ giãn nở thất phải, bệnh van ba lá, nhịp tim, áp lực trong lồng ngực (nỗ lực hô hấp và PEEP) cũng như tư thế của bệnh nhân. Khả năng là một giá trị áp lực tĩnh mạch trung tâm bất kỳ dự đoán chính xác đáp ứng với truyền dịch chỉ đạt mức 56%.
Giảm áp lực tĩnh mạch trung tâm là dấu hiệu tương đối muộn của tình trạng thiếu hụt thể tích trong lòng mạch nhất là ở bệnh nhân có trương lực thành mạch bình thường.
Vì những lý do trên, không nên dựa vào duy nhất vào áp lực tĩnh mạch trung tâm để hướng dẫn quyết định xử trí truyền dịch, mà nên kết hợp với nắm vững sinh lý bệnh nền và các thông số huyết động bổ sung của bệnh nhân.
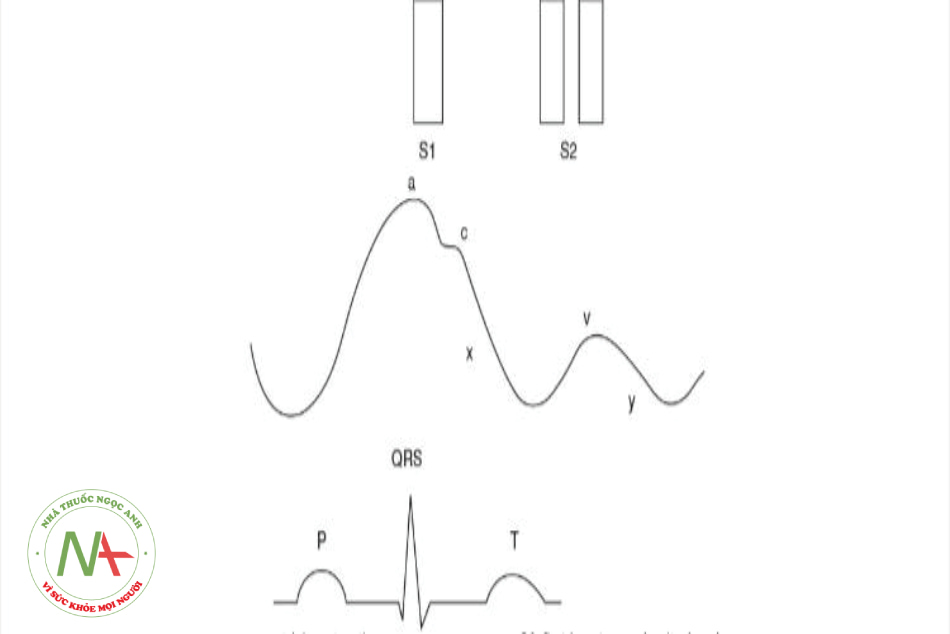
Sóng a: co cơ nhĩ
Sóng c: đóng van 3 lá và tăng áp lên nhĩ phải hoặc sóng dội từ động mạch cảnh.
Sóng v: đổ đầy nhĩ Sóng y: Tháo rỗng nhĩ
S1: Tiếng T1, đóng van hai lá và van ba lá
S2: Tiếng T2 đóng van động mạch phổi và van động mạch chủ
Sóng P: Khử cực nhĩ
Phức hợp QRS: Khử cực thất
Sóng T: Tái cực thất
- Hình 10.4: Đường ghi áp lực tĩnh mạch trung tâm bình thường
Đường ghi áp lực tĩnh mạch trung tâm thường có dạng đặc trưng trong các tình trạng bệnh lý khác nhau:
- Mất sóng a trong rung nhĩ.
- Các sóng a lớn (dạng sóng đại bác) trong tình trạng phân ly nhĩ thất có thể xảy ra do tình trạng cơ tim nhĩ đối kháng lại van nhĩ thất đã đóng kín.
- Sóng cv lớn trộn lẫn với nhau được gặp ở bệnh nhân hở van ba lá.
- Hẹp van 3 lá sẽ gây ra các sóng a khổng lồ và sườn xuống của sóng y giảm đi.
- Trong viêm màng ngoài tim co thắt, sườn xuống của sóng y nổi trội và dốc hơn trong thì hít vào.
3.6. Vai trò siêu âm tĩnh mạch chủ dưới (IVC)
- Phụ thuộc vào người làm siêu âm.
- Giá trị đường kính IVC có tương quan với áp lực nhĩ phải (RAP).
- Các yếu tố ảnh hưởng: Béo phì, tăng áp lực lồng ngực do ứ khí phổi, tràn khí màng phổi, bụng chướng.
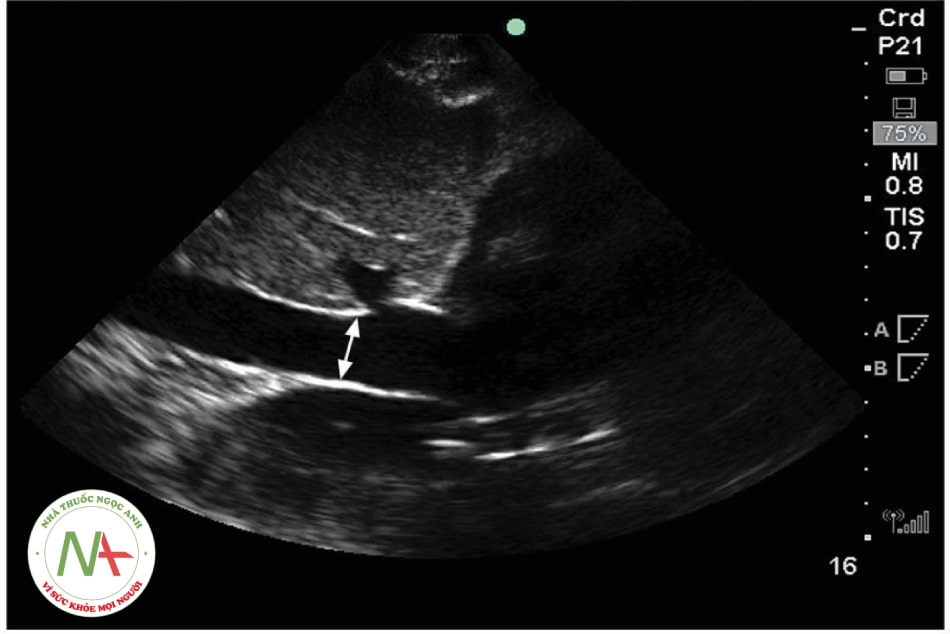
- Hình 10.5. Hình ảnh siêu âm tĩnh mạch chủ dưới
3.7. Vai trò áp lực mao mạch phổi bít (PAOP)
- Đo được bằng cách đặt catheter tại nhánh động mạch phổi (Pulmonary Artery Catheter – PAC/Catheter Swan-Ganz).
- Có giá trị bằng áp lực thất trái cuối tâm trương (LVEDP) nếu giả định sức cản mạch phổi bình thường và không có hẹp van 2 lá.
- Tương tự áp lực tĩnh mạch trung tâm (CVP), PAOP bị ảnh hưởng bởi nhiều yếu tố: thay đổi độ giãn nở của cơ tim (sepsis, thiếu máu cục bộ cơ tim, đái tháo đường), quá tải thất phải, bệnh lý màng ngoài tim, tăng áp lực lồng ngực do thông khí áp lực dương.
- Một số biến chứng trong quá trình đặt và rút catheter: Rối loạn nhịp tim, nhồi máu phổi, kẹt ống thông, tổn thương động mạch phổi.
3.8. Vai trò GEDVI (Global end-diastolic volume index)
- Global end-diastolic volume index là ước tính thể tích của tổng lượng máu trong các buồng
- GEDVI có thể tính được bằng phương pháp hòa loãng nhiệt xuyên phổi.
- Theo nghiên cứu của Michard và cộng sự, GEDVI có sự tương quan chặt với sự thay đổi thể tích nhát bóp (∆SV) với hệ số tương quan r = 0,72 và p = 0,001; trong khi đó sự thay đổi CVP có tương quan không chặt với ∆CI. Do đó ở những bệnh nhân sốc nhiễm khuẩn, GEDVI là chỉ số đáng tin cậy hơn so với CVP để đánh đáp ứng truyền dịch.
- Theo Michard và cộng sự, GEDVI < 500 dự đoán bệnh nhân có đáp ứng truyền dịch với độ nhạy là 100%, GEDVI ở mức 550 (ml/m2) dự đoán có đáp ứng truyền dịch với độ nhạy là 90%, GEDVI ở mức 600 (ml/m2) dự đoán có đáp ứng truyền dịch với độ nhạy là 77%.
- Ưu điểm của việc sử dụng GEDVI để đánh giá đáp ứng truyền dịch là: không bị ảnh hưởng bởi áp lực đường thở và PEEP, tình trạng tăng áp lực ổ bụng và bệnh lý tim phổi trước đó. Tuy nhiên để đo được GEVDI chúng ta cần coi PiCCO là một thủ thuật xâm lấn tối thiểu, vẫn có nguy cơ nhiễm khuẩn, bị ảnh hưởng bởi những dòng shunt trong tim, nguy cơ chảy máu ở những bệnh nhân bị rối loạn đông máu nặng.
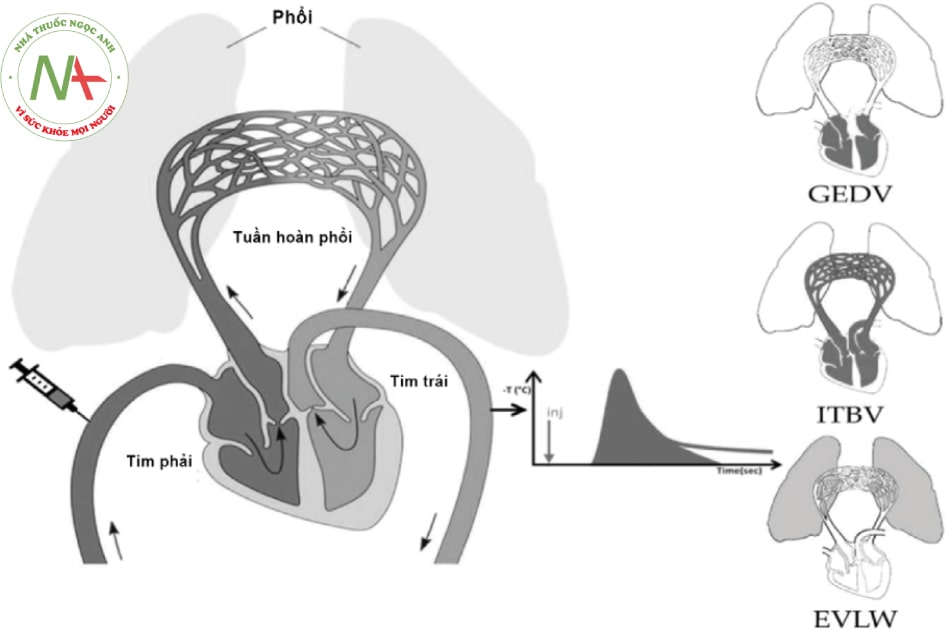
- Hình 10.6. Đánh giá huyết động bằng phương pháp hòa loãng nhiệt
Chú thích: GEDVI (Global end-diastolic volume index): Thể tích của tổng lượng máu trong các buồng tim.; ITBV (Intra-Thoracic Blood Volume): Thể tích máu trong lồng ngực; EVLW(Extravascular lung water): Lượng dịch ngoài mạch phổi.
3.9. Vai trò SVV và PPV
Biến đổi áp lực mạch (PPV) hoặc biến đổi thể tích tống máu (SVV) > 10-12% dự kiến bệnh nhân có thể đáp ứng với truyền dịch đạt độ nhạy và độ đặc hiệu cao.
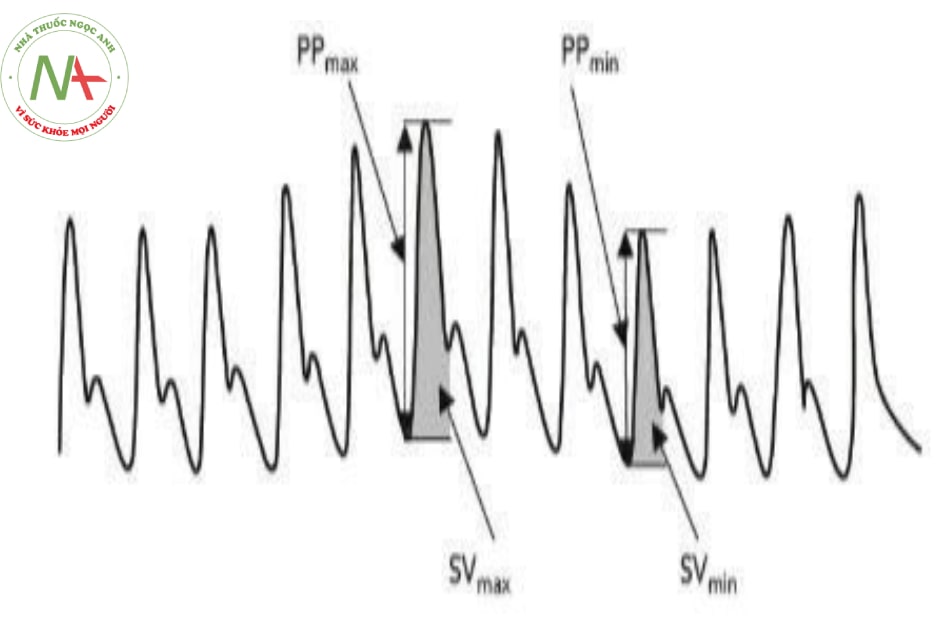
- Hình 10.7. Đường ghi áp lực động mạch cho thấy có tình trạng biến đổi áp lực mạch (PPV) và biến đổi thể tích tống máu (SVV)
Biến đổi áp lực mạch = 100 x (PPVmax – PPVmin)/(PPVmax+ PPVmin)/2 Biến đổi thể tích tống máu = 100 x (SVVmax – SVVmin)/(SVVmax + SVVmin)/2 Trong đó:
- PPV: Biến đổi áp lực mạch.
- SVV: Biến đổi thể tích tống máu.
3.10. Các nghiệm pháp đánh giá đáp ứng với truyền dịch
Nâng cao chân thụ động (Passive Leg Raise):
- Là một test truyền dịch tự thân vì vậy không cần phải truyền thêm bất kì một chút dịch nào và tránh được tác hại của sự quá tải dịch. Theo Jean– Louis Teboul và cộng sự thì khi thực hiện nghiệm pháp nâng chân thụ động sẽ huy động 300ml–500ml máu từ nửa dưới cơ thể trở về tim phải.
- Các hiệu ứng huyết động của nghiệm pháp nâng chân thụ động được đánh giá trực tiếp bằng sự thay đổi của cung lượng tim (∆CO), chỉ số tim (∆CI), chỉ số thể tích nhát bóp (∆SVI). Các kỹ thuật để đo các thay đổi huyết động được áp dụng như phân tích sóng mạch, siêu âm tim, siêu âm Doppler qua thực quản, Các thông số huyết động cần được theo dõi liên tục trước–trong–và sau khi làm nghiệm pháp vì những thay đổi về huyết động gây ra bởi nghiệm pháp nâng chân thụ động sẽ chỉ xảy ra trong khoảng từ 1–2 phút sau khi thực hiện nghiệm pháp.
- Nếu tuân thủ đầy đủ các nguyên tắc trên thì nghiệm pháp nâng chân thụ động sẽ là một thử nghiệm đáng tin cậy để đánh giá đáp ứng truyền dịch ở bệnh nhân sốc nhiễm khuẩn. Với những ưu thế đó, nghiệm pháp nâng chân thụ động được xem có thể thay thế cho phương pháp đánh giá đáp ứng truyền dịch cổ điển bằng cách truyền dịch tinh thể vì điều đó làm tăng nguy cơ quá tải dịch.
- Các bước thực hiện nghiệm pháp nâng chân thụ động:
- Bước 1: Bệnh nhân ở tư thế đầu cao 45° trong vòng 2 phút, mục đích để dồn toàn bộ lượng máu từ nửa trên cơ thể về tim và sau đó xuống nửa dưới cơ thể theo chu chuyển của vòng tuần hoàn. Khi làm động tác này sẽ giúp hiệu quả của nghiệm pháp nâng chân thụ động sau đó sẽ tốt hơn vì lượng máu dự trữ ở nửa dưới cơ thể sẽ lớn hơn. Đối với những trường hợp thể tích tuần hoàn thiếu hụt quá nhiều (bệnh nhân sốc nhiễm khuẩn có tình trạng tiêu chảy mất nước không được bù dịch thỏa đáng trước đó, bệnh nhân nhẹ cân có chỉ số BMI thấp <18 kg/m2) thì lượng máu huy động từ nửa dưới cơ thể không đủ 300-500ml máu, do vậy kết quả đánh giá đáp ứng truyền dịch có thể sẽ thiếu chính xác.
- Bước 2: Chuyển bệnh nhân về tư thế đầu bằng sau đó nâng cao chân bệnh nhân bằng giường tự động điều chỉnh tư thế (điều kiện lý tưởng nhất) hoặc có thể dùng hai tay hoặc đệm cứng nghiêng 45° để nâng chân bệnh nhân (đảm bảo bệnh nhân được an thần, giãn cơ thở hoàn toàn theo máy, tránh các kích thích gây đau, tránh các kích thích giao cảm có thể gây tăng nhịp tim). Tư thế nâng cao hai chân 45° được duy trì trong thời gian 2 phút. Việc giữ đầu và ngực của bệnh nhân trong tư thế nằm ngang khi thực hiện nghiệm pháp nâng chân thụ động giúp tránh những nguy cơ của trào ngược dịch dạ dày, viêm phổi do hít. Các thông số huyết động sẽ được đo bằng thiết bị thăm dò huyết động không xâm lấn (USCOM) tại thời điểm trước khi thực hiện nghiệm pháp nâng chân thụ động (T1), theo dõi liên tục trong vòng 2 phút cho tới khi kết thúc nghiệm pháp và đo các thông số huyết động (T2). Theo kết quả nghiên cứu của Teboul và cộng sự thì những ảnh hưởng của nghiệm pháp nâng chân lên huyết động ở bệnh nhân sốc nhiễm khuẩn bao gồm: cung lượng tim, chỉ số tim, chỉ số thể tích nhát bóp, vận tốc dòng máu qua van động mạch chủ.
Truyền dịch lượng nhỏ (Mini fluid challenge): 100ml. Đáp ứng khi thay đổi SV (CO): 6%.
Truyền dịch “tiêu chuẩn” (Standard fluid challenge): 300-500 ml. Đáp ứng khi thay đổi SV (CO): 15%.
3.11. Thăm dò huyết động ở bệnh nhân COVID-19
- Hình 10.8. Thăm dò huyết động ở bệnh nhân COVID-19
4. XỬ TRÍ HUYẾT ĐỘNG Ở BỆNH NHÂN COVID-19
4.1. Mục tiêu hồi sức huyết động theo Surviving Sepsis Campaign trên bệnh nhân COVID-19
- Bù dịch tinh thể muối.
- Không bù dịch như dextrans,
- Vận mạch ưu tiên là
- Không dùng dopamin nếu có
- Trên bệnh nhân có sốc kết hợp với rối loạn chức năng tim dai dẳng mặc dù đã đảm bảo đủ dịch và noradrenalin có thể phối hợp thêm với dobutamin.
- Với những bệnh nhân sốc kháng trị chúng tôi gợi ý có thể phối hợp với liệu pháp corticoid liều thấp.
Một số lưu ý trong quá trình hồi sức huyết động cho bệnh nhân:
- Hồi sức dịch sớm sẽ giúp ổn định tưới máu trong sốc.
- Cần bình thường hóa lactate máu.
- Các biện pháp theo dõi đáp ứng dịch bằng CVP vẫn có thể áp dụng trong điều kiện chúng ta không có các thăm dò sâu hơn như PPV, SVV…
- Tuân thủ gói 1 giờ:
- Đo lactat xét nghiệm lại lactat nếu lactat cao > 2 mmol/l.
- Cấy máu trước khi dùng kháng
- Kháng sinh phổ rộng.
- Bù nhanh dịch tinh thể 30 ml/kg cân nặng nếu tụt huyết áp hoặc lactat > 4 mmol/l.
- Cho thuốc qua mạch trong và sau bù dịch để duy trì huyết áp trung bình (MAP) > 65
4.2. Bồi phụ thể tích dịch
Mục tiêu:
- Duy trì huyết áp trung bình > 65 mmHg, nước tiểu > 1 ml/kg/h.
- Lựa chọn dịch: ưu tiên dung dịch tinh thể natri clorua 0,9% hoặc ringer lactat, 30 ml/kg truyền Nếu đã truyền nhiều dung dịch tinh thể nên truyền thêm dung dịch keo gelatin. Duy trì albumin máu > 30 g/l.
- Đánh giá lại sau mỗi lần bù dịch, tránh quá tải dịch gây phù phổi.
- Sử dụng các biện pháp thăm dò huyết động sẵn có:
- Nhịp tim, huyết áp (tốt nhất là HA động mạch xâm lấn).
- Sự biến thiên của thể tích nhát bóp (SVV), áp lực sóng mạch (PPV) hoặc thể tích nhát bóp (SV) sau mỗi lần truyền dịch hoặc nâng chân thụ động…
- Theo dõi lactat máu 2 giờ/lần, hoặc nghiệm pháp làm đầy mao mạch (capillary refill testing CRT) sau mỗi 30 phút (bình thường < 2 giây).
- Theo dõi áp lực tĩnh mạch trung tâm (CVP): duy trì ở người bệnh tự thở (8-12 cmH2O), người bệnh đang thở máy (CVP 12-15 cmH2O).
- Siêu âm đánh giá chức năng tim, đường kính tĩnh mạch chủ dưới.
4.3. Thuốc vận mạch
- Noradrenalin: liều khởi đầu 0,1 μg/kg/phút, tăng dần liều 0,1 μg/kg/ phút mỗi 5 – 10 phút đến khi đạt được huyết áp mục tiêu.
- Nếu không có noradrenalin, có thể thay thế bằng vasopressin (chú ý nguy cơ hoại tử ngọn chi) hoặc adrenalin (chú ý nguy cơ mạch nhanh).
- Không sử dụng dopamin do tăng nguy cơ rối loạn nhịp.
- Nếu dùng noradrenalin liều cao mà huyết áp không đạt mục tiêu, dùng thêm vasopressin hoặc
- Dobutamin: khi đã bù đủ dịch với noradrenalin liều cao nhưng vẫn tụt huyết áp. Và có bằng chứng suy giảm chức năng co bóp cơ Liều khởi đầu 5 μg/kg/phút, tăng dần 5 μg/kg/phút/lần, sau mỗi 5-10 phút, liều tối đa 20 μg/kg/phút.
- Trong trường hợp sốc trơ: dùng thêm liệu pháp corticoid với liều thấp (hydrocortison 200-300 mg/ngày).
4.4. Điều trị rối loạn nhịp tim
- Điều chỉnh rối loạn điện giải K+, Mg2+.
- Sử dụng thuốc điều trị rối loạn nhịp.
- Sốc điện khi cơn nhịp nhanh gây nên tụt huyết áp.
- Nhịp chậm kéo dài, không đáp ứng với thuốc: đặt máy tạo nhịp.
TÀI LIỆU THAM KHẢO
- Surviving Sepsis Campaign: guidelines on the management of critically ill adults with Coronavirus Disease 2019 (COVID-19).
- The Washington Manual of Critical care (2017).
- Bednarczyk JM, Fridfinnson JA, Kumar A, Blanchard L, Rabbani R, Bell D, Funk D, Tur- geon AF, Abou-Setta AM, Zarychanski R. Incorporating dynamic assessment of fluid responsiveness into goal-directed therapy: a systematic review and meta-analysis. Crit Care Med. 2017;45:1538–1545.
- Bentzer P, Griesdale DE, Boyd J, MacLean K, Sirounis D, Ayas Will this hemodynamical- ly unstable patient respond to a bolus of intravenous fluids? JAMA. 2016;316:12981309.