Bệnh hô hấp
Biến đổi áp suất xung động mạch với thông gió cơ học trên bệnh nhân thở máy
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
nhathuocngocanh.com – Để tải file PDF của bài viết Biến đổi áp suất xung động mạch với thông gió cơ học trên bệnh nhân thở máy, xin vui lòng click vào link ở đây.
Dịch bài: BS. Đặng Thanh Tuấn – BV Nhi Đồng 1
Tóm tắt
Truyền dịch chỉ làm tăng đáng kể cung lượng tim ở một nửa số bệnh nhân ICU. Điều này đã dẫn đến khái niệm đánh giá khả năng đáp ứng của dịch trước khi truyền dịch. Sự thay đổi áp lực mạch (PPV), định lượng sự thay đổi của áp lực mạch động mạch trong quá trình thở máy, là một trong những biến số động lực học có thể dự đoán khả năng đáp ứng dịch. Giả thuyết cơ bản là những thay đổi lớn về hô hấp trong thể tích nhát bóp thất trái, và do đó áp lực mạch, xảy ra trong các trường hợp đáp ứng tiền tải tâm thất. Một số nghiên cứu cho thấy PPV dự đoán chính xác khả năng đáp ứng dịch khi bệnh nhân thở máy kiểm soát. Tuy nhiên, trong nhiều điều kiện gặp phải trong ICU, việc giải thích PPV là không đáng tin cậy (thở tự phát, loạn nhịp tim) hoặc nghi ngờ (Vt thấp). Để khắc phục một số hạn chế này, các nhà nghiên cứu đã đề xuất sử dụng các thử nghiệm đơn giản như thử thách Vt để đánh giá đáp ứng động của PPV. Khả năng áp dụng của PPV cao hơn trong môi trường phòng mổ, nơi các chiến lược dịch truyền được thực hiện trên cơ sở PPV cải thiện kết quả sau phẫu thuật. Ở những bệnh nhân bị bệnh nặng về nội khoa, mặc dù không có thử nghiệm đối chứng ngẫu nhiên nào so sánh việc quản lý dịch dựa trên PPV với chăm sóc tiêu chuẩn, các hướng dẫn của Chiến dịch Nhiễm trùng huyết sống sót khuyến nghị sử dụng các chỉ số đáp ứng dịch, bao gồm cả PPV, bất cứ khi nào có thể áp dụng. Kết luận, PPV hữu ích để quản lý liệu pháp truyền dịch trong các điều kiện cụ thể, nơi đáng tin cậy. Động học của PPV trong các xét nghiệm chẩn đoán hoặc điều trị cũng hữu ích cho việc quản lý dịch.
Cho đến giữa những năm 1990, việc hồi sức huyết động của bệnh nhân suy tuần hoàn thường được hướng dẫn bởi các dữ liệu do catheter động mạch phổi cung cấp. Kể từ đó, việc sử dụng ống thông động mạch phổi đã giảm sút nghiêm trọng (1). Các yếu tố đã góp phần vào sự suy giảm này là rất nhiều, bao gồm cả việc công bố các thử nghiệm ngẫu nhiên có đối chứng cho thấy không có lợi ích (2) hoặc thậm chí tác dụng có hại (3) của các chiến lược nhằm tối đa hóa việc cung cấp oxy ở bệnh nhân ICU. Hơn nữa, một nghiên cứu lâm sàng đa trung tâm không phân loại cho thấy tỷ lệ tử vong liên quan đến đặt ống thông động mạch phổi tăng lên (4), mặc dù các thử nghiệm đối chứng ngẫu nhiên tiếp theo không xác nhận những phát hiện này (5, 6). Những phát hiện này cuối cùng đã góp phần vào việc 1) chuyển từ khái niệm cung cấp oxy tối đa sang khái niệm cá nhân hóa chiến lược điều trị, và 2) phát triển các phương pháp thay thế mới và ít xâm lấn hơn cho đặt ống thông động mạch phổi (7).
Hai mươi năm trước: Sự xuất hiện của khái niệm về khả năng đáp ứng dịch và đánh giá tại giường của nó
Khái niệm dự đoán khả năng đáp ứng dịch
(prediction of fluid responsiveness) đã xuất hiện trong bối cảnh cá nhân hóa liệu pháp huyết động và chiếm một vị trí chính trong việc hướng dẫn hồi sức cho bệnh nhân ICU ngày nay (8, 9). Khả năng đáp ứng dịch thường được định nghĩa là khả năng của tim tăng thể tích nhát bóp hoặc cung lượng tim để đáp ứng với một lượng dịch (10). Về mặt sinh lý, khả năng đáp ứng dịch ngụ ý rằng cả hai tâm thất đều đáp ứng tiền tải (tức là chúng hoạt động trên phần dốc của đường cong được vẽ từ mối quan hệ thể tích nhát bóp tương ứng so với tiền tải; cơ chế Frank-Starling) (Hình 1). Một đánh giá có hệ thống về tài liệu đã báo cáo rằng khả năng đáp ứng dịch chỉ có ở 50% bệnh nhân ICU mà bác sĩ điều trị đưa ra quyết định truyền dịch cho họ (10). Tuy nhiên, không thể loại trừ khả năng tỷ lệ phần trăm sẽ cao hơn nếu chỉ xem xét những bệnh nhân bị sốc. Tuy nhiên, do quá tải dịch có thể gây hại cho bệnh nhân ICU (11), đặc biệt là đối với những người không đáp ứng dịch (12), điều quan trọng là phải phát hiện khả năng đáp ứng dịch trước khi truyền bất kỳ dịch truyền nào.
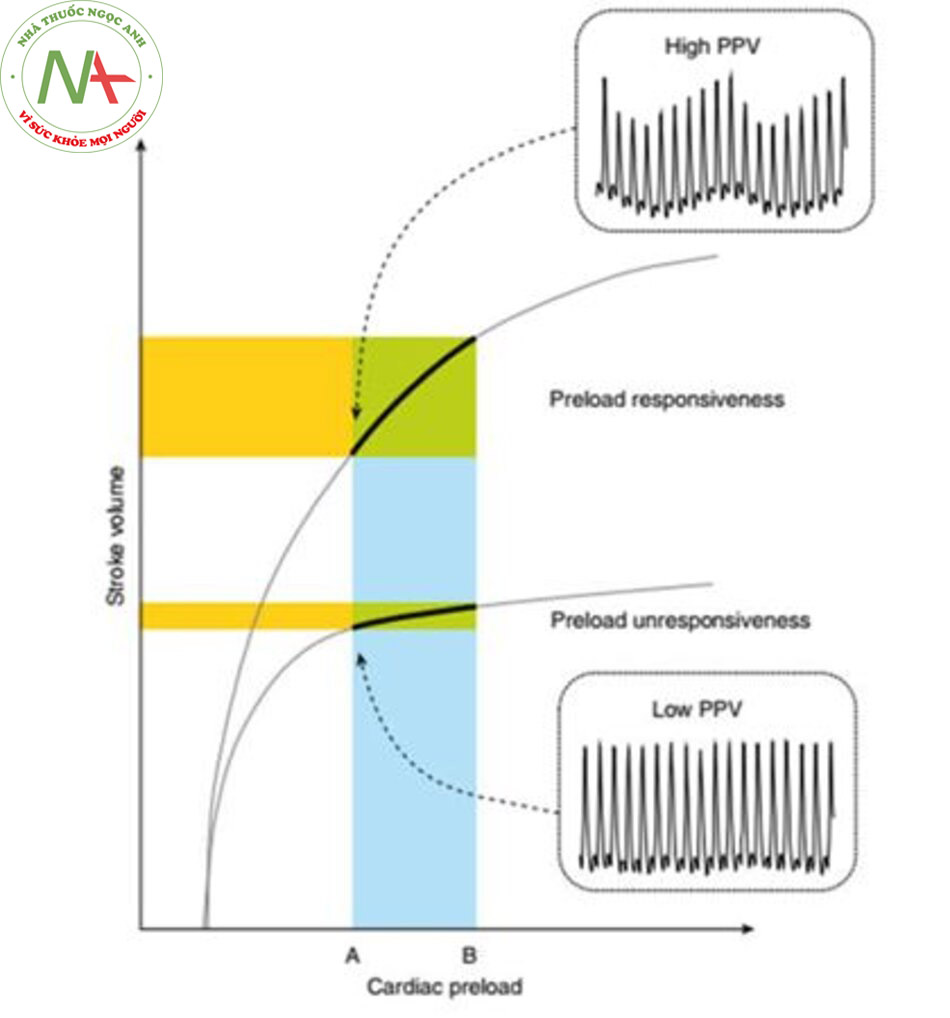
Các phép đo tiền tải của tim, chẳng hạn như áp lực tĩnh mạch trung tâm (central venous pressure − CVP), không hữu ích để dự đoán khả năng đáp ứng dịch (13). Một giá trị nhất định của tiền tải tim có thể liên quan đến khả năng đáp ứng dịch hoặc không đáp ứng dịch, tùy thuộc vào hình dạng của đường cong Frank-Starling (Hình 1). Có sự khác biệt lớn về hình dạng của đường cong Frank-Starling giữa các cá nhân, chủ yếu liên quan đến sự khác biệt về sức co bóp của tim.
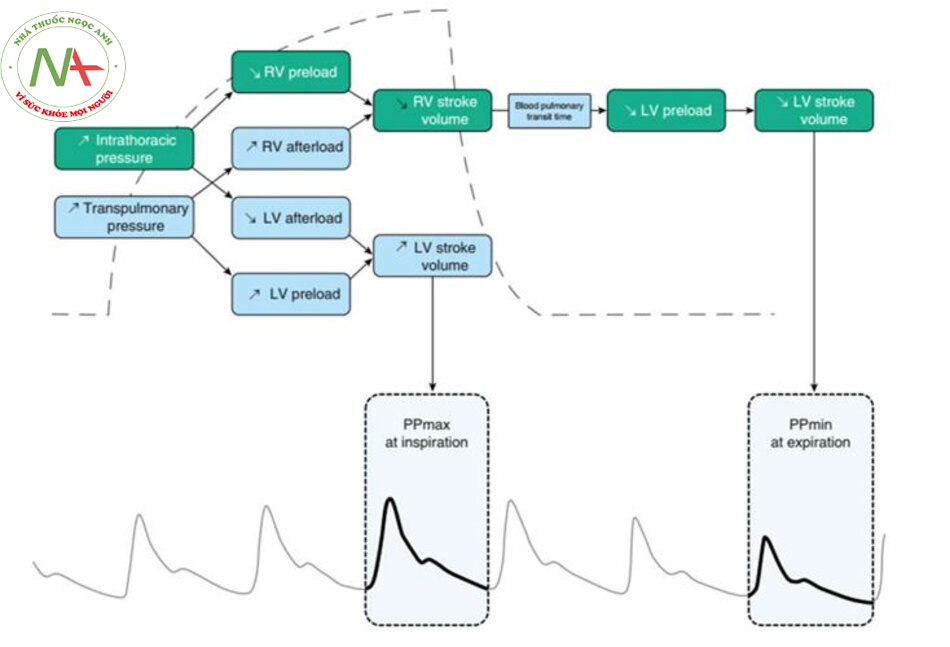
Một phương pháp có giá trị hơn để dự đoán khả năng đáp ứng của dịch là ước tính độ dốc của đường cong Frank-Starling bằng cách đo những thay đổi ngắn hạn về thể tích nhát bóp (hoặc thông số thay thế của nó) để đáp ứng với sự thay đổi ngắn của tiền tải tim. Phương pháp cổ điển (truyền một lượng nhỏ dịch trong thời gian ngắn) liên quan đến việc truyền dịch, có thể gây hại cho những người không đáp ứng dịch, đặc biệt khi thử nghiệm được lặp lại thường xuyên. Do đó, các thử nghiệm động, thách thức mối quan hệ Frank-Starling mà không cần truyền dịch, đã trở nên rất phổ biến. Vào cuối những năm 1990, việc định lượng sự thay đổi theo hô hấp của thể tích nhát bóp nổi lên như một ứng dụng thực tế của các nguyên tắc lý thuyết tương tác tim – phổi được các chuyên gia về sinh lý tim mạch và hô hấp mô tả vào những năm 1980 (1416). Cơ sở sinh lý là thở máy gây ra những thay đổi theo chu kỳ trong điều kiện tải của cả hai tâm thất (14–17) (Hình 2). Việc hít vào làm giảm tiền tải thất phải (right ventricular − RV) do hậu quả của việc giảm trở lại tĩnh mạch do tăng áp lực trong lồng ngực thì hít vào. Việc bơm phồng phổi nói chung làm tăng hậu tải RV do hậu quả của việc tăng áp lực xuyên phổi (18), đặc biệt là khi điều kiện vùng 2 của West – khi áp lực phế nang trở nên cao hơn áp lực tĩnh mạch phổi – được kéo dài (19). Kết quả là, thể tích nhát bóp RV là tối thiểu khi kết thúc quá trình bơm phồng (15, 18). Thông thường người ta cho rằng sự giảm trở lại của tĩnh mạch ở thì hít vào là cơ chế chủ yếu, đặc biệt nếu tâm thất phải hoạt động trên phần dốc của đường cong Frank-Starling (khả năng đáp ứng tiền tải RV). Sự giảm thể tích nhát bóp RV do hít vào dẫn đến giảm lượng đổ đầy thất trái (left ventricular − LV) sau một pha trễ từ hai đến bốn nhịp tim do thời gian vận chuyển máu qua phổi. Điều này thường xảy ra trong thời gian thở ra (17). Trong các trường hợp đáp ứng tiền tải LV, việc giảm tiền tải LV cuối cùng dẫn đến giảm thể tích nhát bóp LV, do đó nhỏ nhất trong thời gian thở ra. Từ những nguyên tắc sinh lý này, người ta đã công nhận rằng trong quá trình thở máy, những thay đổi lớn về thể tích nhát bóp LV sẽ xảy ra trong các trường hợp đáp ứng tiền tải của hai thất, trong khi không có thay đổi về thể tích nhát bóp LV nếu ít nhất một tâm thất không đáp ứng được (17). Nhiều nghiên cứu đã chứng minh một cách nhất quán rằng mức độ thay đổi theo hô hấp của thể tích nhát bóp dự đoán khả năng đáp ứng dịch với độ chính xác cao ở những bệnh nhân thở máy (12, 20, 21).
Sự thay đổi áp lực mạch: Một chỉ số có giá trị để dự đoán khả năng đáp ứng dịch ở những bệnh nhân thở máy
Trong số tất cả các chỉ số về khả năng đáp ứng dịch, sự thay đổi áp lực mạch (pulse pressure variation − PPV) là một trong những chỉ số được nghiên cứu nhiều nhất và được sử dụng nhiều nhất trong thực hành lâm sàng.
Áp lực mạch động mạch chủ (huyết áp tâm thu trừ huyết áp tâm trương) tỷ lệ thuận với thể tích nhát bóp LV và tỷ lệ nghịch với độ giãn nở của động mạch chủ (22).
Chúng tôi công nhận rằng PPV phản ánh những thay đổi theo hô hấp trong thể tích nhát bóp và do đó, sẽ giúp đánh giá khả năng đáp ứng dịch (23, 24). Đây là giả định rằng độ giãn nở của động mạch không thay đổi trong chu kỳ hô hấp, một giả thuyết đã được xác nhận bằng thực nghiệm (25). Một trong những lợi thế của việc sử dụng PPV thay vì sự thay đổi huyết áp tâm thu, đã được đánh giá trước đây (26, 27), là áp lực mạch, vốn là sự khác biệt, ít bị ảnh hưởng trực tiếp bởi những thay đổi theo chu kỳ của áp lực trong lồng ngực hơn là huyết áp tâm thu. Theo đó, chúng tôi đã chỉ ra rằng PPV là một yếu tố dự đoán tốt hơn về khả năng đáp ứng dịch hơn là sự thay đổi huyết áp tâm thu (24). Điều quan trọng, trong nghiên cứu này được thực hiện ở những bệnh nhân bị sốc nhiễm trùng, PPV là một yếu tố dự báo khả năng đáp ứng dịch tốt hơn nhiều so với áp lực làm đầy tim. Chúng tôi xác định khả năng đáp ứng dịch bằng cách tăng cung lượng tim do pha loãng nhiệt lên hơn 15% để đáp ứng với một liều dịch (dung dịch keo 500 ml được truyền trong 30 phút) (24). Các nghiên cứu sâu hơn trong các cơ sở lâm sàng khác nhau đã xác nhận công dụng của PPV như một yếu tố dự đoán đáng tin cậy về khả năng đáp ứng dịch ở những bệnh nhân thở máy với Vt ít nhất 8 ml/kg (19, 20), miễn là họ không có hoạt động thở tự phát và/hoặc rối loạn nhịp tim (28). Trong một phân tích tổng hợp bao gồm 22 nghiên cứu và 807 bệnh nhân, PPV dự đoán khả năng đáp ứng dịch với diện tích dưới đường cong ROC (receiving operating characteristic) là 0,94 và ngưỡng 12% (20). Đáng chú ý là trong các nghiên cứu bao gồm, khả năng đáp ứng dịch được xác định bằng cách sử dụng một trong các kỹ thuật sau: pha loãng nhiệt, pha loãng nhiệt xuyên phổi (transpulmonary thermodilution), phân tích đường viền xung (pulse contour analysis), hoặc Doppler thực quản (20).
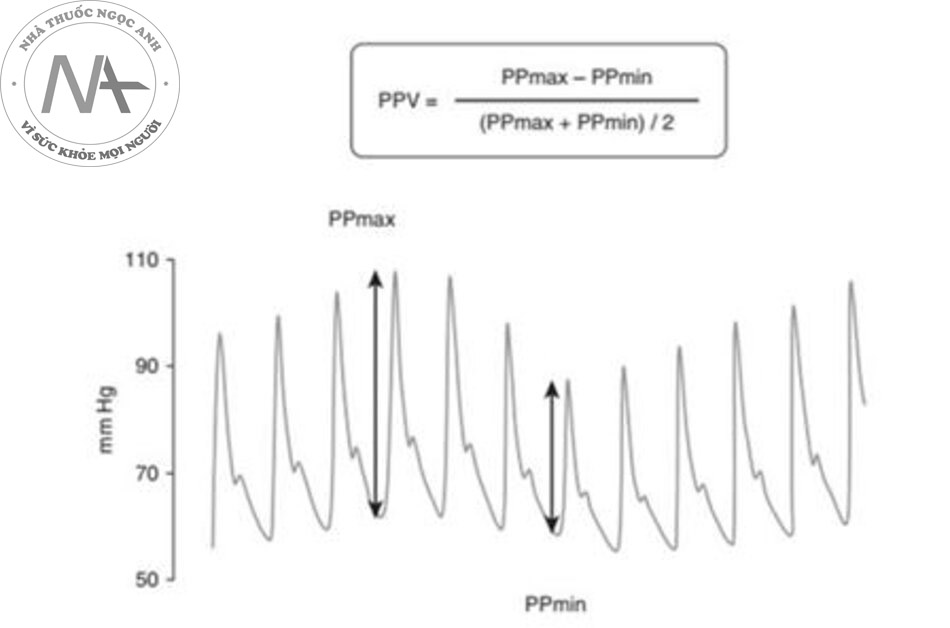
Ban đầu, PPV được xác định theo cách thủ công bằng tỷ số của sự khác biệt giữa giá trị cực đại và cực tiểu của áp lực mạch so với giá trị trung bình của hai giá trị này và được biểu thị bằng phần trăm (Hình 3) (23). Ngày nay, hầu hết các máy theo dõi huyết động đều cho phép tính toán tự động PPV với việc hiển thị liên tục giá trị của nó trong thời gian thực (29). Sử dụng các thuật toán độc quyền, một số máy monitor ước tính thể tích nhát bóp trên cơ sở phân tích dạng sóng áp lực động mạch (30). Họ cũng tính toán và hiển thị sự thay đổi thể tích nhát bóp (stroke volume variation − SVV), được giả định để phản ánh sự thay đổi theo hô hấp của thể tích nhát bóp ở bệnh nhân thở máy (31). Trong một phân tích tổng hợp, SVV đã dự đoán khả năng đáp ứng dịch với độ chính xác cao hơn so với các dấu hiệu của tiền tải tim ở bệnh nhân thở máy (19). Tuy nhiên, SVV kém chính xác hơn đáng kể so với PPV (đường cong AUROC: 0,84 so với 0,94, tương ứng) (19). Kết quả không có gì đáng ngạc nhiên, bởi vì việc tính toán PPV dễ có ít lỗi hơn so với việc tính toán phức tạp hơn của SVV. Một ưu điểm khác của PPV so với SVV là nó chỉ yêu cầu catheter động mạch đơn giản để thu thập dữ liệu.
Các thiết bị không xâm lấn đo lường sự thay đổi theo hô hấp trong các tín hiệu huyết động khác nhau cũng có thể được sử dụng để dự đoán khả năng đáp ứng của dịch trong quá trình thở máy. PPV được đo bằng thiết bị đo huyết áp ngón tay (phương pháp kẹp thể tích) (volume clamp method) cũng đáng tin cậy như PPV thu được xâm lấn để dự đoán khả năng đáp ứng dịch trong phòng mổ (operating room − OR) (32) cũng như trong bối cảnh ICU (33). Những thay đổi theo hô hấp trong biên độ của tín hiệu plethysmographic (của máy pulse oximeter) dự đoán khả năng đáp ứng dịch với độ chính xác chấp nhận được (34, 35), ngoại trừ ở những bệnh nhân dùng norepinephrine (36, 37). Các thay đổi về hô hấp trong các biến số siêu âm, chẳng hạn như tích phân thời gian vận tốc của đường ra LV (siêu âm tim) (38), lưu lượng máu động mạch chủ (Doppler thực quản) (39), đường kính của tĩnh mạch chủ dưới (40) hoặc tĩnh mạch chủ trên (41), và đường kính của tĩnh mạch cảnh trong (42), đã được chứng minh là những yếu tố dự báo khả năng đáp ứng dịch có thể chấp nhận được, mặc dù chúng ít được nghiên cứu hơn và ít được xác nhận hơn PPV. Nhìn chung, điều này khẳng định cơ sở lý thuyết rằng tương tác tim – phổi trong quá trình thở máy có thể được sử dụng một cách thận trọng để dự đoán khả năng đáp ứng dịch. Các chỉ số về khả năng đáp ứng dịch không xâm lấn, như đã mô tả ở trên, có thể hữu ích khi không thực hiện đặt catheter động mạch. Ngoài ra, nên siêu âm tim càng sớm càng tốt, vì đây là phương thức ưu tiên để đánh giá ban đầu loại sốc (8).
PPV trong các tình huống lâm sàng cụ thể: Hạn chế là gì? Làm thế nào nó có thể vượt qua?
Một số điều kiện, được liệt kê trong Bảng 1, hạn chế việc giải thích PPV (27). Do đó, điều quan trọng là phải thảo luận về lợi ích của PPV trong một số bối cảnh cụ thể.
| Bảng 1. Các điều kiện mà sự thay đổi áp lực mạch kém tin cậy hơn | |
| Thở tự nhiên | + giả |
| Rối loạn nhịp tim | + giả |
| Vt thấp | − giả |
| Độ giãn nở của phổi thấp | − giả |
| Tăng áp lực trong ổ bụng | + giả |
| Tần số hô hấp rất cao (HR/RR <3,6) | − giả |
| Rối loạn chức năng thất phải | + giả |
HR = heart rate; RR = respiratory rate.
PPV và Hội chứng suy hô hấp cấp tính
Ít nhất hai yếu tố hạn chế việc sử dụng PPV trong hội chứng suy hô hấp cấp (ARDS): thông khí Vt thấp và độ giãn nở của phổi thấp (43).
Thông khí Vt thấp được khuyến cáo ở bệnh nhân ARDS (9). Trong những điều kiện này, sự thay đổi theo hô hấp của áp lực trong lồng ngực có thể không đủ để tạo ra những thay đổi đáng kể của tiền tải. Theo đó, báo cáo rằng trong trường hợp Vt lớn hơn hoặc bằng 8 ml/kg, PPV dự đoán chính xác khả năng đáp ứng dịch (đường cong AUROC, 0,89, với giá trị ngưỡng 12%), trong khi dự đoán yếu hơn (đường cong AUROC, 0,70, với giá trị ngưỡng 8%) khi Vt nhỏ hơn 8 ml/kg (44). Tuy nhiên, trong quá trình thông khí Vt thấp, ba vấn đề quan trọng cần được làm nổi bật. Đầu tiên, PPV cao (ví dụ: > 12%) vẫn cho thấy khả năng đáp ứng dịch. Thứ hai, PPV thấp không thể loại trừ khả năng đáp ứng dịch. Thứ ba, để khắc phục khó khăn trong việc giải thích PPV thấp, người ta đã đề xuất đo đáp ứng của PPV với sự gia tăng Vt (45) thoáng qua (<1 phút). Myatra và cộng sự xác nhận rằng PPV dự đoán kém khả năng đáp ứng dịch ở mức 6 ml/kg Vt (đường cong AUROC, 0,69) (46). Sau khi Vt được tăng lên 8 ml/kg, PPV dự đoán đáng tin cậy hơn về đáp ứng huyết động với truyền dịch, được ghi nhận là 6 ml/kg (đường cong AUROC, 0,91) (46). Điều thú vị là sự gia tăng giá trị tuyệt đối của PPV lớn hơn hoặc bằng 3,5% trong thử thách Vt đã dự đoán khả năng đáp ứng dịch với độ chính xác tuyệt vời (đường cong AUROC, 0,99) (46). Một cách khác để khắc phục hạn chế của việc sử dụng PPV trong trường hợp Vt thấp là chia PPV theo sự thay đổi theo hô hấp của áp lực thực quản (đường cong AUROC, 0,94 so với 0,78 không điều chỉnh) (47). Nhược điểm của việc sử dụng chỉ số này là cần phải có đầu dò thực quản.
Mức độ giãn nở của phổi và hệ thống hô hấp thấp (Crs = Vt/áp lực đẩy), là đặc điểm của ARDS, cũng có thể dẫn đến giải thích sai về PPV bằng cách giảm sự truyền áp lực đường thở đến các cấu trúc trong lồng ngực (43). Mặc dù độ giãn nở của thành ngực nói chung là giảm, nhưng hậu quả là làm giảm sự truyền áp lực đường thở đó, như được minh họa bởi mối tương quan giữa Crs và sự truyền áp lực đường thở được tìm thấy trong một nghiên cứu trước đây (48). Người ta chứng minh rằng khi Crs lớn hơn 30 ml/cm H2O, PPV dự đoán chính xác khả năng đáp ứng của dịch (đường cong AUROC, 0,98), trong khi Crs nhỏ hơn hoặc bằng 30 ml/cm H2O, dự đoán kém hơn (đường cong AUROC, 0,69) về cơ bản là do tỷ lệ âm tính giả cao (49). Điều thú vị là trong số những người đáp ứng dịch, có một nhóm bệnh nhân được thở máy với Vt nhỏ hơn 8 mL/kg, Crs lớn hơn 30 ml/cm H2O và PPV cao, và một nhóm nhỏ khác có Vt lớn hơn 8 ml/kg, Crs nhỏ hơn hoặc bằng 30 ml/cm H2O và PPV thấp (trung bình 5%), cho thấy Crs giảm có thể đóng vai trò quan trọng hơn Vt thấp trong giá trị dự đoán kém của PPV (49).
Các yếu tố khác hạn chế việc giải thích PPV trong ARDS. Hoạt động thở liên tục trong khi thở máy là phổ biến, vì khuyến cáo hiện tại là giảm thiểu việc sử dụng thuốc an thần và cho phép bệnh nhân sử dụng một phần cơ hô hấp của mình (9), mặc dù vấn đề này vẫn còn là vấn đề tranh luận (50). Trong những trường hợp như vậy, PPV không thể dự đoán khả năng đáp ứng dịch (51), bởi vì những thay đổi theo hô hấp trong áp lực lồng ngực là không đều, cả về tỷ lệ hoặc biên độ. Trong trường hợp thông khí có kiểm soát Vt thấp, có thể cần tạo nhịp hô hấp cao. Trong trường hợp như vậy, sự giảm làm đầy LV thứ phát sau sự giảm thể tích nhát bóp RV do thiếu hụt gây ra có thể xảy ra khi bơm phồng chứ không phải khi thở ra, dẫn đến PPV thấp ngay cả trong các trường hợp đáp ứng dịch. Một nghiên cứu lâm sàng cho thấy PPV không thể được giải thích một cách đáng tin cậy khi tỷ số nhịp tim/nhịp hô hấp thấp hơn 3,6 (52). Ngoài ra, tư thế nằm sấp thường được sử dụng ở những bệnh nhân ARDS nặng. Một nghiên cứu lâm sàng đã báo cáo giá trị dự đoán thấp của PPV khi nằm sấp ở bệnh nhân ARDS (53), có thể do thông khí Vt thấp và độ giãn nở của phổi thấp. Cuối cùng, mức áp lực dương cuối kỳ thở ra (PEEP) không được ảnh hưởng đến giá trị tiên đoán của PPV. Thật vậy, PEEP làm tăng áp lực đường thở trung bình nhưng không làm thay đổi sự thay đổi theo chu kỳ của áp lực đường thở trong một nhịp thở cơ học, đây là yếu tố quyết định chính của PPV. Một số công bố cho thấy giá trị tiên đoán tốt đối với PPV trong thời gian thở máy bao gồm bệnh nhân được điều trị PEEP (23, 24, 33, 41, 54). Điều thú vị là PPV cũng có thể được sử dụng để dự đoán tác động huyết động của PEEP (23). Chúng tôi suy đoán rằng PPV cao ở bệnh nhân ARDS có liên quan đến sự hiện diện của phụ thuộc tiền tải hai thất và giảm đáng kể cung lượng tim với PEEP chỉ xảy ra ở những bệnh nhân phụ thuộc tiền tải hai thất. Theo đó, chúng tôi đã chỉ ra rằng PPV trước khi áp dụng PEEP càng cao thì cung lượng tim càng giảm rõ rệt với PEEP (23).
PPV và Rối loạn chức năng RV
Người ta cho rằng rối loạn chức năng RV có thể dẫn đến giá trị dương tính giả của PPV (tức là PPV cao mặc dù không đáp ứng dịch). Điều này xảy ra do tác động chủ yếu của suy giảm cơ học đối với hậu tải RV thông qua việc ép các vi mạch trong phế nang bởi áp lực xuyên phổi. Vì tâm thất phải bị suy và giãn ra nhạy cảm hơn với hậu tải của nó hơn là tiền tải của nó, sự giảm thể tích nhát bóp RV trong quá trình bơm phồng sẽ liên quan nhiều đến sự phụ thuộc hậu tải RV hơn là phụ thuộc vào tiền tải RV. Hai nghiên cứu lâm sàng báo cáo giá trị PPV cao (> 12%) mặc dù không đáp ứng dịch trong bối cảnh rối loạn chức năng RV (55, 56). Tuy nhiên, trong những nghiên cứu này, Vt lớn hơn 8 ml/kg, và trong một nghiên cứu không thể loại trừ sự suy giảm của hiện tượng phụ thuộc hậu tải RV khi thông khí Vt thấp. Ngoài ra, trong các nghiên cứu này, được thực hiện trước khi xuất bản các hướng dẫn quốc tế (57), cách đánh giá chức năng RV có thể được tranh luận.
PPV và Suy tim sung huyết
Rất ít nghiên cứu đã đề cập đến vấn đề đáp ứng dịch ở bệnh nhân suy tim sung huyết, có thể là do truyền dịch hiếm khi được chỉ định ở những bệnh nhân như vậy. Trong một số nghiên cứu, bao gồm cả những bệnh nhân bị rối loạn chức năng thất trái và nhịp xoang, PPV (hoặc SVV) đã được báo cáo để dự đoán khả năng đáp ứng dịch với độ chính xác có thể chấp nhận được (41, 58). Tuy nhiên, sự hiện diện của rối loạn nhịp tim là một chống chỉ định rõ ràng đối với việc sử dụng PPV, vì sự thay đổi của áp lực mạch chủ yếu liên quan đến sự không đều của tâm trương tim, bất kể chu kỳ hô hấp.
PPV và tăng áp lực trong ổ bụng
Dữ liệu thực nghiệm cho thấy PPV vẫn có thể dự đoán khả năng đáp ứng dịch trong trường hợp tăng áp lực trong ổ bụng nhưng giá trị ngưỡng có thể cao hơn so với trường hợp áp lực ổ bụng bình thường (59). Tuy nhiên, các điều kiện thực nghiệm (tăng áp lực trong ổ bụng cấp tính, các giá trị áp lực trong ổ bụng đạt được rất cao, Vt cao và độ giãn nở của lồng ngực thấp) khác xa so với các bệnh nhân ICU. Ở một loạt bệnh nhân thở máy bị suy gan cấp, các tác giả kết luận rằng PPV dự đoán khả năng đáp ứng dịch, trong khi những thay đổi theo hô hấp trong tích phân thời gian vận tốc không dự đoán được (60).
PPV trong dân số chung của ICU
Một nghiên cứu quan sát quốc tế được công bố vào năm 2015 đã điều tra 2.213 bệnh nhân để xác định xem liệu các chỉ số đáp ứng dịch có được sử dụng trước khi thực hiện các thử thách với dịch hay không (61). CVP là biến được sử dụng nhiều nhất (576 trường hợp) so với PPV hoặc SVV (176 trường hợp) và nâng chân thụ động (248 trường hợp) (61). Những thực hành này có khả năng phát triển, vì phiên bản gần đây nhất của hướng dẫn Chiến dịch Nhiễm trùng huyết sống sót đề xuất sử dụng các chỉ số động về khả năng đáp ứng dịch (bao gồm cả PPV khi có thể áp dụng) thay vì CVP khi cần đánh giá lại huyết động sau khi truyền dịch ban đầu (9).
Thông khí Vt thấp thường được sử dụng ở những bệnh nhân nặng không có ARDS, như được minh họa bởi một nghiên cứu thu hút 540 bệnh nhân thở máy, phần lớn trong số họ được thông khí Vt thấp (62). PPV cũng như các chỉ số đáp ứng dịch trong siêu âm tim không dự đoán một cách đáng tin cậy khả năng đáp ứng dịch (62). Tuy nhiên, trong nghiên cứu này, khả năng đáp ứng dịch được xác định bằng cách nâng chân thụ động chứ không phải bằng cách truyền dịch (62). Bởi vì nâng chân thụ động được chứng minh là tương đương về mặt huyết động với truyền dịch 312 ml (tối thiểu, 250 ml; tối đa, 350 ml) (63), có thể có một số lượng đáng kể những người đáp ứng dịch 500 ml thực sự được đánh giá là không đáp ứng bằng cách nâng cao chân thụ động và một số người không đáp ứng bằng dịch được phân loại là người đáp ứng bằng cách nâng chân thụ động (62). Điều này có thể dẫn đến tỷ lệ dương tính giả cao hơn, và ở một mức độ thấp hơn là tỷ lệ âm tính giả cao hơn, các trường hợp PPV (64) so với các nghiên cứu đánh giá khả năng đáp ứng dịch khi sử dụng dịch thực tế.
Các điều kiện mà độ tin cậy của PPV bị hạn chế khá phổ biến trong ICU. Ví dụ, trong một nghiên cứu tiền cứu bao gồm các bệnh nhân ICU thực sự được truyền dịch, tỷ lệ các trường hợp có thể sử dụng PPV không giới hạn là 17% (65). Tỷ lệ này có thể thay đổi theo chức năng của hỗn hợp trường hợp và cài đặt máy thở. Một nghiên cứu khác cho thấy trong các trường hợp sốc, các điều kiện áp dụng PPV có mặt ở 39% bệnh nhân nhiễm trùng huyết và 53% bệnh nhân chấn thương (66). Hiệu suất thử thách Vt trong trường hợp thông khí Vt thấp nên mở rộng các điều kiện sử dụng PPV.
PPV và tác động đến kết quả
Ở những bệnh nhân phẫu thuật, có bằng chứng chắc chắn rằng cả việc truyền dịch không đủ và quá nhiều đều có liên quan đến việc tăng tỷ lệ biến chứng sau phẫu thuật (67). Điều chỉnh việc sử dụng dịch theo nhu cầu cá nhân được khuyến khích (68). Duy trì bệnh nhân gần với phần uốn cong của đường cong Frank-Starling (tức là, duy trì PPV trong phạm vi 10–15%) sẽ bảo vệ khỏi hậu quả của cả giảm thể tích tuần hoàn và quá tải dịch (69). Một phân tích tổng hợp của 14 thử nghiệm ngẫu nhiên có đối chứng đã kết luận rằng việc sử dụng PPV hoặc SVV để hướng dẫn quản lý dịch trong và/hoặc ngay sau phẫu thuật có liên quan đến việc giảm đáng kể tỷ lệ mắc bệnh sau phẫu thuật (70). Tuy nhiên, do kết quả của sự không đồng nhất và không nhất quán giữa các nghiên cứu được đánh giá, nên cần phải xác nhận thêm.
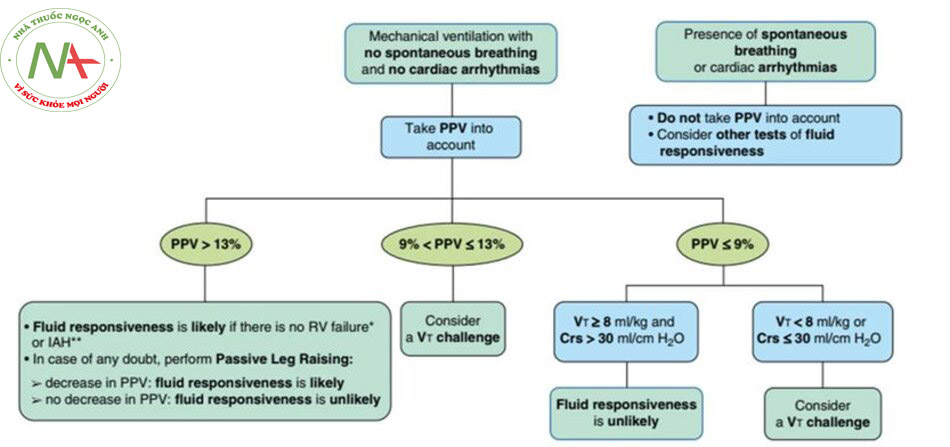
Hình 4. Thực tế sử dụng biến thiên áp lực mạch (PPV). * Phát hiện bằng siêu âm tim; ** được phát hiện bằng cách đo áp lực trong ổ bụng. Crs = độ giãn nở của hệ thống hô hấp; IAH = tăng áp lực trong ổ bụng; RV = thất phải.
Ở bệnh nhân ICU nội khoa, không có thử nghiệm ngẫu nhiên tập trung vào kết quả nào so sánh việc quản lý dịch dựa trên PPV với chăm sóc tiêu chuẩn.
Sử dụng PPV trong thực tế
PPV chỉ nên được xem xét để dự đoán đáp ứng dịch khi bệnh nhân không có hoạt động thở tự phát và có nhịp xoang (Hình 4).
Trong trường hợp giá trị cao (ví dụ:> 13%), PPV phải có giá trị dự đoán tốt ngay cả khi Vt hoặc Crs thấp. Trong trường hợp nghi ngờ về PPV dương tính giả (ví dụ, trong trường hợp rối loạn chức năng RV được chẩn đoán bằng siêu âm tim), có thể thực hiện xét nghiệm nâng chân thụ động; PPV giảm khi nâng chân thụ động cho thấy bệnh nhân thực sự đáp ứng dịch, trong khi PPV không giảm sẽ cho thấy bệnh nhân không đáp ứng dịch và giá trị PPV cao là dương tính giả.
Trong trường hợp giá trị thấp (ví dụ, <9%), PPV có giá trị dự đoán tuyệt vời nếu Vt ít nhất là 8 ml/kg và Crs lớn hơn 30 ml/cmH2O. Ở bệnh nhân ARDS, việc giải thích khó khăn hơn (trường hợp âm tính giả) vì thông khí Vt thấp hoặc Crs thấp. Như đã đề cập ở trên, đây là một kịch bản tốt trong đó thực hiện một thử thách Vt bao gồm Vt tăng tạm thời (từ 6 đến 8 ml/kg) và đo những thay đổi tuyệt đối trong PPV (45, 46).
Một số tác giả đã mô tả “vùng xám” đối với PPV (ví dụ, từ 9% đến 13%), khi không thể đưa ra kết luận về khả năng đáp ứng dịch, ngay cả khi Vt lớn hơn hoặc bằng 8 ml/kg (71). PPV thử thách sau khi Vt tăng thoáng qua từ 8 lên 12 ml/kg đã được đề xuất để khắc phục hạn chế này (72).
Cuối cùng, PPV không nên được giải thích trong các trường hợp rối loạn nhịp tim và hoạt động thở tự phát (Bảng 1 và Hình 4). Tình trạng thứ hai này bao gồm: 1) bệnh nhân được đặt nội khí quản và thở máy với nỗ lực hô hấp liên tục, 2) bệnh nhân thông khí không xâm lấn, và 3) bệnh nhân không thở máy, có hay không có thở ra chủ động (73). Đây là nơi thích hợp cho các thử nghiệm động khác về khả năng đáp ứng dịch, chẳng hạn như nâng chân thụ động hoặc thử nghiệm tắc cuối kỳ thở ra (49).
Dù sử dụng phương pháp nào, sự hiện diện của đáp ứng dịch, là một hiện tượng sinh lý, không nên tự động dẫn đến việc truyền dịch. Trong thực tế, cần phân biệt ba tình huống khác nhau.
Quyết định bắt đầu truyền dịch khẩn cấp ở giai đoạn đầu của sốc không nên dựa trên sự hiện diện của các chỉ số đáp ứng dịch, đặc biệt trong trường hợp sốc nhiễm trùng (9), chảy máu hoạt động hoặc mất dịch rõ ràng.
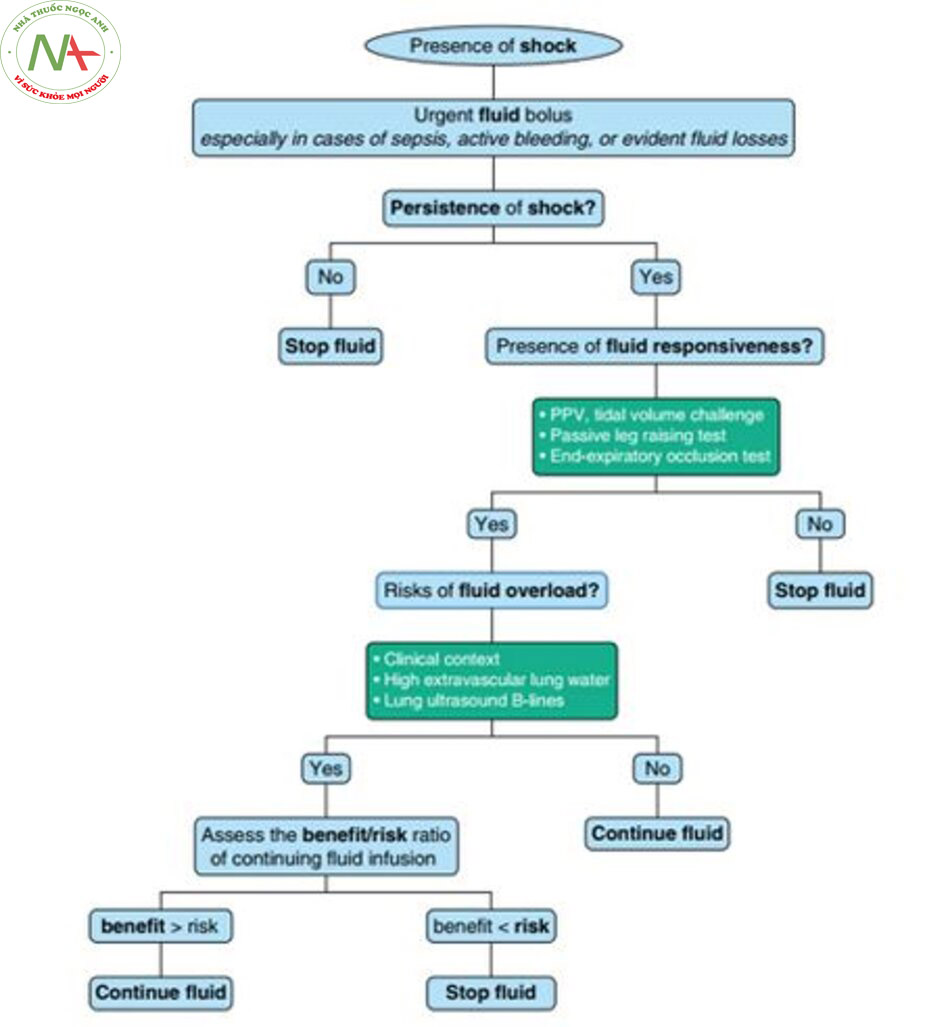
Quyết định tiếp tục truyền dịch sau khi hồi sức dịch ban đầu là một vấn đề khác, ngoại trừ trường hợp chảy máu hoạt động hoặc mất dịch kéo dài. Bởi vì không phải tất cả bệnh nhân đều đáp ứng dịch, các yếu tố dự báo khả năng đáp ứng dịch, mặc dù được yêu cầu, chỉ đại diện cho một yếu tố của quá trình ra quyết định (Hình 5). Quyết định truyền dịch phải dựa trên sự hiện diện của ba yếu tố: 1) dấu hiệu sốc, 2) khả năng đáp ứng dịch, và 3) hạn chế nguy cơ do quá tải dịch. Trong trường hợp phù phổi là một nguy cơ có thể xảy ra, các biến số bổ sung, chẳng hạn như nước phổi ngoài mạch (74) hoặc sự hiện diện của B-line khi kiểm tra siêu âm phổi (75), rất hữu ích trong việc đưa ra quyết định thích hợp. Quyết định ngừng truyền dịch chỉ nên dựa trên sự hiện diện của một trong ba yếu tố sau: 1) biến mất các dấu hiệu sốc, 2) không đáp ứng dịch rõ ràng, hoặc 3) xuất hiện các dấu hiệu phù phổi.
Trong bối cảnh OR, liệu pháp truyền dịch không giới hạn ở những bệnh nhân bị sốc. Trong phẫu thuật có nguy cơ cao, cơ sở lý luận của việc truyền dịch là để tối ưu hóa huyết động học để ngăn ngừa các biến chứng sau phẫu thuật. Như đã đề cập ở trên, các chiến lược dịch do PPV (hoặc SVV) hướng dẫn có thể giúp cải thiện kết quả (70).
Gần đây, các nhà nghiên cứu đã đề xuất sử dụng tỷ lệ PPV/SVV – được gọi là độ đàn hồi động mạch động (dynamic arterial elastance) – để dự đoán đáp ứng của huyết áp với việc truyền dịch. Hai nghiên cứu lâm sàng (76, 77) cho rằng tỷ lệ PPV/SVV thấp dự báo sự không đáp ứng của huyết áp với dịch và do đó sẽ khuyến nghị sử dụng thuốc vận mạch. Tuy nhiên, các nghiên cứu khác đã thất bại trong việc lặp lại những kết quả này (78, 79). Một nghiên cứu thử nghiệm (80) cho thấy rằng thuốc vận mạch làm giảm tỷ lệ PPV/SVV, khiến người ta đặt câu hỏi về việc khuyến cáo sử dụng thuốc vận mạch khi tỷ lệ này thấp. Một số tác giả đã báo cáo rằng tuổi là yếu tố quyết định chính của tỷ lệ PPV/SVV vì tỷ lệ này ở người cao tuổi cao hơn ở bệnh nhân trẻ tuổi (81). Do đó, nên thận trọng khi giải thích tỷ lệ PPV/SVV như một chỉ số để bắt đầu điều trị bằng thuốc vận mạch (82).
Kết luận
PPV là một dấu hiệu dễ lấy nhưng không phải lúc nào cũng dễ sử dụng để biết khả năng đáp ứng dịch. Bỏ qua những hạn chế của nó có thể dẫn đến hiểu sai nghiêm trọng. Một cuộc khảo sát cho thấy một tỷ lệ lớn những bác sĩ hồi sức không có kiến thức đầy đủ về các yếu tố gây nhiễu cho việc giải thích PPV (83). Điều này cho thấy cần phải cải thiện giáo dục.
References
PPV được áp dụng cho những bệnh nhân thở máy, không thở tự phát và không loạn nhịp tim. Giá trị của nó là không thể chối cãi trong các trường hợp thông khí với Vt lớn hơn hoặc bằng 8 ml/kg, phổi có độ giãn nở tốt với thay đổi tối thiểu, và không có suy RV và không có tăng áp lực trong ổ bụng. Các điều kiện để sử dụng tối ưu thường được đáp ứng trong OR, nơi các chiến lược quản lý dịch được thực hiện trên cơ sở theo dõi PPV (hoặc SVV) đã được chứng minh là làm giảm tỷ lệ mắc bệnh sau phẫu thuật (70). Hơn nữa, theo dõi động của PPV cũng được quan tâm, bởi vì trong quá trình truyền dịch, sự giảm PPV tương quan nghịch với sự gia tăng cung lượng tim (23, 24, 84). Các công cụ giám sát PPV không xâm lấn nên được sử dụng ngày càng nhiều trong OR (85), với điều kiện là các tiến bộ công nghệ sẽ tối ưu hóa hiệu lực của chúng.
Tuy nhiên, trong ICU, các điều kiện tối ưu để sử dụng PPV ít có khả năng xảy ra hơn. Tuy nhiên, một số hạn chế của việc diễn giải PPV có thể được khắc phục bằng cách thực hiện các thử nghiệm dựa trên động lực của PPV, chẳng hạn như thử thách Vt.
- Wiener RS, Welch HG. Trends in the use of the pulmonary artery catheter in the United States, 1993-2004. JAMA 2007;298:423–429.
- Gattinoni L, Brazzi L, Pelosi P, Latini R, Tognoni G, Pesenti A, et al. A trial of goal-oriented hemodynamic therapy in critically ill patients: SvO2 Collaborative Group. N Engl J Med 1995;333:1025– 1032.
- Hayes MA, Timmins AC, Yau EH, Palazzo M, Hinds CJ, Watson D. Elevation of systemic oxygen delivery in the treatment of critically ill patients. N Engl J Med 1994;330:1717–1722.
- Connors AF Jr, Speroff T, Dawson NV, Thomas C, Harrell FE Jr, Wagner D, et al.; SUPPORT Investigators. The effectiveness of right heart catheterization in the initial care of critically ill patients. JAMA 1996;276:889–897.
- Richard C, Warszawski J, Anguel N, Deye N, Combes A, Barnoud D, et al.; French Pulmonary Artery Catheter Study Group. Early use of the pulmonary artery catheter and outcomes in patients with shock and acute respiratory distress syndrome: a randomized controlled trial. JAMA 2003;290:2713–2720.
- Harvey S, Harrison DA, Singer M, Ashcroft J, Jones CM, Elbourne D, et al.; PAC-Man study collaboration. Assessment of the clinical effectiveness of pulmonary artery catheters in management of patients in intensive care (PAC-Man): a randomised controlled trial. Lancet 2005;366:472–477.
- De Backer D, Bakker J, Cecconi M, Hajjar L, Liu DW, Lobo S, et al. Alternatives to the Swan-Ganz catheter. Intensive Care Med 2018;44:730–741.
- Cecconi M, De Backer D, Antonelli M, Beale R, Bakker J, Hofer C, et al. Consensus on circulatory shock and hemodynamic monitoring: task force of the European Society of Intensive Care Medicine. Intensive Care Med 2014;40:1795–1815.
- Rhodes A, Evans LE, Alhazzani W, Levy MM, Antonelli M, Ferrer R, et al. Surviving Sepsis Campaign: international guidelines for management of sepsis and septic shock: 2016. Intensive Care Med 2017;43:304–377.
- Michard F, Teboul JL. Predicting fluid responsiveness in ICU patients: a critical analysis of the evidence. Chest 2002;121:2000–2008.
- Vincent JL, Sakr Y, Sprung CL, Ranieri VM, Reinhart K, Gerlach H, et al.; Sepsis Occurrence in Acutely Ill Patients Investigators. Sepsis in European intensive care units: results of the SOAP study. Crit Care Med 2006;34:344–353.
- Monnet X, Marik PE, Teboul JL. Prediction of fluid responsiveness: an update. Ann Intensive Care 2016;6:111.
- Marik PE, Cavallazzi R. Does the central venous pressure predict fluid responsiveness? An updated meta-analysis and a plea for some common sense. Crit Care Med 2013;41:1774–1781.
- Jardin F, Farcot JC, Gueret P, Prost JF, Ozier Y, Bourdarias JP. Cyclic changes in arterial pulse during respiratory support. Circulation 1983;68:266–274.
- Robotham JL, Cherry D, Mitzner W, Rabson JL, Lixfeld W, Bromberger-Barnea B. A re-evaluation of the hemodynamic consequences of intermittent positive pressure ventilation. Crit Care Med 1983;11:783–793.
- Pinsky MR. The influence of positive-pressure ventilation on cardiovascular function in the critically ill. Crit Care Clin 1985;1:699–717.
- Michard F, Teboul JL. Using heart-lung interactions to assess fluid responsiveness during mechanical ventilation. Crit Care 2000;4:282–289.
- Vieillard-Baron A, Loubieres Y, Schmitt JM, Page B, Dubourg O, Jardin F. Cyclic changes in right ventricular output impedance during mechanical ventilation. J Appl Physiol (1985) 1999;87:1644–1650.
- Magder S, Guerard B. Heart-lung interactions and pulmonary buffering: lessons from a computational modeling study. Respir Physiol Neurobiol 2012;182:60–70.
- Marik PE, Cavallazzi R, Vasu T, Hirani A. Dynamic changes in arterial waveform derived variables and fluid responsiveness in mechanically ventilated patients: a systematic review of the literature. Crit Care Med 2009;37:2642–2647.
- Yang X, Du B. Does pulse pressure variation predict fluid responsiveness in critically ill patients? A systematic review and meta-analysis. Crit Care 2014;18:650.
- Chemla D, Hébert JL, Coirault C, Zamani K, Suard I, Colin P, et al. Total arterial compliance estimated by stroke volume-to-aortic pulse pressure ratio in humans. Am J Physiol 1998;274:H500– H505.
- Michard F, Chemla D, Richard C, Wysocki M, Pinsky MR, Lecarpentier Y, et al. Clinical use of respiratory changes in arterial pulse pressure to monitor the hemodynamic effects of PEEP. Am J Respir Crit Care Med 1999;159:935–939.
- Michard F, Boussat S, Chemla D, Anguel N, Mercat A, Lecarpentier Y, et al. Relation between respiratory changes in arterial pulse pressure and fluid responsiveness in septic patients with acute circulatory failure. Am J Respir Crit Care Med 2000;162:134–138.
- Mesquida J, Kim HK, Pinsky MR. Effect of tidal volume, intrathoracic pressure, and cardiac contractility on variations in pulse pressure, stroke volume, and intrathoracic blood volume. Intensive Care Med 2011;37:1672–1679.
- Perel A, Pizov R, Cotev S. Systolic blood pressure variation is a sensitive indicator of hypovolemia in ventilated dogs subjected to graded hemorrhage. Anesthesiology 1987;67:498–502.
- Tavernier B, Makhotine O, Lebuffe G, Dupont J, Scherpereel P. Systolic pressure variation as a guide to fluid therapy in patients with sepsis-induced hypotension. Anesthesiology 1998;89:1313–1321.
- Michard F, Chemla D, Teboul JL. Applicability of pulse pressure variation: how many shades of grey? Crit Care 2015;19:144.
- Auler JO Jr, Galas F, Hajjar L, Santos L, Carvalho T, Michard F. Online monitoring of pulse pressure variation to guide fluid therapy after cardiac surgery. Anesth Analg 2008;106:1201–1206.
- Jozwiak M, Monnet X, Teboul JL. Pressure waveform analysis. Anesth Analg 2018;126:1930–1933.
- Berkenstadt H, Margalit N, Hadani M, Friedman Z, Segal E, Villa Y, et al. Stroke volume variation as a predictor of fluid responsiveness in patients undergoing brain surgery. Anesth Analg 2001;92:984–989.
- Biais M, Stecken L, Ottolenghi L, Roullet S, Quinart A, Masson F, et al. The ability of pulse pressure variations obtained with CNAP device to predict fluid responsiveness in the operating room. Anesth Analg 2011;113:523–528.
- Monnet X, Dres M, Ferré A, Le Teuff G, Jozwiak M, Bleibtreu A, et al. Prediction of fluid responsiveness by a continuous non-invasive assessment of arterial pressure in critically ill patients: comparison with four other dynamic indices. Br J Anaesth 2012;109:330–338.
- Cannesson M, Desebbe O, Rosamel P, Delannoy B, Robin J, Bastien O, et al. Pleth variability index to monitor the respiratory variations in the pulse oximeter plethysmographic waveform amplitude and predict fluid responsiveness in the operating theatre. Br J Anaesth 2008;101:200–206.
- Sandroni C, Cavallaro F, Marano C, Falcone C, De Santis P, Antonelli M. Accuracy of plethysmographic indices as predictors of fluid responsiveness in mechanically ventilated adults: a systematic review and meta-analysis. Intensive Care Med 2012;38:1429–1437.
- Biais M, Cottenceau V, Petit L, Masson F, Cochard JF, Sztark F. Impact of norepinephrine on the relationship between pleth variability index and pulse pressure variations in ICU adult patients. Crit Care 2011;15:R168.
- Monnet X, Guérin L, Jozwiak M, Bataille A, Julien F, Richard C, et al. Pleth variability index is a weak predictor of fluid responsiveness in patients receiving norepinephrine. Br J Anaesth 2013;110:207–213.
- Feissel M, Michard F, Mangin I, Ruyer O, Faller JP, Teboul JL. Respiratory changes in aortic blood velocity as an indicator of fluid responsiveness in ventilated patients with septic shock. Chest 2001;119:867–873.
- Monnet X, Rienzo M, Osman D, Anguel N, Richard C, Pinsky MR, et al. Esophageal Doppler monitoring predicts fluid responsiveness in critically ill ventilated patients. Intensive Care Med 2005;31:1195–1201.
- Feissel M, Michard F, Faller JP, Teboul JL. The respiratory variation in inferior vena cava diameter as a guide to fluid therapy. Intensive Care Med 2004;30:1834–1837.
- Vieillard-Baron A, Chergui K, Rabiller A, Peyrouset O, Page B, Beauchet A, et al. Superior vena caval collapsibility as a gauge of volume status in ventilated septic patients. Intensive Care Med 2004;30:1734– 1739.
- Guarracino F, Ferro B, Forfori F, Bertini P, Magliacano L, Pinsky MR. Jugular vein distensibility predicts fluid responsiveness in septic patients. Crit Care 2014;18:647.
- Teboul JL, Monnet X. Pulse pressure variation and ARDS. Minerva Anestesiol 2013;79:398–407.
- De Backer D, Heenen S, Piagnerelli M, Koch M, Vincent JL. Pulse pressure variations to predict fluid responsiveness: influence of tidal volume. Intensive Care Med 2005;31:517–523.
- Myatra SN, Monnet X, Teboul JL. Use of “tidal volume challenge” to improve the reliability of pulse pressure variation. Crit Care 2017;21:60.
- Myatra SN, Prabu NR, Divatia JV, Monnet X, Kulkarni AP, Teboul JL. The changes in pulse pressure variation or stroke volume variation after a “tidal volume challenge” reliably predict fluid responsiveness during low tidal volume ventilation. Crit Care Med 2017;45:415–421.
- Liu Y, Wei LQ, Li GQ, Yu X, Li GF, Li YM. Pulse pressure variation adjusted by respiratory changes in pleural pressure, rather than by tidal volume, reliably predicts fluid responsiveness in patients with acute respiratory distress syndrome. Crit Care Med 2016;44:342–351.
- Teboul JL, Pinsky MR, Mercat A, Anguel N, Bernardin G, Achard JM, et al. Estimating cardiac filling pressure in mechanically ventilated patients with hyperinflation. Crit Care Med 2000;28:3631–3636.
- Monnet X, Bleibtreu A, Ferré A, Dres M, Gharbi R, Richard C, et al. Passive leg-raising and endexpiratory occlusion tests perform better than pulse pressure variation in patients with low respiratory system compliance. Crit Care Med 2012;40:152–157.
- Fan E, Del Sorbo L, Goligher EC, Hodgson CL, Munshi L, Walkey AJ, et al.; American Thoracic Society, European Society of Intensive Care Medicine, and Society of Critical Care Medicine. An Official American Thoracic Society/European Society of Intensive Care Medicine/Society of Critical Care Medicine Clinical Practice Guideline: mechanical ventilation in adult patients with acute respiratory distress syndrome. Am J Respir Crit Care Med 2017;195:1253–1263.
- Monnet X, Rienzo M, Osman D, Anguel N, Richard C, Pinsky MR, et al. Passive leg raising predicts fluid responsiveness in the critically ill. Crit Care Med 2006;34:1402–1407.
- De Backer D, Taccone FS, Holsten R, Ibrahimi F, Vincent JL. Influence of respiratory rate on stroke volume variation in mechanically ventilated patients. Anesthesiology 2009;110:1092–1097.
- Yonis H, Bitker L, Aublanc M, Perinel Ragey S, Riad Z, Lissonde F, et al. Change in cardiac output during Trendelenburg maneuver is a reliable predictor of fluid responsiveness in patients with acute respiratory distress syndrome in the prone position under protective ventilation. Crit Care 2017;21:295.
- Freitas FG, Bafi AT, Nascente AP, Assunção M, Mazza B, Azevedo LC, et al. Predictive value of pulse pressure variation for fluid responsiveness in septic patients using lung-protective ventilation strategies. Br J Anaesth 2013;110:402–408.
- Mahjoub Y, Pila C, Friggeri A, Zogheib E, Lobjoie E, Tinturier F, et al. Assessing fluid responsiveness in critically ill patients: false-positive pulse pressure variation is detected by Doppler echocardiographic evaluation of the right ventricle. Crit Care Med 2009;37:2570–2575.
- Wyler von Ballmoos M, Takala J, Roeck M, Porta F, Tueller D, Ganter CC, et al. Pulse-pressure variation and hemodynamic response in patients with elevated pulmonary artery pressure: a clinical study. Crit Care 2010;14:R111.
- Rudski LG, Lai WW, Afilalo J, Hua L, Handschumacher MD, Chandrasekaran K, et al. Guidelines for the echocardiographic assessment of the right heart in adults: a report from the American Society of Echocardiography endorsed by the European Association of Echocardiography, a registered branch of the European Society of Cardiology, and the Canadian Society of Echocardiography. J Am Soc Echocardiogr 2010;23:685–713, quiz 786–788.
- Reuter DA, Kirchner A, Felbinger TW, Weis FC, Kilger E, Lamm P, et al. Usefulness of left ventricular stroke volume variation to assess fluid responsiveness in patients with reduced cardiac function. Crit Care Med 2003;31:1399–1404.
- Jacques D, Bendjelid K, Duperret S, Colling J, Piriou V, Viale JP. Pulse pressure variation and stroke volume variation during increased intra-abdominal pressure: an experimental study. Crit Care 2011;15:R33.
- Audimoolam VK, McPhail MJ, Willars C, Bernal W, Wendon JA, Cecconi M, et al. Predicting fluid responsiveness in acute liver failure: a prospective study. Anesth Analg 2017;124:480–486.
- Cecconi M, Hofer C, Teboul JL, Pettila V, Wilkman E, Molnar Z, et al.; FENICE Investigators; ESICM Trial Group. Fluid challenges in intensive care: the FENICE study: a global inception cohort study. Intensive Care Med 2015;41:1529–1537.
- Vignon P, Repessé X, Bégot E, Léger J, Jacob C, Bouferrache K, et al. Comparison of echocardiographic indices used to predict fluid responsiveness in ventilated patients. Am J Respir Crit Care Med 2017;195:1022–1032.
- Jabot J, Teboul JL, Richard C, Monnet X. Passive leg raising for predicting fluid responsiveness:
importance of the postural change. Intensive Care Med 2009;35:85–90.
- Vistisen ST, Enevoldsen J, Scheeren TW. Can passive leg raising be considered the gold standard in predicting fluid responsiveness? Am J Respir Crit Care Med 2017;195:1075–1076.
- Preau S, Dewavrin F, Demaeght V, Chiche A, Voisin B, Minacori F, et al. The use of static and dynamic haemodynamic parameters before volume expansion: a prospective observational study in six French intensive care units. Anaesth Crit Care Pain Med 2016;35:93–102.
- Benes J, Zatloukal J, Kletecka J, Simanova A, Haidingerova L, Pradl R. Respiratory induced dynamic variations of stroke volume and its surrogates as predictors of fluid responsiveness: applicability in the early stages of specific critical states. J Clin Monit Comput 2014;28:225–231.
- Michard F, Biais M. Rational fluid management: dissecting facts from fiction. Br J Anaesth 2012;108:369–371.
- Vincent JL, Pelosi P, Pearse R, Payen D, Perel A, Hoeft A, et al. Perioperative cardiovascular monitoring of high-risk patients: a consensus of 12. Crit Care 2015;19:224.
- Michard F, Lopes MR, Auler JO Jr. Pulse pressure variation: beyond the fluid management of patients with shock. Crit Care 2007;11:131.
- Benes J, Giglio M, Brienza N, Michard F. The effects of goal-directed fluid therapy based on dynamic parameters on post-surgical outcome: a meta-analysis of randomized controlled trials. Crit Care 2014;18:584.
- Cannesson M, Le Manach Y, Hofer CK, Goarin JP, Lehot JJ, Vallet B, et al. Assessing the diagnostic accuracy of pulse pressure variations for the prediction of fluid responsiveness: a “gray zone” approach. Anesthesiology 2011;115:231–241.
- Min JJ, Gil NS, Lee JH, Ryu DK, Kim CS, Lee SM. Predictor of fluid responsiveness in the ‘grey zone’: augmented pulse pressure variation through a temporary increase in tidal volume. Br J Anaesth 2017;119:50–56.
- Magder S. Clinical usefulness of respiratory variations in arterial pressure. Am J Respir Crit Care Med 2004;169:151–155.
- Monnet X, Teboul JL. Transpulmonary thermodilution: advantages and limits. Crit Care 2017;21:147.
- Lichtenstein DA, Mezière GA. Relevance of lung ultrasound in the diagnosis of acute respiratory failure: the BLUE protocol. Chest 2008;134:117–125.
- Monge García MI, Gil Cano A, Gracia Romero M. Dynamic arterial elastance to predict arterial pressure response to volume loading in preload-dependent patients. Crit Care 2011;15:R15.
- Cecconi M, Monge García MI, Gracia Romero M, Mellinghoff J, Caliandro F, Grounds RM, et al. The use of pulse pressure variation and stroke volume variation in spontaneously breathing patients to assess dynamic arterial elastance and to predict arterial pressure response to fluid administration. Anesth Analg 2015;120:76–84.
- Vos JJ, Kalmar AF, Struys MM, Wietasch JK, Hendriks HG, Scheeren TW. Comparison of arterial pressure and plethysmographic waveform-based dynamic preload variables in assessing fluid responsiveness and dynamic arterial tone in patients undergoing major hepatic resection. Br J Anaesth 2013;110:940–946.
- Lanchon R, Nouette-Gaulain K, Stecken L, Sesay M, Lefrant JY, Biais M. Dynamic arterial elastance obtained using arterial signal does not predict an increase in arterial pressure after a volume expansion in the operating room. Anaesth Crit Care Pain Med 2017;36:377–382.
- Monge García MI, Guijo González P, Gracia Romero M, Gil Cano A, Rhodes A, Grounds RM, et al. Effects of arterial load variations on dynamic arterial elastance: an experimental study. Br J Anaesth 2017;118:938–946.
- Stens J, Oeben J, Van Dusseldorp AA, Boer C. Non-invasive measurements of pulse pressure variation and stroke volume variation in anesthetized patients using the Nexfin blood pressure monitor. J Clin Monit Comput 2016;30:587–594.
- Jozwiak M, Monnet X, Teboul JL, Monge García MI, Pinsky MR, Cecconi M. The dynamic arterial elastance: a call for a cautious interpretation: discussion on “Predicting vasopressor needs using dynamic parameters”. Intensive Care Med 2017;43:1438–1439.
- Fischer MO, Dechanet F, du Cheyron D, Gérard JL, Hanouz JL, Fellahi JL. Evaluation of the knowledge base of French intensivists and anaesthesiologists as concerns the interpretation of respiratory arterial pulse pressure variation. Anaesth Crit Care Pain Med 2015;34:29–34.
- Le Manach Y, Hofer CK, Lehot JJ, Vallet B, Goarin JP, Tavernier B, et al. Can changes in arterial pressure be used to detect changes in cardiac output during volume expansion in the perioperative period? Anesthesiology 2012;117:1165–1174.
- Michard F, Gan TJ, Kehlet H. Digital innovations and emerging technologies for enhanced recovery programmes. Br J Anaesth 2017;119:31–39.