Thuốc trừ giun sán
Nhà thuốc Ngọc Anh – Chương 10: Thuốc trị giun sán – PGS.TS: Nguyễn Đình Luyện, Tiến sĩ: Nguyễn Văn Hải
Nguồn: Sách Kỹ thuật Hóa Dược, tập 2- Bộ môn Công nghiệp Dược – Đại học Dược Hà Nội
Chủ biên: PGS. TS. NGUYỄN ĐÌNH LUYỆN
ĐẠI CƯƠNG
Giun sán là bệnh phổ biến ở những nước kém phát triển, đặc biệt ở vùng nhiệt đới nóng ẩm. Do vệ sinh ăn uống chưa tốt, nguồn nước uống chưa sạch nên số người mắc bệnh giun sán ở những nước này chiếm một tỷ lệ lớn.
Giun sán vào cơ thể gây đau bụng, rối loạn tiêu hoá, táo bón, thiếu máu, rối loạn thần kinh, dị ứng, viêm tắc ruột v.v… Vì thế, việc tim các thuốc tẩy giun có hiệu quả đã được tiến hành từ rất lâu và liên tục. Cơ chế tác dụng của các thuốc điều trị giun sán chưa thật rõ ràng. Chúng có thể làm hệt cơ, hoặc phá hủy cơ thể kí sinh trùng. Sinh học của giun sán gần giống loại có xương sống, do đó thuốc trừ giun sán có thể gây ngộ độc cho con người và trẻ nhỏ.
Một thuốc trị giun sán tốt phải có:
- Chỉ số trị liệu lớn.
- Rẻ tiền, dễ điều chế và điều chế được từ những nguyên liệu công nghiệp.
- Dễ dùng, ít tác dụng phụ và không phải có chế độ đặc biệt khi sử dụng.
- Có tác dụng với nhiều loại giun sán một lúc.
- Bền vững về mặt hóa học.
CÁC THUỐC TRỊ GIUN SÁN
Piperazin (1)
Biệt dược: antivermin, antepar, vermoxyl…
Thuốc có tác dụng làm liệt cơ giun. Rất ít độc với cơ thể.
Dạng dùng: Viên nén 0,30-0,50g (muối adipat)
Lọ 30-60ml sừo 5ml/50mg (muối citrat)
Liều dùng: 3g/ngày, dùng 3-5 ngày. Không cần uống thuốc tẩy.
Phương pháp tổng hợp:
Tổng hợp piperazin (1) được thực hiện theo 3 phương pháp sau:
a, Đóng vòng ethanoỉamỉn và các dẫn xuất của nó
Phản ứng thực hiện ở 250-290°C, có mặt amoni clorid, amoni phosphat hoặc trong dung môi hữu cơ.
b, Ngưng tụ ethanolamin (2) với dicloroethan
Phản ứng ngưng tụ thực hiện ở 200-300°c, xúc tác ZnCl2 (Patent Balan 1958):
c, Ngưng tụ ethylendiamỉn với monoester của ethỵlenglycol
Ethylendiamin (7) được ngưng tụ với các monoester của ethylenglycol và acid vô cơ (8) ở 300°c trong 24 giờ, xúc tác NH4CI, ZnCI2, FeCI2. cần phải pha loãng khối phản ứng bằng bột talc để tránh thanh hóa.4 Hiệu suất 40-50%.
Levamisol (9)
Biệt dược: Ascaridil, Decaris, Hacaris, Vinacor.
Tên khoa học: (-)-6-phenyl-2,3,5,6-tetrahydroimidazo[2, l-b]thỉazol
Công thức: Là đồng phân tả truyền của tetramisol.
Công dụng: làm liệt cơ giun, dùng tẩy giun đũa và giun móc. Thuốc gây một số tác dụng không mong muốn trên thần kinh trung ương như rối loạn tâm thần, nói ngọng, động tác bất thường, giảm bạch cầu và có thể gây tử vong… Hiện nay không còn dùng để tẩy giun mà dùng làm thuốc tăng cường miễn dịch ở liều thấp.
Phản ứng của cloroacetophenon (17) và 2-iminothiazolidin (18) trong cloroform thu được 19. Acyl hóa nhóm -NH của 19 với anhydrid acetic thu được dẫn chất N-acyl 20. Khử hóa 20 băng NaBKU trong methanol tạo thành 2-N-acetylimino-3-(2-phenyl-2- hydroxy)-ethyl-thiazolidin (21). Sau đó thế nhóm -OH của 21 bằng -Cỉ với tác nhân thionylclorid trong CHCI3 thu được dẫn chất clor 22.
Phản ứng tạo vòng imidazol của 22 trong môi trường nước có mặt K2CO3 cho tetramizol (16). Sản phẩm này được tách riêng các đồng phân quang học nhờ dibenzoyl-tartric thu được levamisol (9).
a. Từ polystyren và ethylen
Phản ứng của Styren -oxyd (10) với ethylenimin (11) thu được alcol (12). Xử lí 12 với kalisulfocyanat, vòng ethylenimin bị mở tạo thành dẫn chất 13. Đóng vòng 13 trong alcol thu được dẫn chất của 2-imino-thiazolidin 14. Nhóm -OH của 14 dược thế bằng CL nhờ tác nhân thionylclorid. Cuối cùng là phản ứng nưng tụ loại HCL tạo vòng imidazole của tetramizol (16), tách các đồng ohaan quang học thu được levamisol (9)
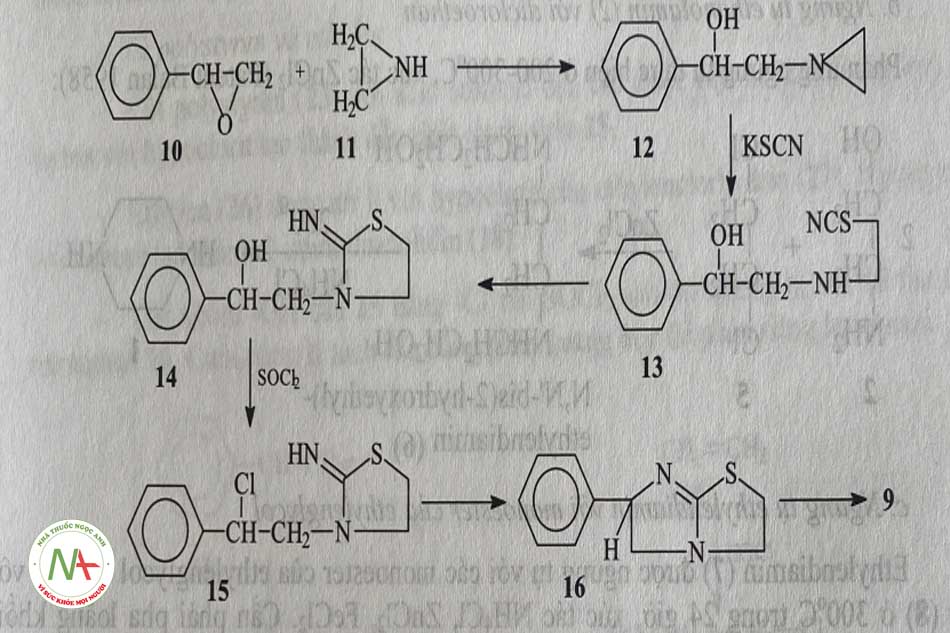
b, Từ cloracetophenon và 2-iminothiazolidin
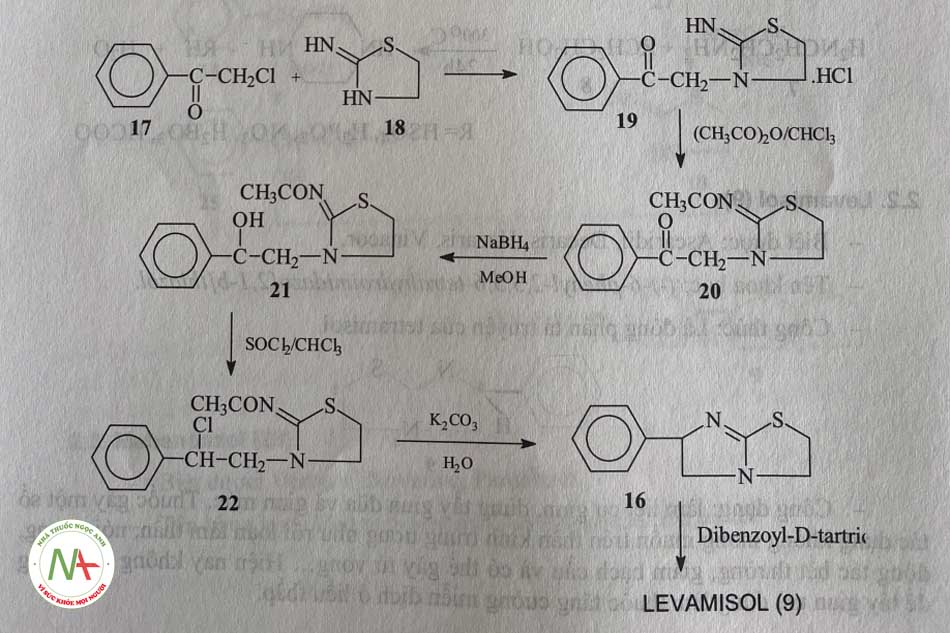
Phản ứng của cloracetophenon (17) và 2-iminothiazollidin (18) trong cloroform thu được 19. Acyl hóa nhóm – NH của 19 với Anhydrid acetic thu được dẫn chất N-acyl 20. Khử hóa 20 bằng NaBH4 trong methanol tạo thành 2-N-acetylimini-3-(1 phenyl-2-hydroxyy)-ethyl-thiazolidin (21). Sau đó thế nhóm -OH của 21 bằng -CL với tác nhân thionylclorid trong CHCL3 thu được dẫn chất clor 22
Phản ứng tạo vòng imidazol của 22 trong môi trường nước có mặt K2CO3 cho tetramizol (16). Sản phẩm này được tách riêng các đồng phân quang học nhờ Dibenzoyl-tartric thu được levamisol.
C. Từ polystyren và ethylen
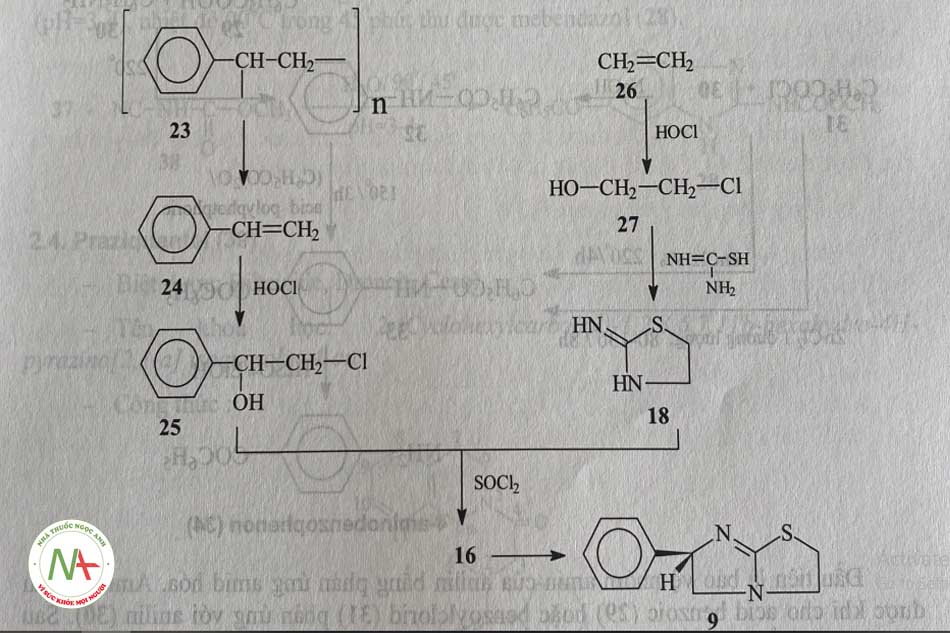
Chất polystyren (23) với acid sulfuric đặc thu được styren (24). Phản ứng của styren với hypoclorit tạo thành dẫn chất clorhydrin 25.
Ethylen (26) được xử lí với hypoclorit cho ethylenclorhydrin (27). Ngưng tụ 27 với thioure tạo thành 2-iminothiazolidin (18).
Thế nhóm -OH của 25 bằng -C1 với SOC2 sau đó ngưng tụ với 18 thu được tetramisol 16. Cuối cùng là tách các đồng phân quang học để phân riêng levamisol.
Mebendazol (28)
Biệt dược: Vermox, Noverme, Pantelmin.
Tên khoa học: Methyl 5- benzoyl-2-benzimidazol-carbamat
Công thức: C16H13N3O3
Có tác dụng với nhiều loại giun, dùng tẩy giun đũa, giun móc, giun tóc, giun kim, giun lươn, giun xoắn. Cơ chế tác dụng là ức chế sự đồng hóa glucose ở giun gây thiếu hụt ATP và làm giun chết dần.
Tổng hợp mebendazol:
– Gồm 4 giai đoạn:
a, Điều chế 4-amino-benzophenone (34)
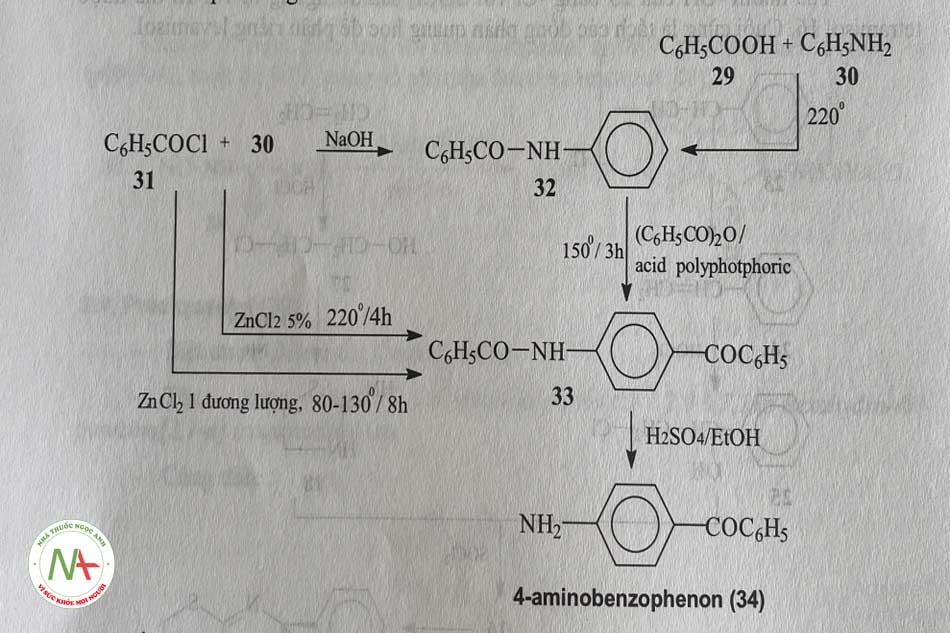
Đầu tiên là bảo vệ nhóm amin của anilin bằng phản ứng amid hóa. Amid 32 thu được khi cho acid benzoic (29) hoặc benzoylclorid (31) phản ứng với anilin (30). Sau đó nó được thế nhóm benzoyl vào vị trí para bằng phản ứng với anhydrid benzoic trong acid polyphosphoric ở 150°c trong 3 giờ. Thủy phân hợp chất 33 với, acid trong alco 1 thu được 4-amino-benzophenon (34).
b, Điều chế 3-nitro-4-amino-benzophenon (36)
Nitro hóa benzophenon (34) bằng acylnitrat ở 40°c thu <Jược dẫn chất 3-nitro (35). Thủy phân 35 loại nhóm acyl tạo thành 3-nitro-4-amino-benzophenon (36).
c, Khử hóa tạo 3,4-diamino-benzophenon (37)
Dẫn chất nitro 36 được khử hóa với Fe trong môi trường nước, xúc tác NH4CI thu được diamin 37.
d, Đóng vòng tạo mebendazol (28)
Diamin 37 được phản ứng với cyan-formamide methyl (38) trong môi trường nước (pH=3-4), nhiệt độ 90°c trong 45 phút thu được mebendazol (28).
Praziquantel (39)
Biệt dược: Biltricide, Droncit, Cesol.
Tên khoa học: 2-(Cyclohexylcarbonyl)-1,2,3,6,7,11b-hexahydro-4H-pyrazino [2,1-a ] isoquinolin-4-on
Công thức C19H24N2O2.
Tính chất: tinh thể màu trắng, nhiệt độ nóng chảy: 136-138°c. Độ tan (g/100ml): ethanol 9,7 ; cloroform 56,7; nước 0,04.
Công dụng: là Ịoại thuốc giun sán mới nhất, trị tất cả cạc loại giun sán. Đặc trị với sán lá phổi, sán gan, ấu trùng sán lợn, sán não.
Liều dùng duy nhất: 10mg/kg trọng lương cơ thể.
Tổng hợp praziquantel:
a, Điều chế 4-(cyclohexul-carbonyl)-2,6-dioxo-piperazin (45)
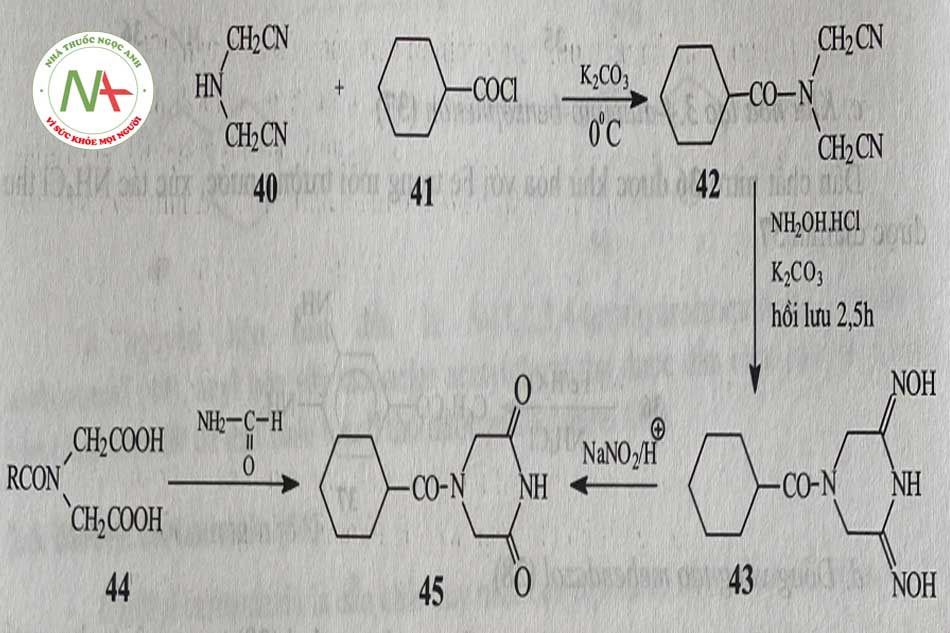
Imonodiacetonitril (40) được ngưng tụ với cyclohexyl-carbonyl-clorid (41) có mặt K2CO3 thu được amid 42. Hồi lưu 42 với hydroxylamin clorhydrat xúc tác K2CO3 tạo thành N-oxim 43. Xủ trí 43 với NANO2 trong môi trường acid thu được 4-(cyclohexyl -carbonyl)-2,6-dioxo-piperazin (45).
Hợp chất 45 còn có thể tổng hợp từ 42 theo cách khác như sau: thủy phân 42 thu được diacetic 44. Sau đó ngưng tụ 44 vơi formamid tạo thành 45.
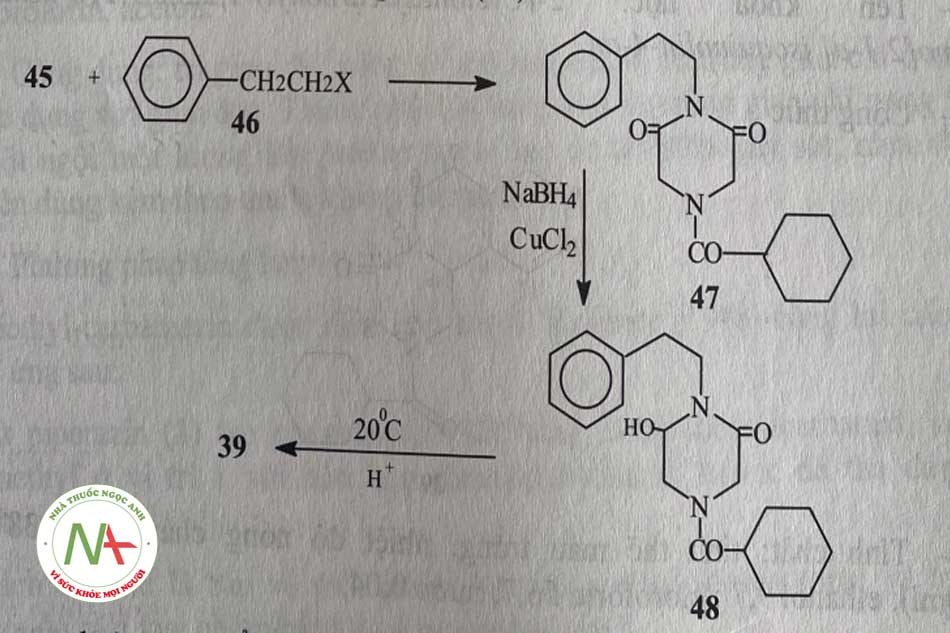
b, Đóng vòng tạo paraziquantel (39)
Ngưng tụ 45 với phenylethyhalogenid (46) thu được hợp chất 47. Khử hóa 47 với NABH4 xúc tác CUCL2 thu được 48. Thực hiện phản ứng đóng vòng loại nước hợp chất 48 ở 20 độ C, xúc tác acid tạo thành praziquantel 39.
Praziquantel còn được tổng hợp theo phương pháp khác theo sơ đồ dưới đây:
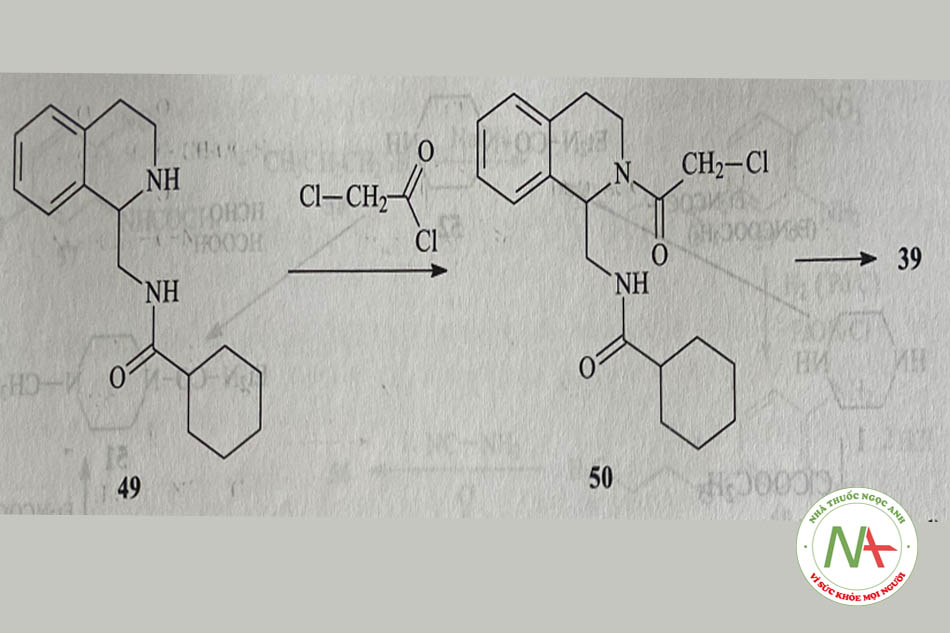
Từ nguyên liệu ban đầu là N-(l,2,3,4-tetrahydroizoquinolin-l-methyl)- carboxamid (49), acyl hóa với monoclor- acetylclorid thu được dẫn chất clor 50. Đóng vòng hợp chất 50 có mặt base mạnh thu được praziquantel (39).
Diethylcarbamazine (51)
Diethylcarbamazin là dẫn chất duy nhất của piperazin được đưa vào điều trị.
Biệt dược : Carbilazine; Caricide; Saponin.
Dạng muối citrat: Banocide; Docid; Franocide; Hetrazan; Long Icid.
Tên khoa học: 1-Dienthy-carbomoyl-4methyl-piperazin
Công thức: C10H21N3O
Tính chất: bột kết tinh trắng, tan trong nước và cồn, không tan trong benzen, ether, cloroform, aceton.
Công dụng: trị giun chỉ, uống sẽ làm mất nhanh ấu trùng giun chỉ ở máu ngoại vi, có tác dụng với giun đũa. Thuốc phá hủy hàng loạt ấu trùng giun chỉ trong máu, giải phóng đột ngột một lượng lớn protein ngoại lai, do đó 90% gây sốt, nhức đầu, buồn nôn… Nên dùng kèm theo thuốc kháng histamin.
Phương pháp tổng hợp:
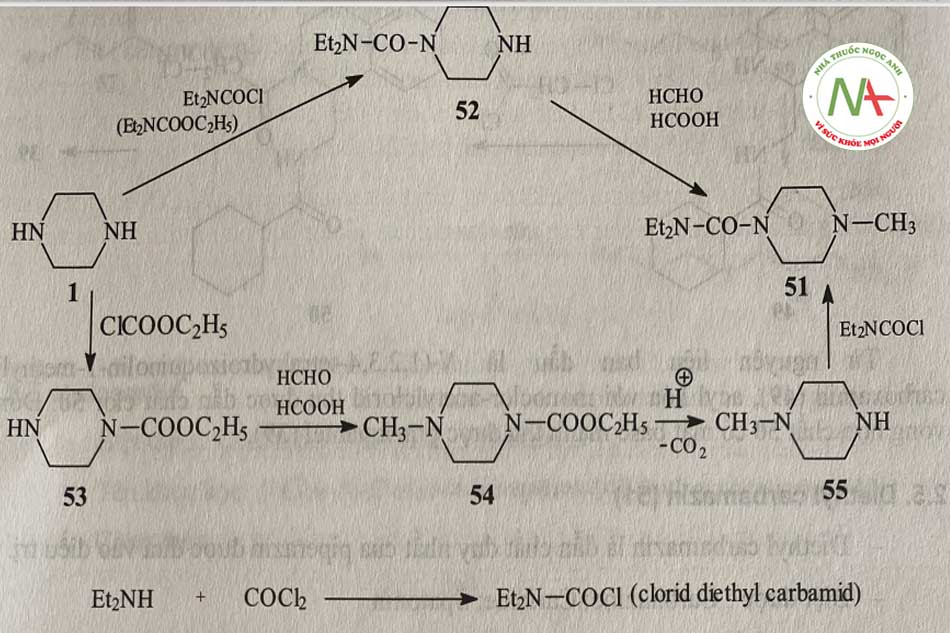
Diethyl-carbamazin được điều chế bởi s. Kushner (1948) bằng hai cách theo sơ đồ phản ứng sau:
Từ piperazin (1) tạo carboxamide (52) bằng clorid-diethyl carbamin, sau đó tạo nhóm methyl ở vị trí 1 với hỗn hợp formaldehyde-acid formic để thu được diethylcarbamazin (51).
Cách thứ hai là bảo vệ một nhóm NH bằng ethyl cloro carbonat và methyl hóa trước, sau đó mới loại nhóm bảo vệ và tạo carboxamide.
Nguyên liệu clorid-diethyl-carbamin được tổng hợp từ diethylamine và photgen.
Albendazol (56)
- Biệt Dược: Albenza, Eskazole, Proftril, Valbazen, Zentel.
- Tên khoa học: Methyl N-[5-(propylthio)-1H-benziimidazol- 2-yl]carbamat.
- Công thức: C12H15N3O2S
- Tính chất: bột kết tinh trắng hoặc không màu. Tan trong acid formic, tan ít trong dicloromethan. Không tan trong nước và ethanol. Nhiệt độ nóng chảy 208-210°c.
- Công dụng: dùng điều trị bệnh nhiễm nhiều loại giun: giun đũa, giun móc, giun tóc, giun kim. Người lớn và trẻ em từ 2 tuổi trở lên uống 1 liều duy nhất 400mg. Trẻ em dưới 2 tuổi uống 1 liều 200mg. Để tẩy giun lươn, sán lợn, sán bò: người lớn và trẻ em từ 2 tuổi trở lên uống 4Ò0mg/ngày X 3 ngày. Trẻ em dưới 2 tuổi uống 200mg/ngày X 3 ngày. Dạng viên nén 200mg, 400mg; hỗn dịch uống 100mg/5ml.
- Phương pháp tổng hợp:
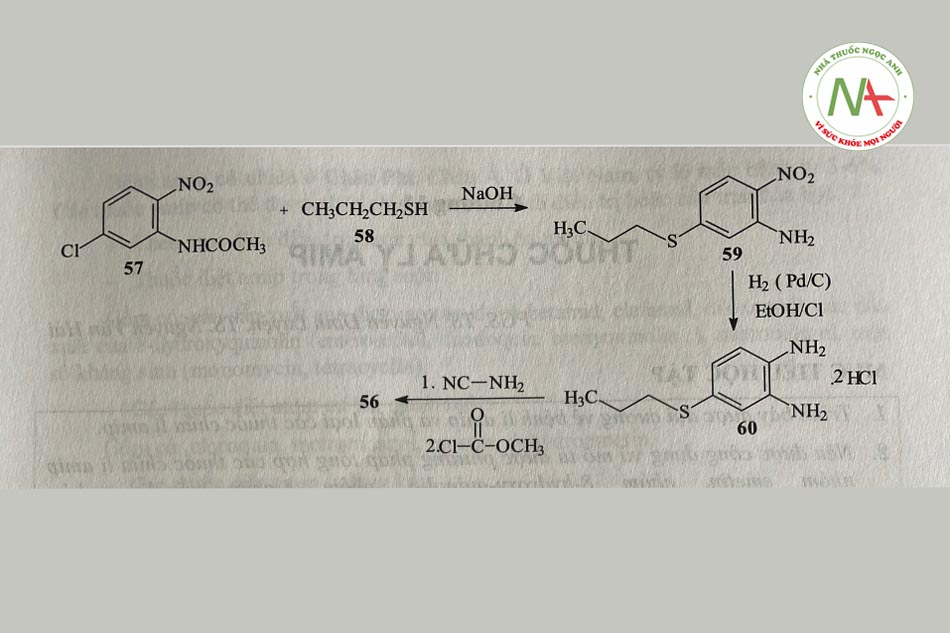
Ngưng tụ 5-chloro-2-nitroacetanilide (57) với propyl mercaptan (58) trong dung dịch nước, có mặt NaOH thu được thioether 59. Khử hóa nhóm nitro của 59 bằng H2 xúc tác Pd/C trong ethanol có mặt HC1 khí tạo thành muối HC1 của phenylendiamin 60. Đóng vòng diamin 60 với cyanamid, sau đó ngưng tụ ngày với methyl cloro carbonat tạo thành benzimidazol 56.
Niclosamid
- Biệt dược: Cestocide, Niclocide, Yomesan..
- Tên khoa học: 5-Clor-N-(2-clor-4-nitrophenyl)-2-hydroxybenzamid (61)
- Công thức: C13H8Cl2N2O4
- Tính chất: Bột kêt tinh màu vàng nhạt. Tan trong aceton, tan ít trong ethanol, cloroform, hầu nhưu không tan trong nước. Nhiệt độ nóng chảy 225-230 độ C.
- Công dụng: Dùng điều trị bệnh nhiễm nhiều laoij sản: Sán bò (Taenia saginata), sán lợn (taenia solium), sán cá (Diphyllobothrium latum), sán sải lùn (Hymenolepis nana).
- Tẩy sán lượn, sán bò, sán cá: người lớn và trẻ em tuef 8 tuổi trở lên uống 1g x 2 lần cahcs nhau 1 giờ vào buổi sáng lúc đói. trẻ em từ 2-7 tuôi liều 2 viên/ ngày, dưới 2 tuổi liều 1 viên / ngày. Dạng viên nén 500mg,
- Phương pháp tổng hợp: Phản ứng tạo amid giữa acid 5-clor-salixylic (62) với 2-clor-4-nitroanilin (63) trong dung môi xylen, có mặt PCl3 thu được niclosamid 61. Sản phẩm được tinh chế bằng cách kết tinh trong ethanol.
Thuốc trừ giun sán
Chi nhánh Công ty cổ phần dược phẩm Phong Phú- Nhà máy sản xuất dược phẩm Usarichpharm
Thương hiệu: Shine Pharma
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công ty cổ phần dược phẩm An Thiên
Thương hiệu: Công ty cổ phần Dược phẩm An Thiên - A.T PHARMA CORP
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công Ty Cổ Phần US Pharma Usa
Thương hiệu: Công ty Cổ phần US pharma USA
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công ty TNHH Liên doanh Stellapharm
Thương hiệu: Công ty Liên doanh StellaPharm – Việt Nam
Xuất xứ: Việt Nam
Thuốc trừ giun sán
STELLA
Thương hiệu: Công ty Liên doanh StellaPharm – Việt Nam
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công ty cổ phần Pymepharco
Thương hiệu: Pymepharco
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công ty cổ phần dược phẩm CPC1 Hà Nội
Thương hiệu: Công ty Cổ phần Dược Phẩm Trung Ương CPC1
Xuất xứ: Công ty cổ phần dược phẩm CPC1 Hà Nội
Thuốc trừ giun sán
Công ty liên doanh Meyer-BPC
Thương hiệu: Công ty Liên doanh Meyer - BPC
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Xuất xứ: Hàn Quốc
Thuốc trừ giun sán
Imexpharm
Thương hiệu: Imexpharm
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công ty Cổ phần Dược phẩm An Thiên
Thương hiệu: Công ty cổ phần Dược phẩm An Thiên - A.T PHARMA CORP
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công ty TNHH Thai Nakorn Patana Việt Nam
Thương hiệu: Thai Nakorn Patana
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Stellapharm
Thương hiệu: Công ty Liên doanh StellaPharm – Việt Nam
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công ty cổ phần dược phẩm SaVi
Thương hiệu: SaViPharm - Công ty Cổ phần Dược phẩm SaVi
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công ty TNHH Dược phẩm Shinpoong Daewoo
Thương hiệu: Shinpoong Daewoo
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Atra Pharmaceuticals Pvt. Ltd
Thương hiệu: APC Pharmaceuticals & Chemicals
Xuất xứ: Ấn Độ
Thuốc trừ giun sán
Thuốc tẩy giun Albendazol 400mg Hataphar (Hộp 1 lọ x 1 viên nhai)
Công ty cổ phần dược phẩm Hà Tây
Thương hiệu: Công ty cổ phần Dược phẩm Hà Tây - Hataphar
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công Ty TNHH Dược phẩm Shinpoong Daewoo
Thương hiệu: Shinpoong Daewoo
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công ty Pharbaco
Thương hiệu: Công ty Dược phẩm Trung Ương 1 - Pharbaco
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công ty TNHH Đạt Vi Phú
Thương hiệu: Davipharm - Công ty Cổ phần Dược phẩm Đạt Vi Phú
Xuất xứ: Việt Nam
Thuốc trừ giun sán
Công Ty CP Dược Phẩm Đạt Vi Phú
Thương hiệu: Davipharm - Công ty Cổ phần Dược phẩm Đạt Vi Phú
Xuất xứ: Việt Nam